皮质基底节变性(CBD)|疑难探究
时间:2023-07-20 21:16:35 热度:37.1℃ 作者:网络
论坛导读:皮质基底节变性(Corticobasal degeneration ,CBD)是一种罕见的神经退行性疾病。CBD最常见的表现是皮质基底综合征(corticobasal syndrome,CBS),这是一组皮质和锥体外系症状和体征。临床病理学研究表明,CBD可以表现出不同的临床表型,包括不流畅、语法缺失的原发性进行性失语综合征、行为、执行障碍和视觉空间综合征,以及进行性核上性麻痹样综合征。相反,多种病理,如CBD、阿尔茨海默病和进行性核上性麻痹可能是CBS患者的基础。这种临床-病理重叠强调了对生物标记物的需要,这将有助于准确诊断CBS患者。
概述
1968年,CBD首次被描述为三例“皮质-齿状回变性伴神经元缺失”,而经典的临床表现被称为皮质-基底综合征(CBS ),直到1989年才被描述。CBS被描述为左旋多巴无反应性帕金森综合征、不对称运动不能/强直、肢体/动眼失用症、肌张力障碍、皮质感觉缺陷、肌阵挛和异肢现象的不同组合。在接下来的几年里,术语皮质基底节变性(CBD)和皮质基底节综合征(CBS)被互换使用,前者指的是一种特定的4-重复(4R)tau病变的病理实体,后者指的是表型。这大大增加了围绕该受试者的困惑,意味着所有的CBD患者都呈现CBS表型,反之亦然。病理标准于2002年建立,临床诊断标准于2013年建立,这进一步增加了不确定性。
临床病理学研究极大地增强对这种罕见的神经退行性疾病的生物化学、遗传学、病理学和临床表现的认识。这些研究表明了CBD的临床多样性,它可以表现为经典的CBS表型,也可以表现为原发性进行性失语症、额叶执行障碍空间综合征和Richardson样综合征。相反,也强调了CBS的病理异质性,各种疾病如CBD、阿尔茨海默病(AD)、进行性核上性麻痹(PSP)和额颞叶变性伴TDP-43 (FTD-TDP43)表现为CBS。CBS是与CBD病理相关的临床表型之一,表现为进行性不对称运动不能强直、左旋多巴反应性差的帕金森综合征,伴有大脑皮质功能障碍。CBD可以表现为几种临床表型,同样,CBS也可以有除CBD以外的病理诊断。
临床病理学研究已经证明,许多CBD患者可以出现其他综合征。其中包括显著的语言障碍,更常见的表现为原发性进行性失语症的非流利语法变异。一些CBD患者表现出额叶行为表型,这与额颞叶痴呆的行为变异不易区分。然而,这些患者通常有额外的视觉空间和视觉结构缺陷,这在行为变异型FTD (bv-FTD)中很少遇到。另一种常见的表型是理查森样综合征,具有明显的核上性麻痹和早期跌倒,以及额叶执行障碍和假性延髓综合征。
CBD主要是一种散发性疾病。据报道,出现了由微管相关tau蛋白(MAPT)突变(ν296ν)引起的家族性病例。该病例中的家族具有CBD的神经病理学特征,但具有伴有显著行为症状的早发性痴呆的临床表型。此外,G389R、p.N410H和P301S MAPT突变在散发性CBS病例中已有描述。LRKK2突变是帕金森病的典型家族病例,也很少表现为CBS [54,55]。前颗粒蛋白(PGRN)突变可以表现为不同的表型,包括CBS。在意大利北部的一个队列中,30%的散发性CBS患者和75%的家族性CBS患者存在PGRN突变。
有趣的是,这个地区家族性CBS的比例极高。据报道,C9orf72基因内含子1中的六核苷酸(GGGGCC)重复扩增通常与FTD-MND谱系障碍有关,并与TDP-43病理有关,也表现为CBS。进行性核上性麻痹(PSP)和CBD可能具有系统性运动神经元TDP-43蛋白病的特性,表明与ALS-TDP有某种联系。由与FUS相互作用改变引起的SFPQ功能障碍可能是共同途径的候选因素。
由于CBD的罕见性、该疾病的巨大临床病理异质性以及直到最近才建立的标准,因此缺乏关于CBD的可靠的流行病学数据。据估计,它比进行性核上性麻痹(PSP)罕见十倍。其发病率估计为0.6-0.9/100,000/年,占帕金森病患者的4-6%。根据发病率和平均存活数据,一项研究预测患病率为每100,000人中4.9-7.3人。然而,在一个120,000的队列中,没有描述CBD的病例。
临床特征
CBD的临床表型以运动、认知和行为特征的多种组合为特征,通常与阿尔茨海默病(AD)或帕金森病相混淆。CBD发病的平均年龄约为64岁,而最年轻的病理确诊病例为43岁。可能会有轻微的女性优势。平均生存期估计为6.5年。其典型临床表现包括不对称帕金森综合征和皮质信号,如失用症、皮质感觉缺失和异体肢体综合征。然而,可能的临床表型变化很大,除了皮质基底综合征(CBS)外,还包括具有空间变化的额叶行为综合征、进行性失语综合征、类似于进行性核上性麻痹(PSP样)的进行性核上综合征,以及经常被误认为AD的主要认知表型。最近的研究表明,CBD可能由不同的病理条件引起,经常导致错误的诊断。
目前的共识标准描述四种CBD表型:
-
皮质基底综合征(CBS)、
-
额叶行为空间综合征(FBS)、
-
原发性进行性失语的非流畅性/语法变异型(nfvPPA)
-
进行性核上性麻痹综合征(PSPS)。
CBS以皮质和锥体外系体征为特征。失用症、皮质感觉缺陷和异肢现象是最常见的皮质体征,而不对称帕金森综合征、肌张力障碍和肌阵挛包括锥体外系体征。
CBS中的帕金森综合征具有高度不对称或单侧的特征。很少有对称皮质基底节变性的报道。少数患者可出现中度但短暂的左旋多巴反应。当存在震颤时在表现上是非典型的。它通常是一种位置性或动作性震颤,可以是不规则的,通常具有肌阵挛性。还描述了典型的左旋多巴诱导的运动障碍,类似于帕金森病。
40%的CBD患者存在肌张力障碍。约80%的患者有上肢肌张力障碍,而颈部,下肢肌张力障碍和眼睑痉挛是罕见的。通常肌张力障碍出现在病程的前两年,并与肌阵挛高度相关。肌阵挛似乎是皮层反射类型,基于巨大的体感电位和脑电图与肌电图之间的潜伏期。CBD中的肌阵挛被假设为由于缺乏来自感觉皮层的抑制性输入而导致初级运动皮层的异常过度兴奋。在CBD病例中缺乏巨大的体感电位被归因于CBD晚期的严重顶叶萎缩。
失用症是CBS的临床标志。虽然被认为是CBD的相对特异性,但一些失用症研究认为,多达75%的PSP患者和30%的PD患者存在失用症。然而,定量分析表明,失用症的严重程度存在差异(特别是在不及物运动中)。此外,定性分析,包括错误类型分析,也可以区分这两种疾病。CBD患者的远端失用比近端失用更严重,这支持了肢体运动性失用的观点。
异己体综合征(alien-limb syndrome)最初被描述为一种识别自己肢体的主观困难,特别是在缺乏视觉输入的情况下。它可以分为后部或感觉变体,与感觉半忽略有关。可能出现手或手臂抬高,这通常是位置依赖性的,可由感觉刺激诱发。病人有一种手臂不属于他的感觉。前部或运动变体的特征是极端的利用和抓握行为,更常见的是优势手,这可能导致手与手之间的冲突(即一只手无意地干扰或甚至阻碍另一只手的有目的的运动)。报道了一种双侧不对称异体肢体综合征。
更罕见的表现还可包括具有遗忘表型(AD样)的痴呆、进行性口面失用症、具有显著重复困难的传导型失语症、后部皮质萎缩症、视神经共济失调、动眼失用症和共视症、前额型步态障碍和具有构音障碍和情绪不稳定的显著假性延髓综合征。CBD还可能具有快速进展的临床过程,类似于免疫介导的脑干脑炎等其他神经系统疾病。
影像学特征
CBD的MRI影像学标志是不对称的皮质萎缩,这种萎缩在中脑周围区域(中央前回和中央后回)、额叶和顶叶后部,对侧为临床上受影响更严重的一侧。随着疾病的进展,皮质萎缩不对称变得更加明显。在80%的患者中,最大萎缩区域的质子密度MRI序列信号异常增加。这可能代表继发于轴突损伤而非胶质增生的脱髓鞘。基底神经节萎缩也可能存在,在T2加权图像中信号异常增加,特别是在壳核的后外侧缘。中脑萎缩,以及胼胝体萎缩,更突出的后方也可以明显。“虎眼”征被认为是泛酸激酶相关神经变性的特征性表现,也曾在CBD患者中出现过。
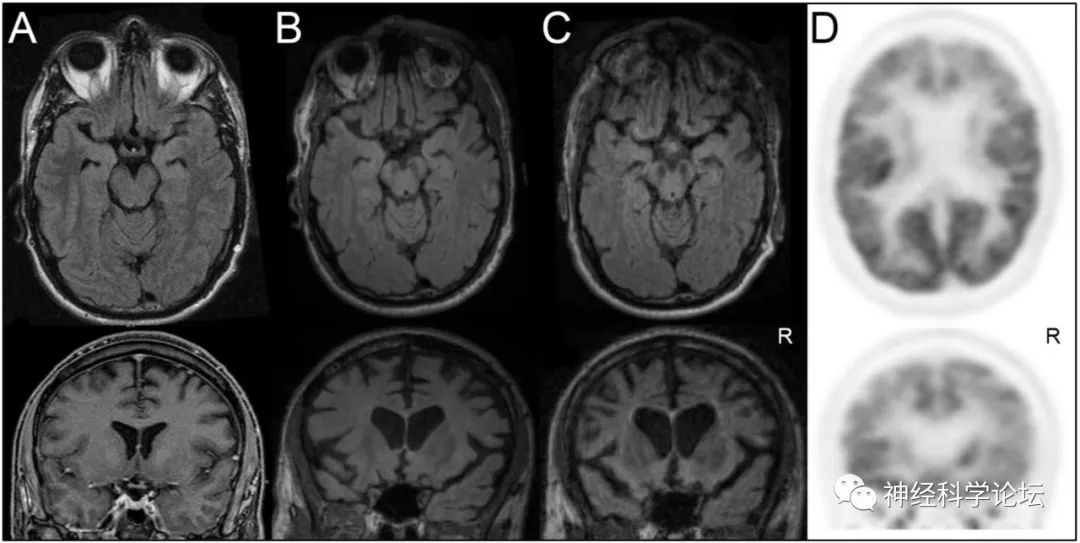
T2 FLAIR轴向/冠状脑磁共振成像。连续成像显示右侧比左侧更严重,以背外侧为主的额顶体积损失,伴有眶额、尾状核和内侧颞区的局灶性萎缩。FDG-正电子发射断层扫描大脑成像显示主要的背侧比腹侧前额叶新陈代谢减少(Neurocase. 2021 Apr;27(2):120-128. )
功能成像模式已经被用于帮助非典型帕金森综合征的鉴别诊断,以及试图表征CBS患者的潜在病理。使用[123 I]碘苯丙胺-SPECT的灌注研究表明,与PSP相比,CBS患者的下前额叶、感觉运动和后顶叶皮质的灌注降低。基底神经节灌注不能区分这两种疾病。与PSP相比,CBD患者的rCBF降低更广泛和不对称,两种疾病共享内侧额叶受累。同样,通过使用99mTc HmPaO SPECT,CBD患者可以与PD患者区分开来,因为CBD患者在颞下区、颞顶区和额内侧区表现出灌注减少。
诊断标准
多年来提出了各种诊断标准,专门针对CBD的CBS表现。2013年推出的最新临床诊断标准旨在通过纳入不同的临床表型来扩展CBD的表型谱。这些标准基于CBD的临床病理学研究,并试图说明CBS和CBD的巨大临床病理学差异。


基于这些标准,五种临床综合征被接受为CBD。这些包括可能的CBS额叶行为和空间综合征(FBS);一种非流利语法原发性进行性失语综合征(NFA-PPA);和进行性核上麻痹样综合征(PSPS)。可能的CBD诊断要求发病年龄大于50岁,而家族史或已知的影响tau蛋白的基因突变是不允许的。在这五种表型中,只有可能的CBS和FBS以及nfa-PPA(增加了CBS特征)符合可能的CBD诊断。对于可能的CBS诊断,标准更宽松。对发病年龄没有要求,允许有阳性家族史或已知的tau蛋白突变。可能的CBD诊断可以通过可能的CBS表型、FBS或nfa-PPA综合征(没有额外的CBS特征)或具有额外CBS特征的PSP-S来确定。
总之,CBD以皮质基底节综合征(CBS)为特征,伴有不对称失用症、强直、肌张力障碍和肌阵挛。只有在尸检时才能做出明确诊断,CBD可能表现为各种临床表型,包括CBS、额叶行为空间综合征、非流利性原发性进行性失语和Richardson综合征(RS)。事实上,尽管CBS是CBD病理最常见的表型,但23.3%经病理证实的CBD病例显示存在与姿势不稳定或早期跌倒、轴向或对称肢体僵硬或运动不能、尿失禁、行为问题以及垂直扫视受限或减慢相关的RS。目前,没有临床特征或影像学发现可以将CBD与其他病理区分开来,鉴于这些表型也与非CBD病理相关,对这些表型的明确诊断依赖于神经病理学。
治疗方法
CBD是一种散发性tau蛋白病,表现为运动、认知和行为特征的各种组合,使其诊断困难。CBD发病率高,预后差,目前尚无有效的根治方法。对症治疗有助于改善运动症状(帕金森综合征、肌张力障碍、肌阵挛),但效果通常不令人满意。为了处理与CBD相关的行为表现,对症状进行有效的药物干预,旨在提高患者的生活质量。由于目前缺乏可用的药理学替代方案,没有针对CBD患者的多学科整合治疗成分的药理学策略或姑息治疗。目前可用药物的低疗效可能与广泛分布的病理变化有关,这解释了CBD临床表现的多样性和复杂性。最近的神经病理学和生理病理学发现对CBD有了新的认识,但是还没有找到针对这种疾病的改良疗法。
参考文献
Riku Y, et al. Motor neuron TDP-43 proteinopathy in progressive supranuclear palsy and corticobasal degeneration. Brain. 2022 Aug 27;145(8):2769-2784.
Constantinides VC, et al. Corticobasal degeneration and corticobasal syndrome: A review. Clin Park Relat Disord. 2019 Aug 30;1:66-71.
Rini J, et al. Genetic pleiotropy and the shared pathological features of corticobasal degeneration and progressive supranuclear palsy: a case report and a review of the literature. Neurocase. 2021 Apr;27(2):120-128.
刘春风, 陈生弟, 陈海波, 等. 皮质基底节变性诊断标准及治疗中国专家共识. 中国神经免疫学和神经病学杂志. 2019. (04): 240-245.
Saranza GM,et al. Corticobasal degeneration. Int Rev Neurobiol. 2019;149:87-136.
Moura J, et al. Rapidly Progressive Corticobasal Degeneration Mimicking Brainstem Encephalitis. Mov Disord Clin Pract. 2022 Dec 15;10(2):300-306.
Bayram E, et al. Pathology-Proven Corticobasal Degeneration Presenting as Richardson's Syndrome. Mov Disord Clin Pract. 2020 Feb 14;7(3):267-272.


