胃食管反流病治疗新选择:盐酸凯普拉生片
时间:2023-04-03 14:02:05 热度:37.1℃ 作者:网络
胃食管反流病(GERD)在全球的发病率高达13.3%【1】,其临床特征是胃与十二指肠内容物反流进入食管后引起的胃灼热和反流等症状。GERD可被分为非糜烂性胃食管反流病(NERD)、糜烂性食管炎(EO)和巴雷特食管(BO),其中EO和BO更为严重【2】。
目前EO的主要治疗药物是质子泵抑制剂(PPI),但PPI在EO治疗中的需求尚未被满足。PPI在高级别EO患者中的抑酸效果不佳【3】,其疗效依赖于CYP2C19的多态性,且只能与活化态的质子泵结合【4】,需餐前服用可能导致患者依从性较差。
凯普拉生是一种新型的口服钾离子竞争性酸阻滞剂(P-CAB)。与PPI不同,凯普拉生在酸性环境中稳定、可溶于水,并能与静息态和活化态的质子泵结合。临床前和I期研究已经证明其稳定性和强抑酸能力以及良好的安全性【5-7】。II期研究表明凯普拉生20mg每日一次治疗十二指肠溃疡有效,且非劣效于兰索拉唑【8】。这项III期研究旨在探讨与兰索拉唑相比,凯普拉生治疗EO的非劣效性和安全性【9】。
研究设计/流程
这是一项多中心、随机、双盲、双模拟、平行对照III期非劣效研究。2020年8月-2021年4月中国44个中心共计入组240名(18-75岁)患者,在随机分组的7天内内镜确诊为EO(LA分级A-D)。240名患者根据LA分级A/B或C/D按照1:1随机分别接受凯普拉生(120名)20mg/天,和兰索拉唑(120名)30mg/天,持续4-8周。受试者将接受至少4周的持续治疗,如果在第4周通过内镜检查证实食管炎黏膜愈合,则停止治疗。如果没有,治疗将延长4周,总治疗期为8周。主要疗效终点为治疗8周内的EO愈合率。
研究设计的流程图
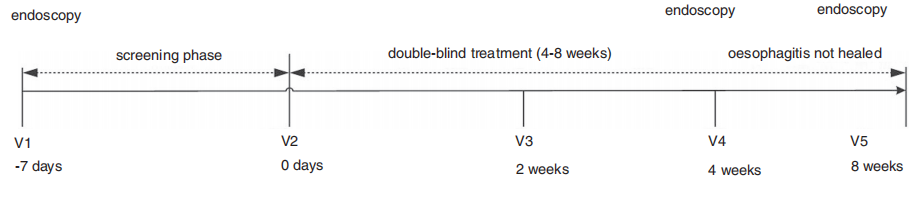
样本量设计及统计分析
根据主要终点假设两组8周黏膜愈合率均为95%,退出率为20%,预计每组120名患者可提供80%的能力来监测非劣效性,边际为−10% (单侧α=0.025)。亚洲国家的胃食管反流负担相对较低。据估计,重度食管炎占所有食管炎的1%-13%。因此,本研究将LA分级为C/D级的患者比例设定为≥20%,足以覆盖临床实践中高级别食管炎的患病率。
主要和次要疗效终点使用全分析集(FAS)和符合方案集(PPS)进行分析。使用安全性分析集(SAS)分析安全终点。
研究结果-有效性
01 8周EO黏膜愈合率
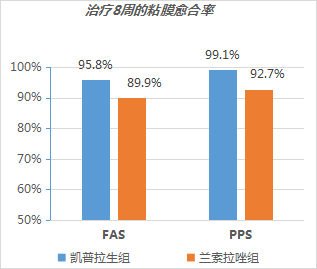
FAS分析显示,凯普拉生组和兰索拉唑组的8周EO黏膜愈合率分别为95.8%和89.9%,组间差异:5.8%;P= 0.081。
PPS分析显示,凯普拉生组的8周EO黏膜愈合率显著高于兰索拉唑组[凯普拉生组 vs. 兰索拉唑组= 99.1% vs. 92.7%; 组间差异: 6.1% ; P= 0.018。
对于主要终点,FAS和PPS分析均证实了凯普拉生与兰索拉唑相比的非劣效性。
02 4周EO黏膜愈合率
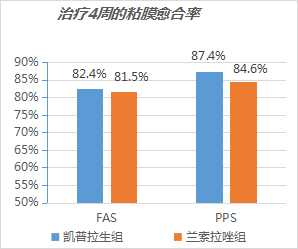
在FAS分析中,凯普拉生组和兰索拉唑组的4周EO黏膜愈合率无显著差异[凯普拉生组 vs. 兰索拉唑组=82.4% vs. 81.5%;P=0.898。
PPS分析也显示,凯普拉生组和兰索拉唑组的4周EO黏膜愈合率无显著差异[凯普拉生组 vs. 兰索拉唑组= 87.4% vs. 84.6%; P=0.608。
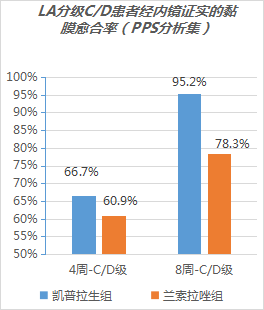
03 LA分级C/D患者-EO黏膜愈合率
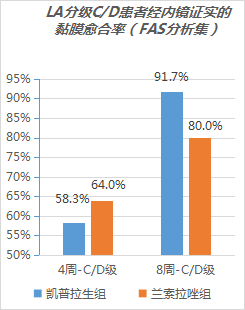
对于基线LA分级C/D的患者,FAS及PPS分析均显示凯普拉生组和兰索拉唑组的4周EO黏膜愈合率无显著差异(FAS:凯普拉生 vs. 兰索拉唑= 58.3% vs. 64.0%; P= 0.684)(PPS:凯普拉生 vs. 兰索拉唑= 66.7% vs. 60.9%;P= 0.690)。
凯普拉生组8周的EO黏膜愈合率数值高于兰索拉唑组。 (FAS: 凯普拉生 vs. 兰索拉唑= 91.7% vs. 80.0%;P= 0.417) (PPS: 凯普拉生 vs. 兰索拉唑= 95.2% vs. 78.3%;P= 0.188)。
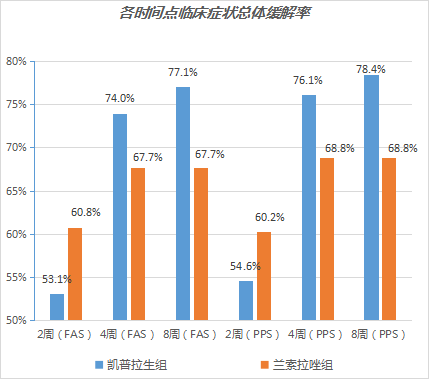
04 临床症状总体缓解率
对于EO相关的胃灼热、反流等临床症状,在治疗2周、4周、8周时,凯普拉生组与兰索拉唑组在发生频次和严重程度上的改善率无显著性差异。
治疗后第2周、第4周和第8周,凯普拉生组和兰索拉唑组的胃灼热、反流缓解率以及总体临床症状具有可比性。
安全性
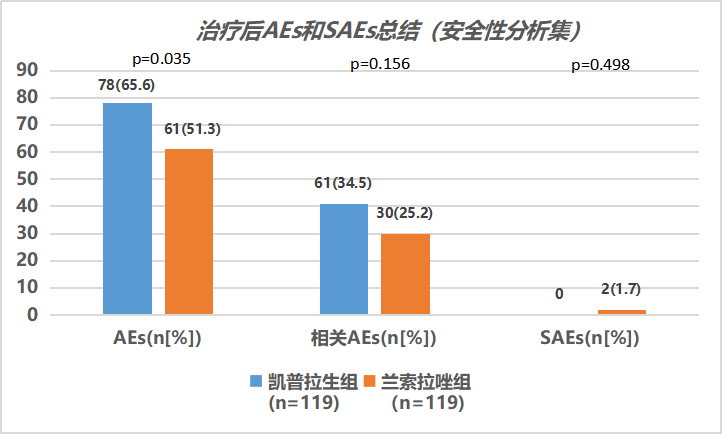
AEs的总体发生率为58.4% (在凯普拉生组为65.6%,兰索拉唑组为51.3%,P=0.035)。
药物相关AEs在凯普拉生组为34.5%,兰索拉唑组为25.2%,P=0.156,两组之间无显著性差异。凯普拉生组没有发生严重不良事件(SAE),而兰索拉唑组有2例发生SAE(1例为系统性硬化症;1例为结直肠息肉;均与药物无关)。
治疗后AEs和SAEs总结(安全性分析集)
研究结论
本研究证实,凯普拉生治疗EO的疗效非劣效于兰索拉唑。药物相关不良事件的发生率在凯普拉生和兰索拉唑之间相当。
- 参考文献 -
1. Eusebi LH, Ratnakumaran R, Yuan Y, Solaymani-Dodaran M, Bazzoli F, Ford AC. Global prevalence of, and risk factors for, gastro-oesophageal reflux symptoms: a meta-analysis. Gut. 2018;67(3):430–40.
2. Maret-Ouda J, Markar SR, Lagergren J. Gastroesophageal reflux disease: a review. JAMA. 2020;324(24):2536–47.
3. Scarpignato C, Gatta L, Zullo A, Blandizzi C. Effective and safe proton pump inhibitor therapy in acid-related diseases - a position paper addressing benefits and potential harms of acid suppression. BMC Med. 2016;14(1):179.
4. Horn JR, Howden CW. Review article: similarities and differences among delayed-release proton-pump inhibitor formulations. Aliment Pharmacol Ther. 2005;22(Suppl 3):20–4.
5. Li R, Zhou H, Ding Y, et al. Safety pharmacology study of carenoprazan hydrochloride. J Nanjing Univ Nat Sci. 2020;42(1):129–34. (In Chinese).
6. Li R, Hou Y, Qiao H. Genotoxicity study of carenoprazan hydrochloride, a novel potassium-competitive acid blocker. J Toxicol. 2019;33(5):428–30. (In Chinese).
7. Cai M, Shu B, Shao Q, et al. Embryo-fetal development toxicity of carenoprazan hydrochloride. J China Pharm Univ. 2018;49(6):725–30. (In Chinese).
8. Author Name Is Multiple. An international forum for clinical practice and research in gastroenterology Abstract issue 29th United European Gastroenterology Week Virtual 2021 Abstracts (THE EFFICACY AND SAFETY OF H008 COMPARED WITH LANSOPRAZOLE IN PATIENTS WITH DUODENAL ULCER [DU]: A PHASE II, RANDOMIZED, DOUBLE-BLIND, DOUBLE-DUMMY, PARALLEL MULTICENTER STUDY IN China). United Eur Gastroent J. 2021;8(S1):8-U899.
9. Chen, Songfeng et al. The efficacy and safety of keverprazan, a novel potassium-competitive acid blocker, in treating erosive oesophagitis: a phase III, randomised, double-blind multicentre study. Alimentary pharmacology & therapeutics vol. 55,12 (2022): 1524-1533.


