CHC 2023:内皮细胞代谢与心血管修复
时间:2023-09-02 13:58:48 热度:37.1℃ 作者:网络
由国家心血管病中心、《中国循环杂志》社有限责任公司、北京楷祺心血管公益基金会三方联合主办的中国心脏大会(CHC)2023 暨第届中国血管大会(CVC)暨第三届中国健康生活方式医学大会于2023年8月1日-9月3日采用线上线下相结合的形式举办。
本次大会,来自于复旦大学附属中山医院的孙爱军教授跟大家分享《内皮细胞代谢与心血管修复》。小编整理重点分享给各位。

目前,外周动脉血管疾病发病率非常高,据统计全球的患病人数达到两亿且预后不佳。

在最近进行的一项研究中目的是确定调节性T细胞调控下肢缺血后血流恢复的关系。以往文献表明,Treg细胞能促进下肢缺血后血管新生血流恢复。

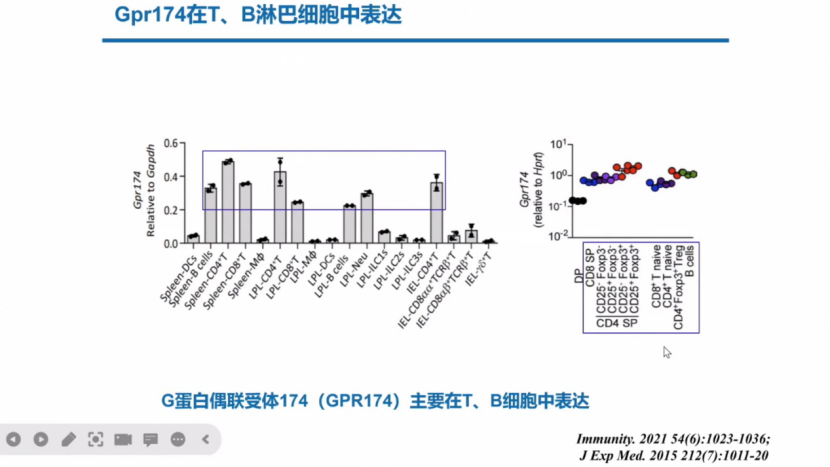
Gpr174主要在T、B细胞中表达并且表达性非常高。
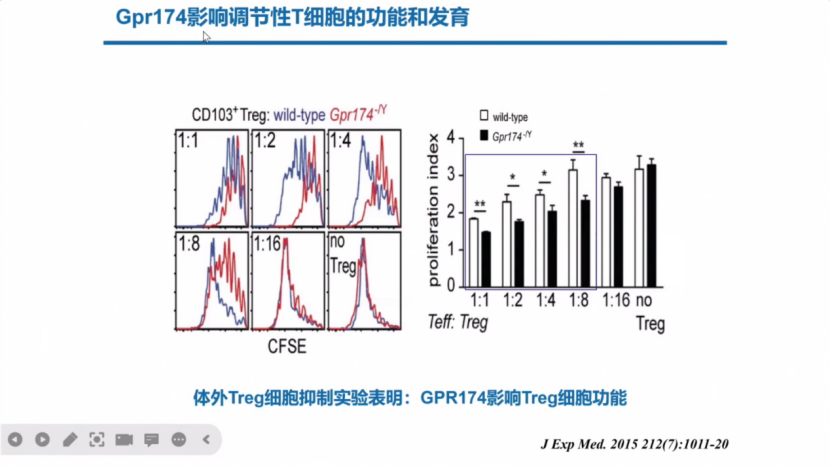
以往研究报道Gpr174影响调节性T细胞的功能和发育。
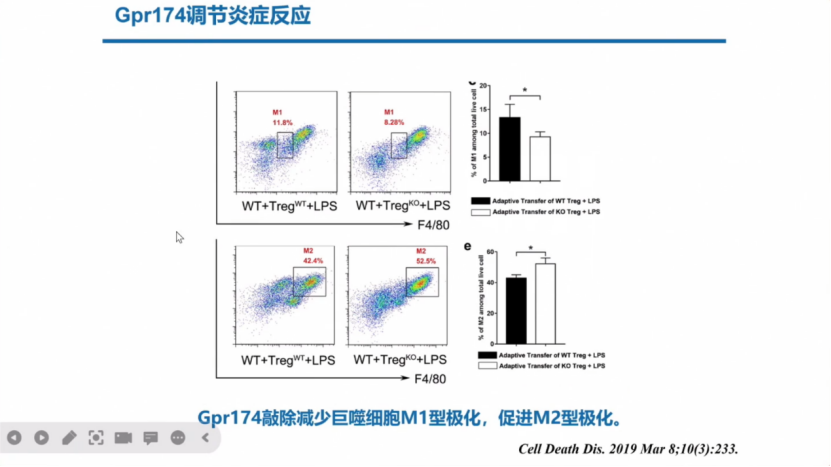
Gpr174可以调节炎症反应,敲除后会减少巨噬细胞M1型极化,促进M2型极化。
基于以上发现,提出科学设想,Gpr174是否参与调控下肢缺血后血流恢复?

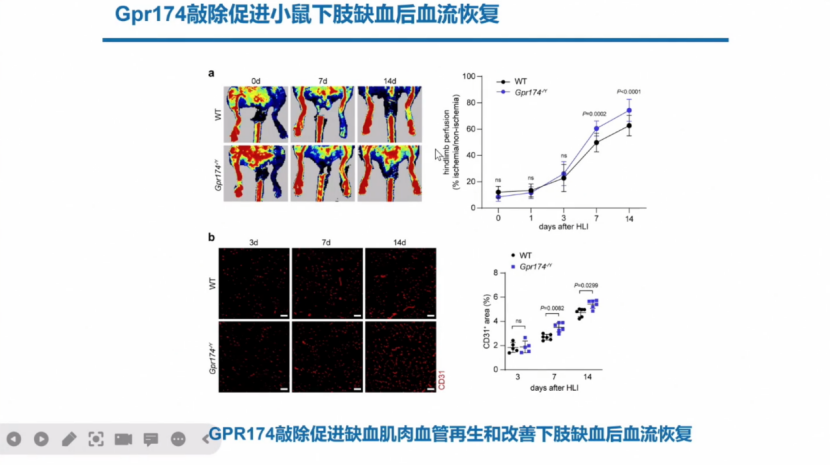
首先在Gpr174全敲除的小鼠中发现能促进小鼠下肢缺血后血流恢复。多普勒显示小鼠下肢血流恢复显著改善。
而在下肢缺血损伤后,调节性T细胞中Gpr174表达明显升高。
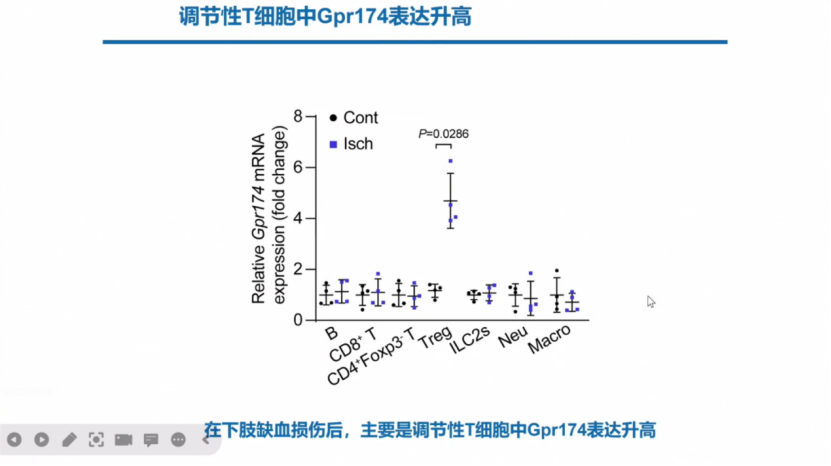
研究对比发现,Gpr174敲除的Treg细胞促进血流恢复的作用比野生型更明显。

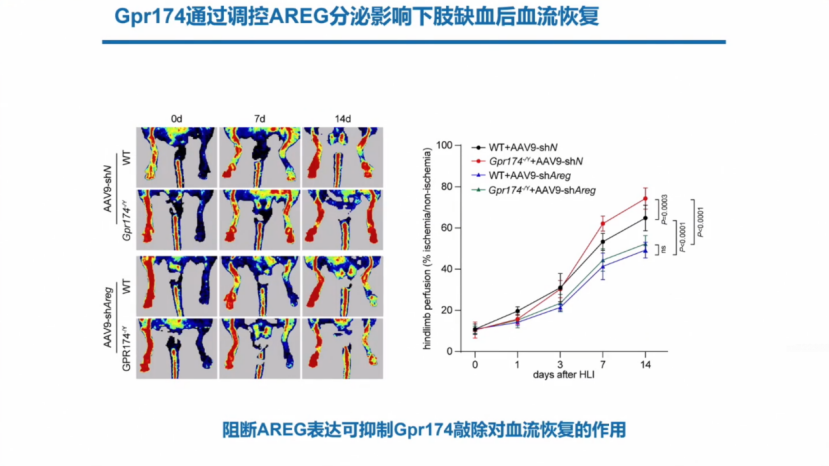
通过基因组学分析发现,下肢缺血后,Gpr174敲除可以促进Treg细胞中AREG的表达,而以往报道说明双调蛋白 (AREG)能够改善肌肉损伤恢复。

当把小鼠AREG蛋白阻断之后,Gpr174敲除对血流恢复的作用被削弱。
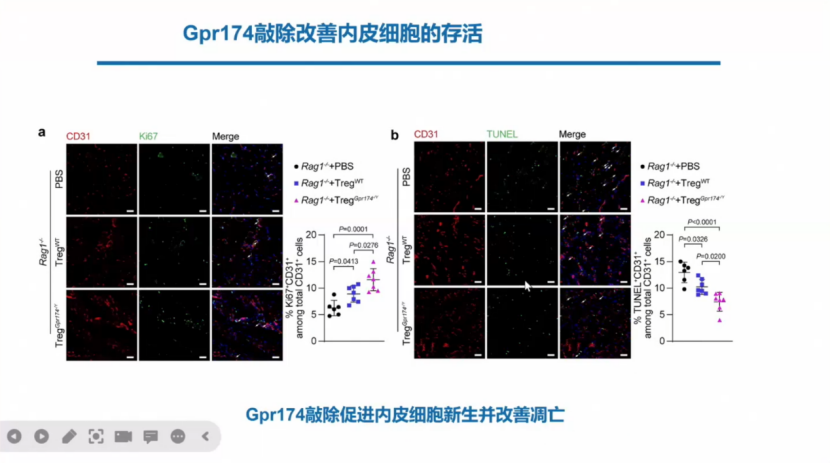
Gpr174的敲除有两方面的作用,一方面能够促进内皮细胞新生并改善凋亡。
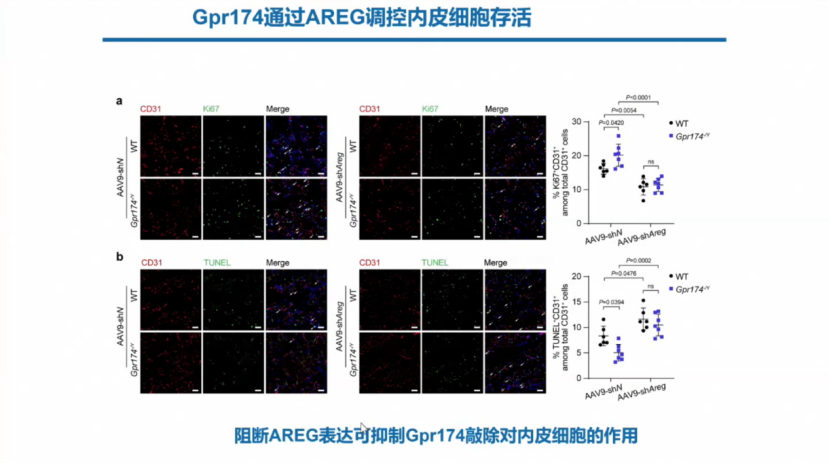
而阻断AREG表达可抑制Gpr174敲除对内皮细胞的作用。
另外一方面Gpr174敲除可以减少巨细胞M1型极化、促进M2型极化。
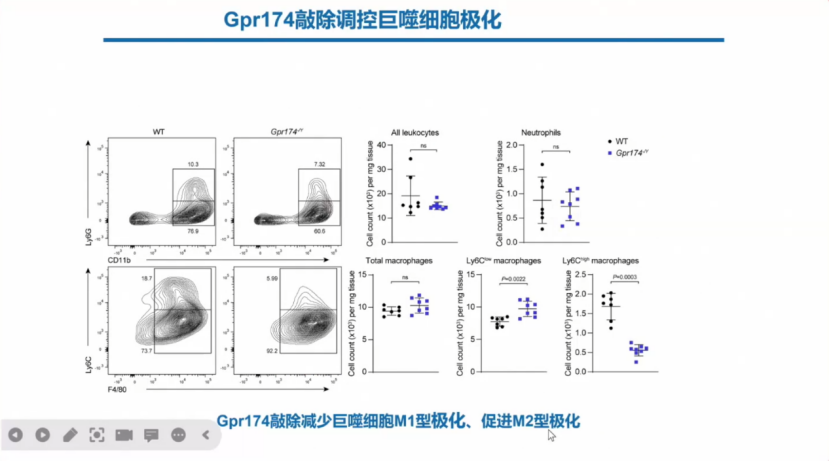
而当阻断AREG后,Gpr174敲除对巨噬细胞的极化作用被抑制。

在下肢缺血后,Treg细胞中Gpr174敲除可以促进EGR1进入细胞核。

Gpr174通过EGR1调控AREG的表达。
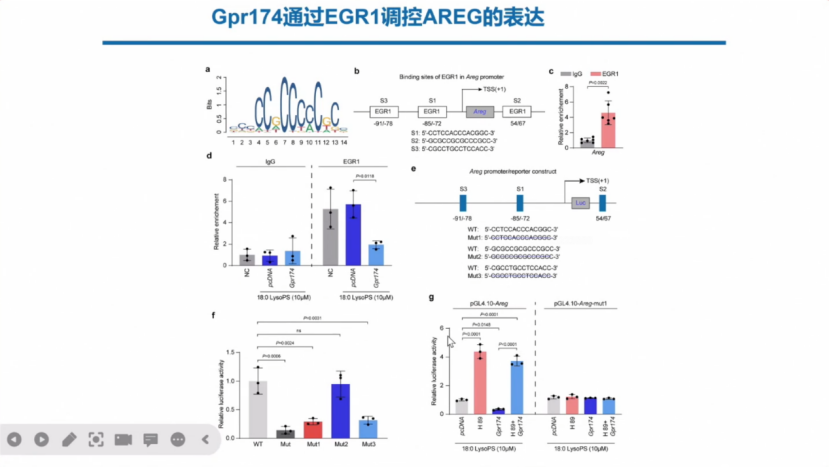
小结
在下肢缺血模型中,Gpr174敲除后可以促进EGR1向细胞核内转运,再促近AREG的转录生成,然后促进血管新生改善下肢缺血后血流灌注。

在下肢缺血模型中,给微血管内皮细胞施加缺氧干预后发现,缺氧导致CMECs整体m6A修饰发生显著下调,而去甲基化酶ALKBH5在缺氧CMECs中显著高表达。

进一步研究证实,当敲低ALKBH5后m6A甲基化上调,促进微血管内皮的新生。
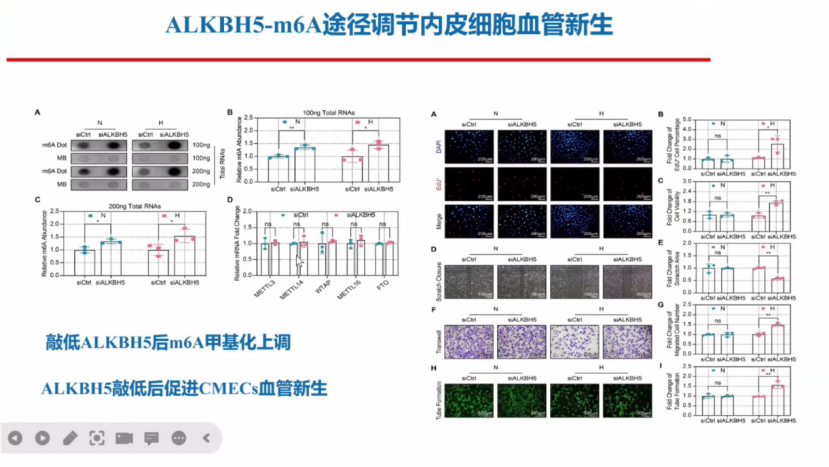
具体的机制是通过MeRIP-qPCR检测发现,当敲低ALKBH5后可以促进WNT5AmRNA m6A修饰的上调,WNT5A mRNA稳定性增加降解过程收到抑制。
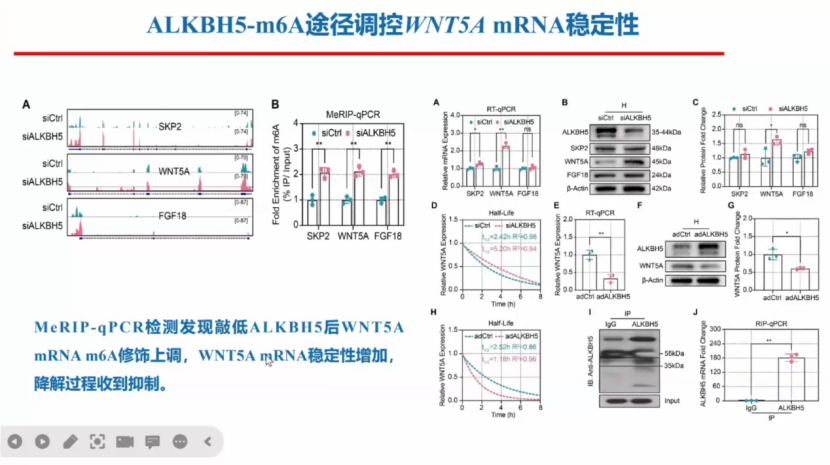
敲除ALKBH5后可以促进缺血下肢血流恢复及血管生成,靶向ALKBH5抑制具有潜在的转化和治疗意义。
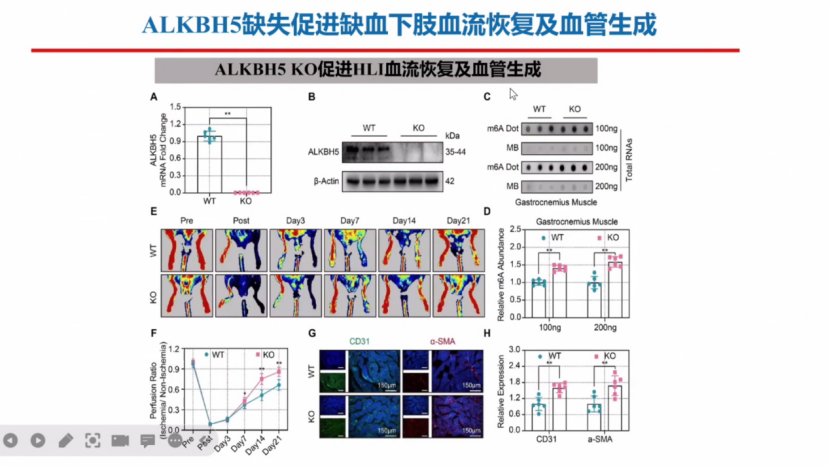
在RNA甲基化研究方面证实了ALKBH5-m6A-WNT5A途径在血管新生调控中的具体机制,靶向ALKBH5抑制具有潜在的缺血性疾病治疗转化意义。

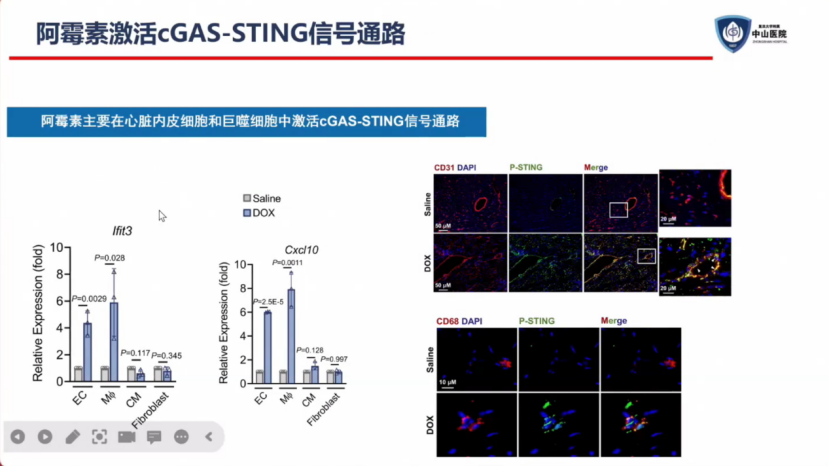
在内皮细胞新近研究中发现,阿霉素能够显著激活小鼠心脏组织CGAS-STING信号通路。

进一步通过细胞各个阻断的分析发现,内皮细胞和巨噬细胞中CGAS-STING信号通路显著增强。
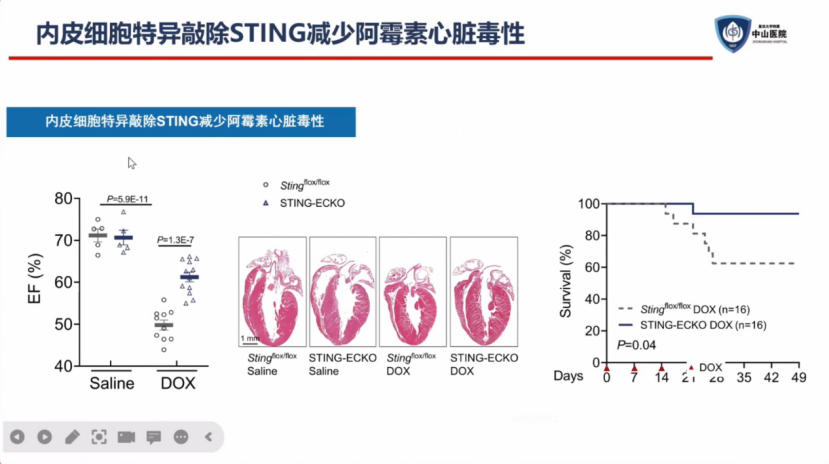
内皮细胞特异敲除STING之后发现,可以减轻阿霉素的心脏毒性,心脏射血分数和生存率得到显著改善。
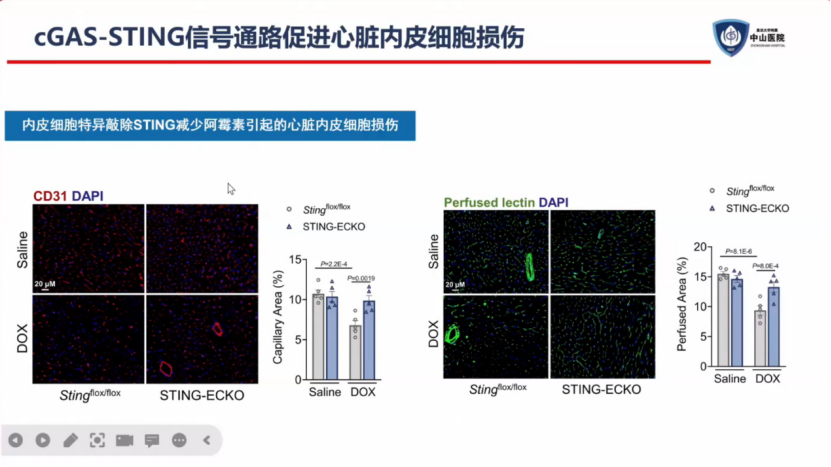
在细胞层面研究也发现,当内皮细胞特异敲除STING以后可以减少阿霉素引起的心脏内皮细胞损伤。
阿霉素激活CGAS-STING信号通路后通过下游受体又激活CD38水解酶,随着DOX作用时间延长CD38水解酶持续升高,NAD水平显著减少。

不但内皮细胞因为NAD下降功能收到显著影响,而且内皮细胞CGSA-STING通过CD38胞外端影响心肌细胞和内皮细胞间隙中的NMN和NAD水平下降,进而影响心肌细胞内NAD水平下降,导致心肌细胞损伤。

通过使用CGAS-STING通路抑制剂发现阿霉素心脏毒性显著减少,改善心脏功能,增加存活率。
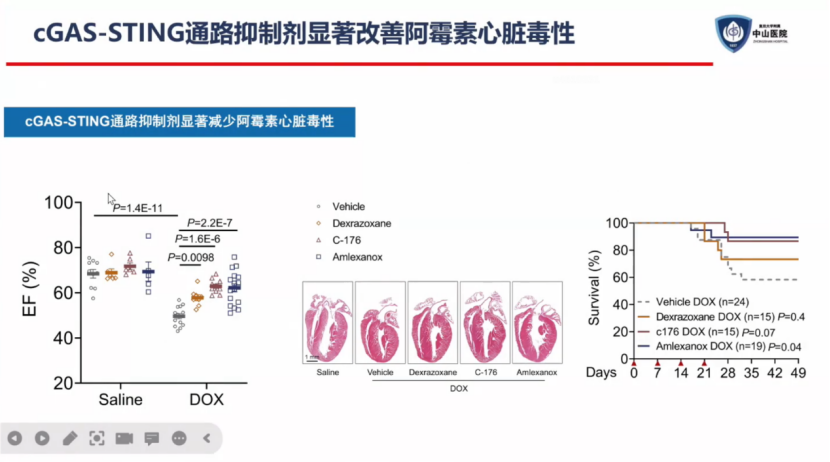
使用TBK1和CD38抑制剂发现,两种抑制剂都可以改善阿霉素心脏毒性,并且与CGAS-STING通路抑制剂相比可以保证阿霉素抗肿瘤效率。


