NEJM evid:儿童2型糖尿病中,达格列净和沙格列汀,选择哪个更合适?(T2NOW研究)
时间:2023-10-05 08:17:57 热度:37.1℃ 作者:网络
全球儿童和青少年2型糖尿病(T2D)的发病率和患病率不断上升,尤其在非白人、种族多样的亚群体中受到了不成比例的影响。在美国,有研究显示T2D的发病率每年增加7.1%,而在种族多样的亚群体中增幅更高。儿童或青少年患上T2D时,病情可能表现出更具侵袭性的特征,病程进展更快,并且并发症的发生比成人患者更早。TODAY(青少年和青少年2型糖尿病的治疗选择)和ADOPT(糖尿病结局进展试验)研究表明,在10至19岁的患者中,β细胞功能每年下降20%至35%,而在成人中下降7%至11%。这种快速下降的后果可能是疾病的恶化和早期需要外源胰岛素。此外,青少年患T2D的治疗失败时间较短,也反映了疾病进展的迅速性。
目前,儿童和青少年的批准治疗方法较少。可注射的胰高血糖素样肽-1受体激动剂(GLP-1 RA),如一日一次的利拉鲁肽和一周一次的艾塞那肽,已经被美国食品和药物管理局以及欧洲药品管理局批准用于10岁及以上的儿童,根据它们各自的第3阶段研究结果。鉴于注射疗法普遍存在的黏附问题,这在年轻患者中可能进一步加剧,因此需要更多的口服治疗选择。
钠-葡萄糖共转运蛋白-2(SGLT-2)抑制剂达格列净是自二甲双胍以来首个获得欧洲药品管理局批准用于10岁及以上儿童的口服治疗药物,根据在北美、拉丁美洲和欧洲进行的10至24岁患者的关键第3阶段试验结果。这项试验包括53名10至17岁的患者(其中29名被随机分配到达格列净组,24名分配到安慰剂组),其余患者(总共19名)年龄为18至24岁。仅有14%的患者来自非白人/黑人/非洲裔美国人群体,因此并不完全代表全球主要受到T2D影响的人群。最近进行的DINAMO(利格列汀和恩格列净治疗儿童和青少年糖尿病研究)第3阶段试验评估了恩格列净(SGLT-2抑制剂)和利格列汀(二肽基肽酶-4 [DPP-4]抑制剂)与单一安慰剂组相比,在T2D患儿中的疗效。厄帕格列净实现了A1C变化的主要终点,而利格列汀没有。低血糖是活性治疗中报告最频繁的不良事件,患者在接受恩格列净治疗的26周内观察到的患者数量较多,与安慰剂相比(总体低血糖:12例[23%] vs. 5例[9%];血浆葡萄糖<3mmol/l [<54mg/dl],表示临床上重要的低血糖:10例[19%] vs. 4例[8%])。
在这里,我们描述了T2NOW试验的结果,该试验比较了SGLT-2抑制剂(达格列净)和DPP-4抑制剂(沙格列汀),与单一安慰剂进行对照的随机对照试验。
这是一项为期 26 周、多中心、双盲 3 期试验,具有 26 周双盲安全延长期。入组的患者年龄为 10 至 17 岁,糖化血红蛋白 (A1C) 为 6.5 至 10.5%,接受饮食、运动和稳定剂量的二甲双胍(≥1000mg)、胰岛素或二甲双胍(≥1000mg)+胰岛素 8 周或更长时间。 21 个国家/地区的站点。经过 2 周的导入期后,患者按照 1:1:1 的比例随机分配接受每日一次口服达格列净 (5mg)、沙格列汀 (2.5mg) 或安慰剂,并按背景治疗分层(仅二甲双胍、仅胰岛素 ,或二甲双胍 + 胰岛素)、性别(男性或女性)和年龄(≥10 至 <15 岁和 ≥15 至 <18 岁)。 在第 12 周接受 A1C ≥7% 的活性药物的患者在第 14 周进一步以 1:1 的比例随机分配,以继续当前剂量或滴定至更高剂量(10mg 达格列净或 5mg 沙格列汀)。 第 26 周后,患者继续当前治疗进入双盲长期治疗期。
主要疗效终点是达格列净或沙格列汀与安慰剂相比,所有剂量和方案相结合的 A1C 从基线到第 26 周的变化。 第 26 周的次要终点是空腹血糖 (FPG) 相对于基线的变化以及达到 A1C <7.0% 的患者比例(基线时 A1C ≥7%)。 所有终点均按以下层次结构单独评估(表 S4): 接受试验药物的患者(所有剂量和方案组合),以下称为“总”组,与安慰剂组进行评估(初步分析); 最初接受低剂量试验药物并在第 14 周(由于第 12 周 A1C ≥7%)被随机分配至高剂量的患者,以及在第 14 周未接受随机分配的患者(由于 A1C <7) % 在第 12 周),因此继续低剂量,以下称为“低剂量/高剂量”方案,与安慰剂进行比较; 最初接受低剂量试验药物的患者在第 14 周被随机分配(由于第 12 周 A1C ≥7%)继续低剂量,加上那些在第 14 周没有接受第二次随机分组的患者(由于第 12 周 A1C <7%) 第 12 周),因此持续低剂量,以下称为“低剂量”方案,与安慰剂进行比较; 在第 12 周 A1C ≥7% 的患者中,接受较低剂量的患者与接受较高剂量的患者,以下称为“低剂量与高剂量”评估。
结果显示,在随机分配的 245 名患者中,81 名患者接受 5mg 达格列净治疗,88 名患者接受 2.5mg 沙格列汀治疗,76 名患者接受安慰剂治疗(图 1)。 在这些患者中,47 例 (19.2%) 存在一项或多项方案偏差,并被排除在符合方案人群之外(达格列净组 n=64,沙格列汀组 n=74,安慰剂组 n=60)。 该试验中方案偏差的数量和类型符合 T2D 儿童和青少年群体的预期,并且没有表明治疗组之间存在任何可能影响数据解释的不平衡。
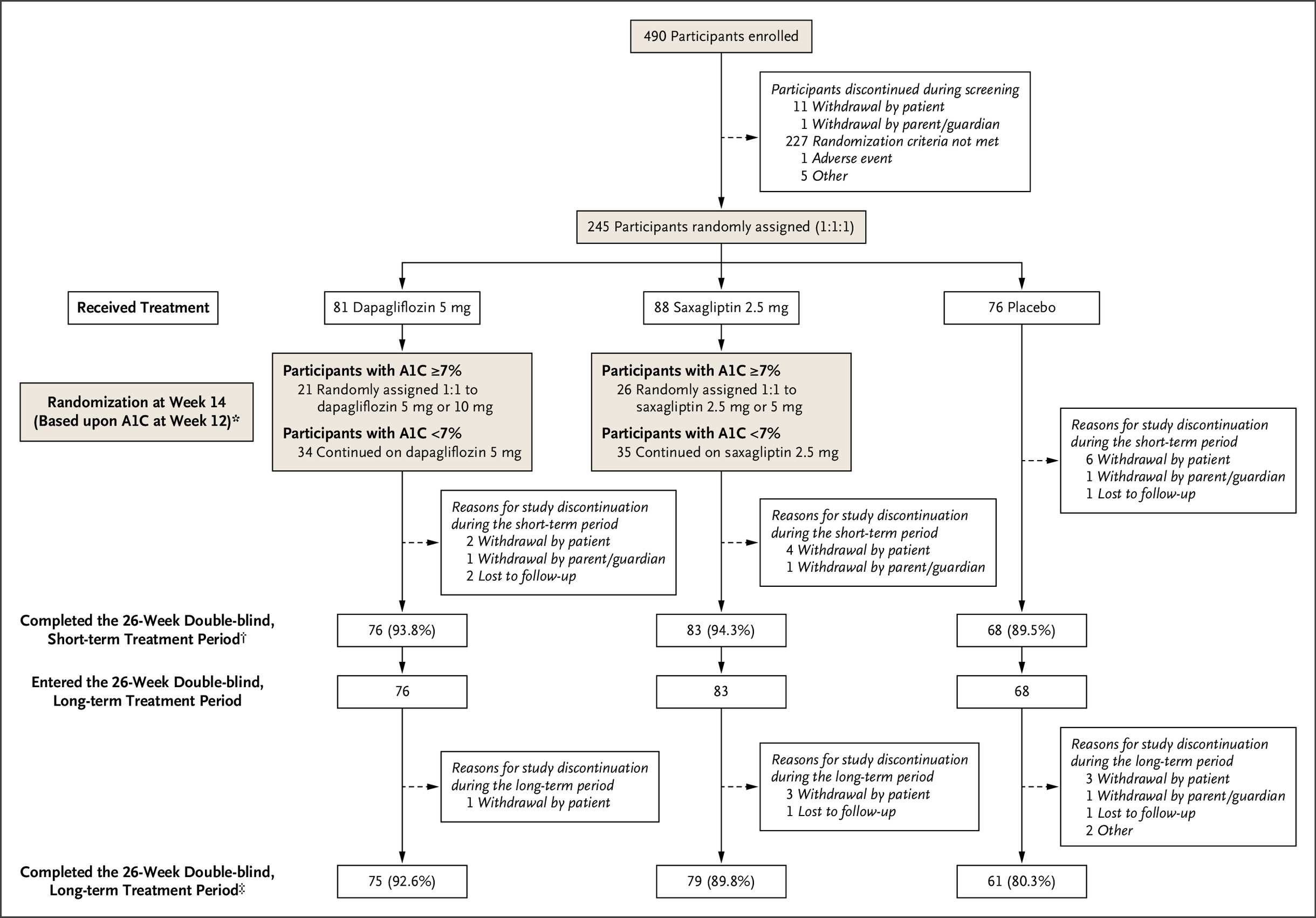
在达格列净组第 14 周,42 名 A1C ≥7% 的患者被随机分配继续接受 5mg 达格列净 (n=21) 或滴定至 10mg 达格列净 (n=21); 34 名 A1C <7% 的患者继续接受 5mg 达格列净治疗。 4 名接受达格列净治疗的患者在第 14 周前停药,另外一名患者错过了第 14 周的评估; 因此,这五名患者不是随机分配的,而是被纳入“低剂量/高剂量”和“低剂量”治疗方案的总体评估中。 在沙格列汀组第 14 周,52 名 A1C ≥7% 的患者被随机分配继续接受 2.5mg 沙格列汀治疗 (n=26) 或滴定至 5mg 沙格列汀治疗 (n=26); 35 名 A1C <7% 的患者继续接受 2.5mg 沙格列汀治疗。 一名接受沙格列汀治疗的患者在第 14 周前停药; 因此,该患者并未被随机分配,而是被纳入“低剂量/高剂量”和“低剂量”治疗方案的总体评估中。
总体而言,达格列净组、沙格列汀组和安慰剂组分别有 76 名 (93.8%)、83 名 (94.3%) 和 68 名 (89.5%) 患者完成了第 26 周和第 75 周 (92.6%)、79 名 (89.8%) 和 达格列净组、沙格列汀组和安慰剂组分别有 61 名 (80.3%) 患者完成了第 52 周的治疗。

第26周时,达格列净组A1C的调整后平均变化(95%置信区间[CI])为整个达格列净组的-0.62个百分点(-1.05至-0.19),+0.41个百分点(-0.01至0.84) 对于安慰剂组,减去安慰剂后的差异为-1.03个百分点(-1.57至-0.49;P<0.001)。 在第 52 周(探索性终点)进行评估时,与安慰剂相比的差异持续存在:-1.19 个百分点(95% CI,-1.99 至 -0.39)(图 S2)。 各基线亚组的结果总体一致(图 S3)。 与基线时 A1C <8% 的患者相比,基线时 A1C ≥8% 的患者达格列净治疗显示出更大的治疗效果(交互作用 P 值 <0.05)。 主要终点的敏感性分析与主要统计分析一致。
第 26 周时,沙格列汀组的 A1C 调整后平均变化 (95% CI) 为沙格列汀总组 +0.06 个百分点(-0.32 至 0.45),安慰剂组为 +0.50 个百分点(0.11 至 0.90),结果 减去安慰剂后的差异为-0.44个百分点(-0.93至0.05;P=0.078)。 在第 52 周(探索性终点)进行评估时,与安慰剂相比的差异为 -0.77 个百分点(95% CI,-1.48 至 -0.05)。 使用多重插补和“随机缺失”假设来处理缺失数据并排除抢救和治疗终止后的数据,对沙格列汀主要终点进行预先设定的敏感性分析,显示与安慰剂相比在第 26 周存在名义上的显着差异:-0.57 个百分点(95% ITT 人群中 CI,-1.09 至 -0.04;名义 P=0.035),符合方案人群中 –0.89 个百分点(95% CI,-1.47 至 -0.31;名义 P=0.003)(表 S12)。

26 周内,达格列净组、沙格列汀组和安慰剂组的患者发生低血糖的比例分别为 24.7%、25.0% 和 26.3%,到 52 周时,各组的患者发生低血糖的比例分别上升至 29.6%、29.5% 和 28.9%
在针对患有 T2D 的儿童和青少年的 T2NOW 试验中,达格列净显着改善了血糖。 沙格列汀在第 26 周的初步分析中未达到统计学显著性。
总之,T2NOW 试验通过证明达格列净治疗早期血糖显着改善且平均持续超过 1 年,提供了有关达格列净对 2 型糖尿病儿童和青少年的疗效和安全性的数据。 没有出现新的安全信号。
原始出处:
Dapagliflozin or Saxagliptin in Pediatric Type 2 Diabetes,NEJM Evid,DOI: 10.1056/EVIDoa2300210


