Lancet Microbe:抗结核治疗方案对痰微生物组的影响
时间:2023-11-26 11:31:37 热度:37.1℃ 作者:网络
呼吸微生物群被描述为呼吸健康的守门人,调节宿主免疫力和病原体对病原体殖民的抵抗力。不同的疾病状态和抗生素暴露已被证明会导致微生物群的发育不良。事实证明,使用2个月的异烟肼、利福霉素、吡吡嗪酰胺、雄胺、雄胺醇(HRZE)以及4个月的异烟酰胺和利福平(HRZE)的标准一线抗结核治疗不会扰乱整体微生物组多样性,但会耗尽一些免疫学上重要的共生细菌,这一结果可能会对个人健康产生长期影响。
短期结核病方案疗程可能会缩短微生物组的长度接触抗生素,降低微生物组长期受损的风险。因此,正在调查新的短期结核病方案课程,包括世卫组织在2022年推荐的4个月含利福喷丁-莫西沙星的方案。
人类肺不育,即使在健康人身上也是如此。人类肺部微生物群通常多样化的核心成分在相对丰度和流行率上各不相同。微生物组可能因年龄(新生儿、婴儿、年轻人和成人)、饮食和疾病而异。肺癌和结核病等疾病与以一些分类群增加或减少为特征的微生物组的变化有关。肺是*结核分枝杆菌*感染的偏好部位,其微生物群与结核病的各种状态有关。

这意味着抗生素治疗等干预措施会给微生物组增加额外的压力,这可以进一步改变肺微生物群的组成和功能。结核病方案对肺微生物群的影响可能与对各种革兰氏阳性和革兰氏阴性细菌有活性的抗生素更相关。因此,有必要研究新的结核病方案课程的效果,特别是那些加入广谱高剂量抗生素的疗法。2023年10月10日发表在Lancet Microbe的文章,使用痰来调查标准护理和研究结核病方案课程对肺微生物群的影响及其对治疗结果的影响。
在这项回顾性研究中,研究人员分析了使用六种实验方案与作为HIMRIF研究2的一部分的标准护理治疗结核病参与者的痰微生物组和PanACEA MAMS-TB为期3个月的治疗随访期的临床试验。样本来自坦桑尼亚姆贝亚、乞力马扎罗、巴加莫约和达累斯萨拉姆的参与者。实验方案由磷脂(R)、异烟肼(H)、吡嗪酰胺(Z)、乙胺醇(E)、莫西沙星(M)和新药SQ109(Q)的不同组合组成。
使用逆转录为每个参与者的总痰RNA创建互补DNA,并使用Illumina元基因组技术对16S rRNA基因的V3-V4区域进行测序。Qiime用于分析扩增子序列变体并估计α多样性。描述性统计数据用于评估治疗前和治疗后开始α多样性的差异以及每种治疗方案的效果。
研究结果显示,从2008年9月26日至2015年6月30日期间在七个治疗方案中采集的397个治疗前和治疗后样本中获得了序列数据。治疗前微生物组(206属)在门层由Firmicutes(2860[44%]的6500个安普利康序列变体[ASVs]中占2860[44%])和属级的链球菌(2340 [36%] ASVs)主导。两种方案在治疗2周后对微生物组产生了显著的抑制作用,HR20mg/kgZM(香农多样性指数p=0.0041)和HR35mg/kgZE(p=0.027)。
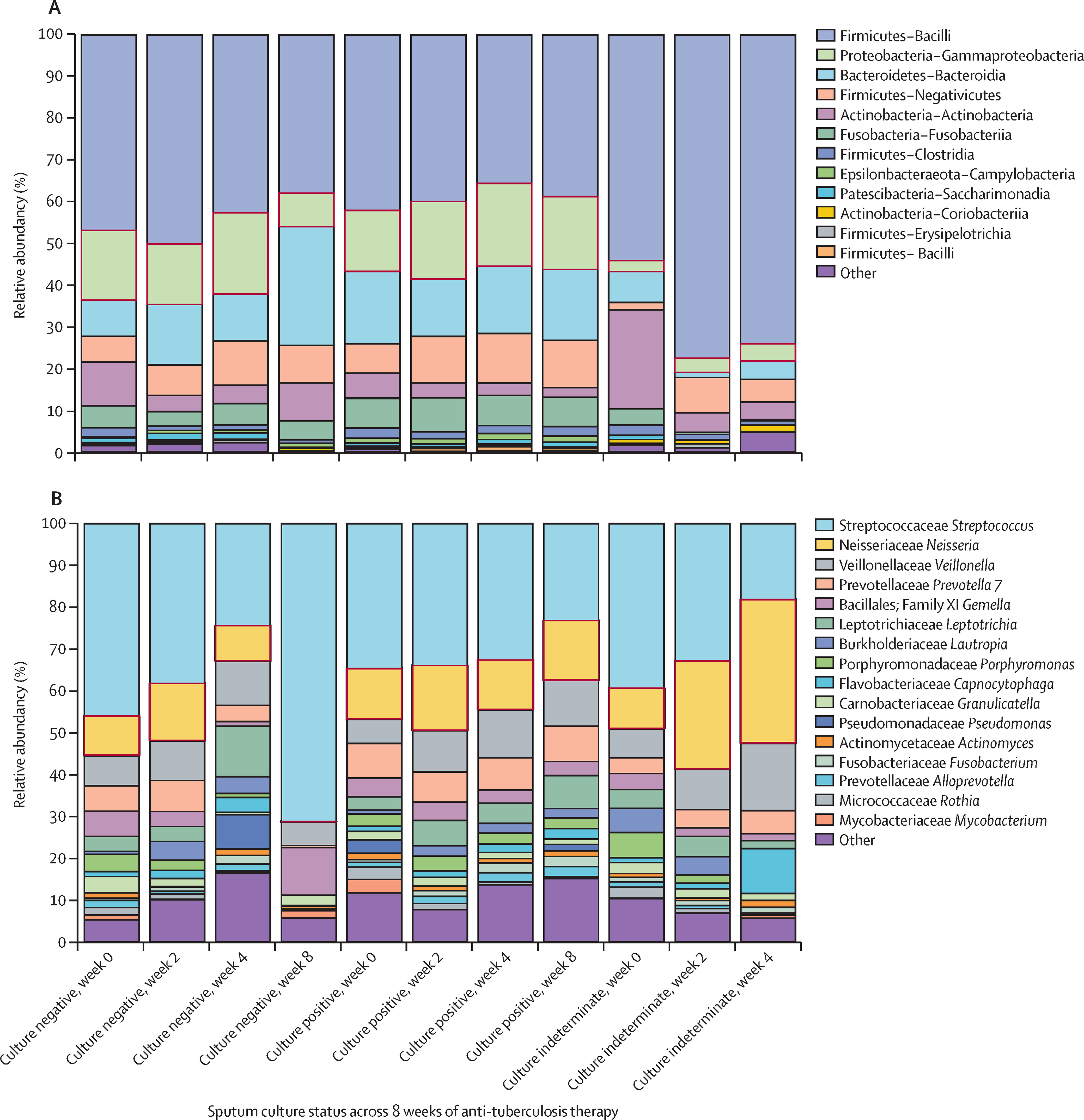
治疗第8周分类群变化和治疗结果的关联
革兰氏阴性细菌对治疗的杀菌活性最敏感,在莫西沙星方案下被抑制的物种数量最多。到治疗开始后的12周,除了HR35mg/kgZE方案和分枝*杆菌属外,微生物组已恢复到治疗前水平,该方案并非在所有方案中都显示恢复。在第8周治疗中将结核病培养转化为阴性与奈瑟菌*属的清除有关,治疗前水平降低了98%。
综上所述,不同的抗结核方案和剂量对痰微生物组有不同的影响。标准的一线方案HR600mgZE或HR10mg/kgZE似乎只对微生物组影响很小,导致分类群均匀度增加,多样性没有显著减少。在标准方案的骨干中,将利福平单独剂量增加到35毫克/千克,从而显著减少了微生物组,到治疗随访的第3个月没有恢复到治疗前水平。
20毫克/千克的低利福平剂量,辅以400毫克莫西沙星,导致微生物组多样性显著减少,到治疗第3个月恢复到治疗前水平。该药物SQ109似乎没有为抗结核治疗方案的性能或其对微生物组的影响增加显著价值。最重要的是,M结核病没有显示出跨方案的恢复,这种效果意味着新型最佳抗结核方案可以缩短治疗过程,而不会对有益的呼吸道微生物群造成不可逆转的损害。
此外,需要进行大规模纵向研究,以确定是否只有M结核病被消除,以及这对恢复的微生物组和治疗结果有什么影响。
原始出处
Musisi, E., Wyness, A., Eldirdiri, S., Dombay, E., Mtafya, B., Ntinginya, N. E., ... & Msefula, C. L. (2023). Effect of seven anti-tuberculosis treatment regimens on sputum microbiome: a retrospective analysis of the HIGHRIF study 2 and PanACEA MAMS-TB clinical trials. The Lancet Microbe, 4(11), e913-e922.


