国际会议 | 2024 ELCC:肺癌重点研究摘要速览!
时间:2024-03-16 21:00:35 热度:37.1℃ 作者:网络
前言
2024 ELCC
2024年欧洲肺癌大会(ELCC)将于中欧时间3月20日-23日以线上+线下(捷克 布拉格)的形式召开,届时将汇集各国肺癌领域专家分享最前沿研究进展和最新的临床研究数据。
目前ELCC官网在线发布了入选研究的摘要信息(最新突破性摘要[LBA]暂未公布),e路新干线小编第一时间整理了药物治疗重点研究,包括的报告类型有:口头汇报(O)、简短口头汇报(MO),以飨读者。
LBA内容将于中欧时间3月19日公布
摘要号:LBA1
Durvalumab in combination with chemoradiotherapy for patients with unresectable stage III NSCLC: Final results from PACIFIC-2
度伐利尤单抗联合放化疗治疗不可切除的Ⅲ期NSCLC:PACIFIC-2研究的最终结果
报告人:Jeffrey D. Bradley
摘要号:LBA2
Clinical outcomes with perioperative nivolumab (NIVO) in patients (PTS) with resectable NSCLC from the phase III CheckMate 77T study
来自Ⅲ期CheckMate 77T研究围手术期纳武利尤单抗(NIVO)治疗可切除NSCLC的临床结果
报告人:Mark Awad
01 NSCLC
摘要号:4O
奥希替尼+化疗为EGFR突变晚期NSCLC提供了初始进展后的临床获益,且OS呈获益趋势
题目:奥希替尼(osi)±铂类-培美曲塞一线(1L)治疗EGFR突变(EGFRm)晚期NSCLC:FLAURA2研究进展后结果
报告人:Natalia Isabel Valdiviezo Lama
背景
osi是一种具有中枢神经系统活性的第三代EGFR酪氨酸激酶抑制剂(EGFR-TKI),可选择性地有效抑制EGFR-TKI敏感突变和EGFR T790M耐药突变。在Ⅲ期FLAURA2研究 (NCT04035486)中,与单独使用osi相比,1L osi+铂类-培美曲塞化疗(CTx)显著改善了 EGFRm晚期NSCLC患者的无进展生存期(PFS)(HR 0.62;95% CI 0.49,0.79;p<0.001)(Planchard et al. NEJM 2023;389:1935-48.)。在此报告了FLAURA2研究进展后结果,包括更新的总生存期(OS)。
方法
WHO体能状态0/1、初治EGFRm(19del/L858R)晚期NSCLC成人患者接受osi 80 mg 每天一次(QD) + CTx(培美曲塞+顺铂或卡铂,4个周期 [Q3W]),然后osi 80 mg QD +培美曲塞 Q3W,或osi 80 mg QD单药治疗,直至进展/满足停药标准。后续治疗由研究者选择。次要终点包括从随机分组至首次后续治疗的时间(TFST)、至第二次进展的时间(PFS2)、至第二次后续治疗的时间(TSST)和OS。数据截止日期(DCO):2023年4月3日。我们报告了第二次期中分析(IA)更新的OS(DCO:2024年1月8日)。
结果
在初次DCO(2023年4月3日)时,osi + CTx组和osi组分别有123/279(44%)和151/278(54%)例患者停止治疗。在这些患者中,57/123(46%;osi + CTx组) vs. 91/151(60%;osi组)开始首次后续治疗,最常见的CTx为37/57(65%) vs. 75/91(82%)。TFST、PFS2和TSST HR(95% CI)分别为0.73(0.56,0.94)、0.70(0.52,0.93)和0.69(0.51,0.93)。虽然OS结果仍不成熟,并且在第二次IA分析中没有达到统计学意义(41%成熟度;DCO:2024年1月8日),但是观察到OS获益趋势。osi + CTx组未达到中位OS(95% CI,38.0,不可计算[NC]),osi组中位OS为36.7个月(95% CI,33.2,NC);OS HR为0.75(95% CI,0.57,0.97)。OS在预先指定的亚组中是一致的。
结论
FLAURA2研究进展后结果表明,与osi相比,1L osi + CTx在EGFRm晚期NSCLC患者初始进展后具有临床获益,更新的OS数据显示出令人鼓舞的OS获益趋势。
摘要号:108O
围手术期替雷利珠单抗+新辅助化疗不影响手术的可行性和完成度
题目:RATIONALE-315研究的手术结果:围手术期替雷利珠单抗+新辅助化疗治疗可切除NSCLC的随机、双盲、Ⅲ期研究
报告人:岳东升 教授(天津医科大学肿瘤医院)
背景
RATIONALE-315研究(NCT04379635)评估了围手术期替雷利珠单抗(TIS)或安慰剂(PBO)联合新辅助化疗(CT)在可切除NSCLC患者中的疗效和安全性。在此报告了该研究的关键手术结果。
方法
纳入ECOG PS≤1、无已知EGFR突变或ALK基因易位的初治可切除Ⅱ-ⅢA期NSCLC中国患者。患者随机分配(1:1)至3-4个周期的TIS 200 mg或PBO IV Q3W + CT,然后进行手术和最多8个周期的辅助TIS 400 mg或PBO IV Q6W。主要终点是主要病理缓解(MPR,之前已报道)和无事件生存期。关键次要终点是病理完全缓解(pCR)率。手术结果是探索性终点。
结果
共纳入453例患者,两组之间的基线特征相似。TIS组和PBO组分别有190/226(84.1%)和173/227(76.2%)例患者接受了根治性手术(结果见表1)。手术取消的主要原因分别是患者退出(20 vs. 28例)、疾病进展(6 vs. 17例)和不良事件(AE)(6 vs. 2例)。手术延迟分别有31例(16.3%)和22例(12.7%),主要是由于12例(6.3%)(TIS组)和6例(3.5%)(PBO组)发生AE,大多数在两周内发生。TIS组的R0切除率为95.3%,PBO组为93.1%。两组的中位手术持续时间(2.7 vs. 2.8小时)和住院时间(7 vs. 7天)相似。在TIS组与PBO组中,任何级别AE和≥3级术后并发症发生率分别为63.7% vs. 61.3%和11.1% vs. 15.6%,90天术后死亡分别有3例(1.3%)和4例(1.8%)。
表1 手术情况汇总
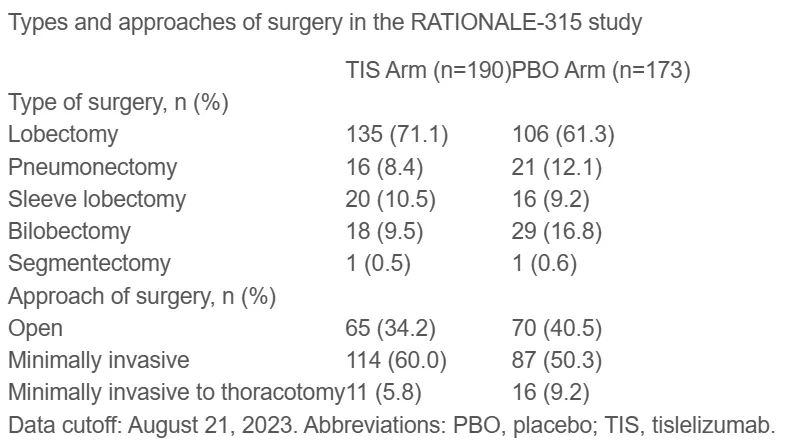
结论
围手术期TIS+新辅助CT不影响手术的可行性和完成度,MPR和pCR具有统计学意义的显著改善,安全性可控,表明TIS是可切除NSCLC患者的围手术期治疗选择。
摘要号:1MO
赛沃替尼治疗初治或经治MET ex14突变NSCLC安全有效
题目:赛沃替尼治疗MET 14号外显子突变局部晚期或转移性NSCLC的Ⅲb期研究
报告人:张永昌 教授(湖南省肿瘤医院)
背景
赛沃替尼是一种有效的具有高度选择性口服MET酪氨酸激酶抑制剂,基于一项Ⅱ期研究(NCT02897479),赛沃替尼在中国被批准用于治疗既往全身治疗后进展或无法耐受化疗的MET 14号外显子(MET ex14)突变NSCLC患者。在此报告了Ⅲb期确证性研究的主要分析结果(NCT04923945;数据截止日期:2023年10月20日;随访时间:初治患者≥12个月,既往经治患者≥6个月)。
方法
纳入既往经治(≥2L)或初治(1L)晚期或转移性MET ex14突变NSCLC患者。患者接受赛沃替尼QD 600 mg(≥50 kg)或400 mg(<50 kg)。主要终点是BIRC根据RECIST 1.1评估的ORR。次要终点主要包括DCR、DoR、TTR、PFS和OS。
结果
初治患者(n=87;中位年龄:70岁;男性:58.6%;ECOG PS 1:81.6%;腺癌:80.5%;PSC:8.0%;脑转移:11.5%),BIRC评估的ORR为62.1%,DCR为92.0%;中位随访时间分别为18.0和20.8个月,mPFS为13.7个月,mOS未达到。既往经治患者(n=79;中位年龄:68.8岁;男性:57.0%;ECOG PS 1:87.3%;腺癌:78.5%;PSC:5.1%;脑转移:26.6%),ORR为39.2%,DCR为92.4%;中位随访时间分别为11.0和12.5个月,mPFS为11.0个月,mOS尚不成熟(结果见表2)。100例患者发生≥3级与研究药物相关TEAE(100/162,60.2%)。最常见(≥5%)的是肝功能异常(16.9%)、丙氨酸转氨酶升高(14.5%)、天冬氨酸转氨酶升高(12.0%)、γ -谷氨酰转氨酶升高(6.0%)和外周水肿(6.0%)。
表2 疗效数据汇总

结论
数据显示,赛沃替尼治疗MET ex14突变NSCLC具有令人鼓舞的疗效和可接受的安全性,为初治和经治患者人群提供了新的标准治疗选择。
摘要号:2MO
埃万妥单抗+化疗显著延长了EGFR ex20ins突变晚期NSCLC进展后的TTD和TTST
题目:埃万妥单抗+化疗 vs. 化疗一线治疗EGFR 20号外显子插入突变晚期NSCLC:PAPILLON研究进展后终点分析
报告人:Enriqueta Felip
背景
埃万妥单抗(ami)是一种具有免疫细胞导向活性的EGFR-MET双特异性抗体。在PAPILLON研究(NCT04538664)中,ami联合卡铂-培美曲塞(ami-化疗)与化疗相比显著延长了EGFR ex20ins晚期NSCLC患者的无进展生存期(PFS)(Zhou NEJM 2023)。在此评估了进展后的次要终点,即至治疗停止的时间(TTD)和至后续(全身抗肿瘤)治疗的时间(TTST)。
方法
随机分配了308例患者(ami-化疗:153;化疗:155)。随机至化疗组的患者允许在盲法独立中心审查(BICR)确认进展后交叉。根据研究中心报告的受试者治疗变化情况评估TTD和TTST。
结果
中位随访14.9个月时,ami-化疗组和化疗组分别有54%(83/153)和85%(131/155) 患者停止了治疗。ami-化疗组的中位TTD为13.2个月,化疗组为7.5个月(HR,0.38 [95% CI,0.28–0.51];P<0.0001)。ami-化疗组的中位TTST为17.7个月,化疗组为9.9个月(HR,0.35 [95% CI,0.25–0.49];P<0.0001)。该结果与首次后续治疗后的PFS一致(PFS2;HR,0.49 [95% CI,0.32–0.76];P=0.001),并且ami-化疗组期中OS优于化疗组(HR,0.67 [95% CI,0.42–1.09];P=0.11)(Girard Ann Oncol 2023)。在停药患者中,ami-化疗组和化疗组分别有52%(43/83)和72%(94/131)的患者开始了后续治疗,最常见的是化疗(ami-化疗组;30%[13/43])和ami单药治疗(化疗组;76%[71/94])。ami-化疗组17%(11/63为疾病进展)的患者进展后继续治疗,进展后的中位持续时间为40.4周(95% CI,8.7-NE)。在71例接受二线ami单药治疗的随机化疗患者中,其中65例是研究交叉组的一部分,6例接受非ami方案治疗。在交叉组的65例患者中,46%(30/65)停止了ami单药治疗。中位治疗持续时间为4.9个月(范围,0-18.2),中位TTD为9.7个月(95% CI,6.7-11.0)。
结论
与化疗相比,ami-化疗显著延长了TTD和TTST。ami-化疗为EGFR ex20ins突变晚期NSCLC患者的新一线标准治疗。
摘要号:3MO
埃万妥单抗+化疗显著延长了EGFR突变晚期NSCLC进展后的TTD、TTST和PFS2
题目:埃万妥单抗+化疗 vs. 化疗治疗使用奥希替尼后进展的EGFR突变晚期NSCLC:MARIPOSA-2研究进展后分析
报告人:Ryan D. Gentzler
背景
埃万妥单抗(ami)是一种具有免疫细胞导向活性的EGFR-MET双特异性抗体。在MARIPOSA-2研究(NCT04988295)中,ami联合卡铂-培美曲塞(ami-化疗)与化疗相比显著延长了奥希替尼治疗后进展的EGFR突变晚期NSCLC患者的无进展生存期(PFS)(Passaro Ann Oncol 2023)。在此评估了MARIPOSA-2研究进展后结局。
方法
随机分配了657例患者,分析的重点是随机分配至ami-化疗组的131例(安全性:n=130)和化疗组的263例(安全性:n=243)患者。第三组(ami-拉泽替尼-化疗组)进行了修改,将在未来报告。进展后的终点为至治疗停止的时间(TTD)、至后续治疗的时间(TTST)和首次后续治疗后的PFS(PFS2)。
结果
中位随访8.7个月时,ami-化疗组和化疗组分别有55/130(42%)和173/243(71%)例患者发生疾病进展。在进展患者中,ami-化疗组和化疗组分别有19/55(35%)和28/173(16%) 例患者进展后接受了>4周的治疗,进展后的中位治疗持续时间(95% CI)分别为18.3(9.0-NE) 和9.0(6.0-16.4)周。ami-化疗与化疗相比显著延长了TTD(中位数,11.0 vs. 4.5个月;HR,0.37 [95% CI,0.28–0.50];P<0.0001)、TTST(中位数,12.1 vs. 6.6个月;HR,0.42 [95% CI,0.30–0.59];P<0.0001)和PFS2(中位数,13.9 vs. 11.3个月;HR,0.60 [95% CI,0.40–0.92];P=0.017)。在进展患者中,包括进展后接受治疗的患者,ami-化疗组和化疗组分别有75%(41/55)和93%(161/173)的患者在进展后停止治疗。两组中63%进展患者开始了后续的全身治疗。后续治疗最常使用奥希替尼(ami-化疗组:10%;化疗组:9%)和多西他赛(ami-化疗组:7%;化疗组:9%)。
结论
与化疗相比,ami-化疗显著延长了TTD、TTST和PFS2。ami-化疗为奥希替尼治疗后进展的EGFR突变晚期NSCLC患者的新标准治疗。
摘要号:5MO
埃万妥单抗进行早期剂量调整不会对联合用药的疗效产生不利影响
题目:埃万妥单抗剂量中断对于埃万妥单抗+拉泽替尼一线治疗EGFR突变晚期NSCLC疗效和安全性的影响:MARIPOSA研究的探索性分析
报告人:Maria Rosario García Campelo
背景
埃万妥单抗(ami)是一种具有免疫细胞导向活性的EGFR-MET双特异性抗体。拉泽替尼(laz)是一种具有中枢神经系统渗透性的第三代EGFR TKI。作为一线治疗,ami + laz与奥希替尼相比在EGFR突变晚期NSCLC中显示出优异的无进展生存期(PFS)(Cho Ann Oncol 2023)。MARIPOSA研究(NCT04487080)方案指南建议,如果发生相关≥2级毒性,则应中断ami给药。对于接受一线ami + laz治疗的患者,大多数关键不良事件发生在前4个月(Spira JTO 2023)。在此报告了接受ami + laz治疗但在前4个月内发生ami剂量中断的患者的疗效和安全性。
方法
该分析包括MARIPOSA研究中随机分配至ami + laz组的所有患者(疗效集:n=429,安全性集:n=421)。研究方案规定先于laz对ami进行剂量调整。剂量中断被定义为由于任何原因导致的ami中断。
结果
在随机分配至ami + laz组的429例患者中,421例至少接受了一剂。中位随访22.0个月时,49%(206/421)的患者在治疗前4个月内出现ami剂量中断。在前4个月内发生ami剂量中断的患者中,中位PFS为23.9个月(95% CI,18.5-NE)。前4个月内发生和未发生ami剂量中断的患者中位PFS、客观缓解率(ORR)和中位缓解持续时间(DoR)与随机分配至ami + laz组的所有患者相似,结果见表3。会议期间将介绍最新的分析,包括剂量中断对治疗耐受性的影响。
表3 疗效数据汇总

结论
在接受ami + laz治疗的患者中,根据方案指南对ami进行早期剂量调整不会对联合用药的疗效产生不利影响。ami + laz是EGFR突变晚期NSCLC患者的新一线标准治疗。
摘要号:137MO
becotarug+奥希替尼治疗EGFR ex20ins突变NSCLC安全有效
题目:becotarug(JMT101)联合奥希替尼治疗EGFR 20号外显子插入(ex20ins)突变局部晚期或转移性NSCLC的Ⅱ期研究(BECOME研究)
报告人:张力 教授(中山大学肿瘤防治中心)
背景
EGFR ex20ins突变阳性NSCLC患者的治疗选择有限且预后差。becotarug是一种靶向EGFR的人源化IgG1单克隆抗体。在既往Ⅰb期研究中,becotarug联合奥希替尼显示出令人鼓舞的疗效(Zhao et al,Nature Communications;2023)。在此报告了becotarug联合奥希替尼Ⅱ期研究的结果(NCT05132777)。
方法
这是一项多中心、开放标签的Ⅱ期研究,纳入了既往含铂化疗失败的EGFR ex20ins突变局部晚期或转移性NSCLC患者。符合条件的患者接受becotarug(6 mg/kg Q2W)联合奥希替尼(160 mg QD)治疗,直至IRC评估的疾病进展、出现不可耐受的毒性或退出研究(以先发生者为准)。主要目标是评估becotarug联合奥希替尼的疗效。次要目标包括安全性、药代动力学和免疫原性。
结果
在2021年11月26日至2023年6月21日期间,共纳入了126例患者,中位年龄为59岁(范围34-82岁)。122例患者被纳入ITT(定义为经中心实验室确认的EGFR ex20ins突变患者),89%(n=100)经IRC评估为肿瘤退缩。IRC确认的客观缓解率(ORR)为50%(95%CI,40-60%),疾病控制率(DCR)为80%(95%CI,71-87%)。值得注意的是,脑转移患者的ORR为43%(18/42,95%CI,28-59%)。125例(99%)患者报告了治疗相关不良事件(TRAE),其中99例(79%)为≥3级TRAE。最常见的TRAE是皮疹(80%)、腹泻(68%)、食欲下降(64%)、口腔黏膜炎(65%)和体重下降(59%),但大多数是低级别,相应≥3级的发生率分别为32%、10%、4%、11%和2%。大多数TRAE是与EGFR靶向相关的毒性,且可以得到很好的控制,仅5%患者因TRAE而永久停药。
结论
becotarug联合奥希替尼治疗EGFR ex20ins突变NSCLC显示出可控的安全性和令人鼓舞的抗肿瘤活性。
02 SCLC
摘要号:194MO
低剂量放疗+度伐利尤单抗+化疗一线治疗ES-SCLC延长PFS且耐受性良好
题目:低剂量放疗(LDRT)+度伐利尤单抗(D)+依托泊苷/铂类(EP)一线治疗ES-SCLC的Ⅱ期研究(LEAD):疗效和安全性结果
报告人:张衍 教授(四川大学华西医院)
背景
Ⅲ期CASPIAN试验将D + EP确立为ES-SCLC的一线 (1L) 标准治疗。然而,大多数患者没有获得持久的临床获益。LDRT可诱导局部控制,与免疫检查点抑制剂发挥协同作用。LEAD研究评估了LDRT + D + EP 1L治疗ES-SCLC。
方法
LEAD研究是一项单臂、多中心、Ⅱ期试验。纳入年龄≥18岁且ECOG PS 0-1的初治ES-SCLC 患者。D 1500 mg + EP Q3W 4个周期,然后D维持治疗。在第1个周期中同步进行LDRT(15 Gy/5f)。根据研究者判断,允许进行预防性颅脑放疗(PCI)。主要终点是无进展生存期(PFS)。次要终点包括总生存期(OS)和安全性。
结果
在2022年3月至2023年2月期间,纳入了来自中国4个中心的30例患者。至数据截止日期(2023年11月9日),中位年龄为58岁(范围40-77);97%(29)为男性;60%(17)ECOG PS为1。分别有20%(6)和10%(3)的患者在基线时存在肝转移和脑转移。57%(17)接受了PCI。删失患者PFS中位随访时间为17.3个月,73%(22)的患者发生PFS事件,mPFS为8.3个月[95% CI,4.6-15.2],6个月和12个月PFS率分别为57%和40%。mOS未达到[95% CI,10.8-NE]。总体客观缓解率(ORR)为87%。在肝转移和脑转移患者中,ORR分别为50%和100%。≥3级TEAE的发生率为80%(24),最常见的≥3级TEAE是血液学毒性。13.3%(4)的患者报告了≥3级免疫相关AE(irAE)。放疗相关SAE的发生率为16.7%(5)。1例患者发生间质性肺病(2级)。至数据截止日期,33.3%(10)的患者仍在接受治疗,进一步评估仍在进行中。
结论
在LEAD研究中,同步LDRT和D + EP 1L治疗ES-SCLC显示出有前景的mPFS延长,并且耐受性良好。这一结果值得在ES-SCLC中进一步研究该治疗方式。
摘要号:195MO
tarlatamab在既往经治的SCLC中表现出持久的缓解和优异的生存结果
题目:tarlatamab治疗既往经治的小细胞肺癌(SCLC):Ⅰ期DeLLphi-300研究的长期结果和颅内活性
报告人:Horst-Dieter Hummel
背景
tarlatamab是一种靶向δ样配体3(DLL3)的双特异性T细胞衔接器(BiTE®)免疫疗法,在既往经治的SCLC中显示出持久的抗肿瘤活性和可控的安全性。在此报告了Ⅰ期DeLLphi-300研究的长期结果和颅内活性。
方法
在既往经治的SCLC患者中评估tarlatamab。纳入经治、脑转移稳定的患者。主要终点是安全性。次要终点包括研究者根据mRECIST 1.1评估的客观缓解率(ORR)、缓解持续时间(DOR)、无进展生存期(PFS)和总生存期(OS)。在回顾性探索性分析中,BICR根据mRANO-BM评估基线时有≥1个脑病灶患者的CNS肿瘤直径之和(SOD)。本报告的数据截止日期(DCO)比Paz-Ares,J Clin Oncol 2023多14.5个月,包括所有接受临床相关剂量(≥10 mg)tarlatamab治疗的患者队列。
结果
152例患者接受tarlatamab≥10 mg治疗(随访时间范围0.2-34.3个月;中位12.1个月)。在各队列中,ORR为25.0%,mDOR为11.2个月(结果见表4)。25例患者的治疗持续时间≥52周(范围52-150),包括8例治疗≥104周。mPFS和mOS分别为3.5个月和17.5个月,12个月PFS率和OS率估计值分别为16.7%和57.9%。在基线CNS病灶≥10 mm的16例患者中,10例(62.5%)CNS肿瘤SOD缩小≥30%。在tarlatamab开始治疗前≥50天完成脑放疗(RT)的8例患者中,3例(37.5%)CNS肿瘤SOD缩小≥30%。没有发现新的安全信号。
表4 疗效数据汇总

结论
在DeLLphi-300研究的长期随访中,tarlatamab在既往经治的SCLC中表现出持久的缓解和前所未有的生存结果。虽然仅限于对经治、脑转移稳定患者的分析,但tarlatamab治疗和RT后长期的CNS肿瘤退缩支持进一步研究tarlatamab的颅内疗效。
摘要号:196MO
安罗替尼联合化疗一线治疗ES-SCLC显示出显著的PFS改善和数值上的OS获益
题目:安罗替尼+依托泊苷/卡铂(EC) vs. 安慰剂+EC一线治疗广泛期小细胞肺癌(ES-SCLC):一项随机、双盲、平行对照、Ⅲ期试验(ETER701)
报告人:程颖 教授(吉林省肿瘤医院)
背景
免疫化疗对ES-SCLC总生存期(OS)的改善远不能令人满意。研究发现,安罗替尼(一种抗血管生成药物)与免疫检查点抑制剂和/或化疗联合使用时,可以重新编程免疫抑制性肿瘤微环境和协同治疗获益。ETER701是首个评估安罗替尼+依托泊苷/卡铂(EC)±benmelstobart(一种新型的PD-L1抑制剂) vs. 安慰剂+EC一线治疗ES-SCLC的随机Ⅲ期试验。与安慰剂+EC相比,安罗替尼+EC + benmelstobart观察到历史上最长的OS。在此报告了安罗替尼+EC(安罗替尼组) vs. 安慰剂+EC(EC组)的数据。
方法
在这项多中心、双盲、安慰剂对照的Ⅲ期研究中,符合条件的ES-SCLC患者被随机分配(1:1:1)接受benmelstobart+安罗替尼+EC或安慰剂+安罗替尼或安慰剂+EC治疗,4个21天周期,然后benmelstobart+安罗替尼或安慰剂+安罗替尼或安慰剂+EC维持治疗。共同主要终点是独立审查委员会(IRC)评估的无进展生存期(PFS)和意向治疗人群的OS。
结果
在2020年3月18日至2021年12月18日期间,纳入了738例患者。245例患者被分配至安罗替尼组,247例被分配至EC组。中位随访时间为14.0个月(数据截止日期为2022年5月14日),安罗替尼组的中位PFS显著长于EC组(5.6个月 vs. 4.2个月;HR,0.44;95% CI,0.36-0.55;P<0.0001),安罗替尼组的中位OS为13.3个月,EC组为11.9个月(HR,0.86;95% CI,0.67-11.10;P=0.1723)。3级或更高级别治疗相关不良事件的发生率分别为94.3%和87.0%,5级分别为2.5%和1.6%。
结论
与化疗相比,安罗替尼联合化疗一线治疗ES-SCLC显示出显著的PFS改善和数值上的OS获益。抗血管生成联合化疗的生存获益与免疫化疗相当,安全性是可接受和可控的。
摘要号:197MO
阿维鲁单抗联合铂类化疗治疗ES-SCLC未达到1年PFS率的主要终点
题目:阿维鲁单抗联合铂类化疗治疗ES-SCLC患者的最终结局、免疫表型和生物标志物分析(PAVE):希腊肿瘤协作组的一项试验性Ⅱ期研究
报告人:Giannis Mountzios
背景
广泛期小细胞肺癌(ES-SCLC)是一种预后不良的疾病,一线化疗免疫疗法目前是标准治疗。我们假设,在两个诱导化疗周期后,新抗原最大程度释放时进行免疫治疗可能会增强免疫反应和整体疗效。
方法
PAVE是一项抗PD-L1单抗阿维鲁单抗联合铂类-依托泊苷的单臂、多中心Ⅱ期研究。在Ⅱ期部分之前进行了安全导入,未经治疗的ES-SCLC患者每三周接受一次标准化疗,持续4-6个周期。从第3周期到化疗完成,每两周一次阿维鲁单抗 10 mg/kg,之后作为维持治疗。主要终点为1年PFS率。通过靶向NGS对FFPE肿瘤进行基因分型,评估肿瘤浸润淋巴细胞 (TIL) 密度并分析CD8和PD-L1。
结果
在2018年9月至2020年9月期间,纳入了55例患者,中位年龄为65.9岁,男性为67.3%。转移部位包括肝脏(54.5%)、骨骼(32.7%)、脑(10.9%)。中位随访10.3个月时,1年PFS率为12.7%,中位PFS为5.8个月,1年OS率为38.2%,中位OS为10.3个月。在ITT患者中,ORR为69.1%(CR 5.5%,PR 63.6%),中位DOR为5.6个月,56%的患者发生3/4级AE。QoL、整体健康状况和疾病相关症状均得到显著改善。肿瘤中TIL/CD8的存在没有任何预测或预后价值。除一个肿瘤外,所有肿瘤都携带基因突变,其中TP53(89.5%)、RB1(57.9%)、NOTCH(31.6%)和MYC(23.7%)是最常见的突变基因。存在肝转移、RB1或TP53/RB1共突变、未行PCI和年龄较大(>65岁)是PFS和OS的不良预后因素。
结论
阿维鲁单抗联合铂类-依托泊苷治疗未达到1年PFS率的主要终点。然而,我们的研究结果表明,该方法与已发表的一线化疗免疫治疗方案具有相当的疗效,具有临床相关的PFS、DoR和改善的QoL,值得评估。


