阿培利司在PIK3CA突变晚期妇科癌症中显示出有前景的临床活性
时间:2024-06-05 14:00:49 热度:37.1℃ 作者:网络
复发性妇科肿瘤(如子宫内膜癌和卵巢癌)是不可治愈的疾病。因此,迫切需要新的治疗方案。PTEN-AKT-PI3K通路在这些肿瘤中经常发生变异,代表了潜在的治疗靶点。阿培利司是一种α特异性PI3K抑制剂,已被批准用于治疗PIK3CA突变的晚期乳腺癌。研究者报告了在一个对照计划中前瞻性使用阿培利司治疗的一大系列PIK3CA突变妇科癌症患者的结果。2021年4月-2022年12月,36例PIK3CA突变晚期妇科癌症患者接受了阿培利司300 mg口服、1次/天治疗。客观缓解率(ORR)和疾病控制率(DCR)是衡量阿培利司抗肿瘤活性的指标,这是本研究的主要目的。
纳入的患者有子宫内膜癌(17/36[47%])、卵巢癌(10/36[28%])或其他妇科癌症(9/36[25%])。大多数患者既往接受过2-3种全身治疗(子宫内膜,47.2%;卵巢,60%;其他,56%),并且基线时有内脏转移(分别为82%、70%和56%)。总体而言,发现了17种不同的PIK3CA突变,其中53%位于激酶结构域(最常见的是H1047R),36%位于螺旋结构域(最常见的是E545K)。总体而言,ORR为28%,DCR为61%,在子宫内膜癌患者中观察到的获益最大(分别为35%和71%)。
对于携带PIK3CA突变的复发性妇科癌症患者,阿培利司是一种积极治疗方案。这些发现支持在妇科癌症中开展生物标志物驱动的PI3K抑制剂随机试验的必要性。
-
PTEN-AKT-PI3K通路在妇科肿瘤中经常发生变异;
-
对于携带PIK3CA突变的妇科肿瘤,目前可用的治疗方案很少;
-
口服PI3K α选择性抑制剂阿培利司(Alpelisib)的疗效很有前景(ORR为28%;PFS为6.3个月);
-
阿培利司耐受性良好。
研究背景
精准肿瘤学是妇科肿瘤领域一种新的、有前景的治疗方法。大约15年前,癌症基因组图谱研究网络开启了肿瘤学研究的新时代,重点关注可靶向的变异,尤其是子宫内膜癌(西方国家最常见的妇科肿瘤)和卵巢癌(最致命的妇科癌症)。
在卵巢癌治疗方面,发现一半的患者存在同源重组途径的缺陷,促使将PARP抑制剂用于对铂类化疗有反应的患者的维持治疗。此后,新的预测性和预后性分子生物标志物(如BRCA基因状态和同源重组缺陷[HRD])被添加到治疗流程中,以帮助指导诊断后的治疗。此外,子宫内膜癌的分子分型也揭示了新的预后和预测生物标志物。尤其是具有错配修复缺陷(dMMR)的超突变子宫内膜癌,已被认为是免疫检查点抑制剂治疗的理想候选者。
尽管卵巢癌和子宫内膜癌都取得了这些重大突破,但复发性疾病几乎总是无法治愈的。因此,需要新的治疗策略和抗癌药物。特别是对于PARP抑制剂和免疫检查点抑制剂治疗后疾病复发的患者,迫切需要新的治疗方法,对于这些患者,标准细胞毒性药物似乎活性较低。此外,一些罕见的妇科肿瘤(如外阴癌、非浆液性上皮性卵巢癌)已被排除在新治疗方法的临床试验之外,这些肿瘤的分子特征直到最近才被探索。
PTEN-PI3K-AKT通路在妇科肿瘤中经常发生变异,尤其是在子宫内膜癌(近一半的患者发现PIK3CA突变)和宫颈癌(达70%的患者发现PIK3CA突变)中。尽管如此,仍缺乏PI3K抑制剂的临床活性证据,尤其是在子宫内膜癌和卵巢癌中。阿培利司(BYL719)是一种小分子α特异性PI3K抑制剂,可选择性抑制p110α。阿培利司已被批准与氟维司群联合用于治疗PIK3CA突变的晚期乳腺癌。
本文介绍了迄今最大规模的PIK3CA突变妇科癌症患者系列,这些患者在接受靶向分子分析后接受了阿培利司治疗。这是在管理准入项目队列治疗计划(Managed Access Program cohort Treatment Plan,NCT04085653)前瞻性收集的妇科癌症女性队列中,首次有证据表明PI3K抑制剂有活性。
研究结果
患者:
2021年4月至2022年12月,18个癌症中心的37例患PIK3CA突变晚期妇科癌症的女性被纳入阿培利司管理的入组计划(图1)。在这37例患者中,1例患者从未开始使用阿培利司,因此被排除。子宫内膜癌是最常见的癌症类型(17例患者,47%),其次是卵巢癌(10例患者,28%)和其他癌症类型(9例患者,25%)。
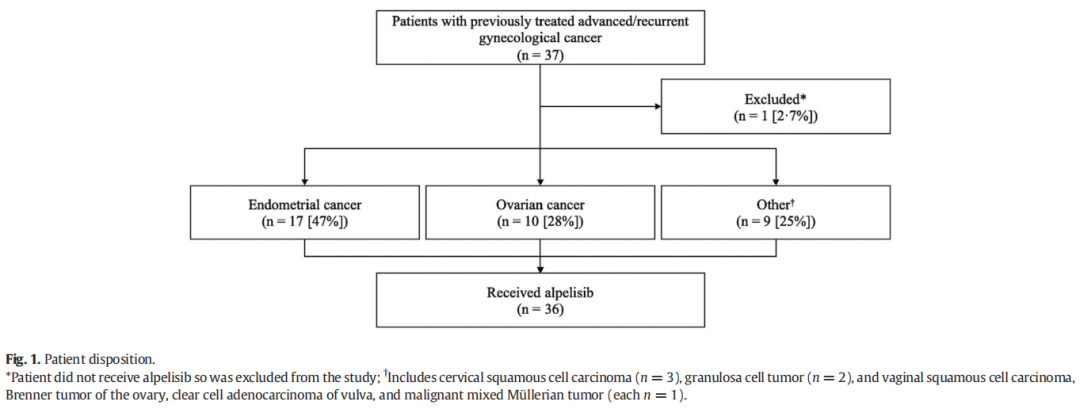
图1
各癌症组患者的基线人口统计学数据和临床特征见表1。子宫内膜癌组的中位年龄为58.1岁,卵巢癌组为50.7岁,其他类型妇科癌症患者为52.0岁。考虑到之前存在的合并症,所有患者均未患2型糖尿病,这是阿培利司潜在毒性的一个值得注意的情况。所有患子宫内膜癌或卵巢癌的患者既往均接受过手术,而22%患其他妇科癌症的患者未接受过手术。在组织学方面,35%的子宫内膜癌为非子宫内膜样亚型,而大多数卵巢癌患者表现为透明细胞癌(60%)。其他癌症类型组包括各种罕见癌症(表1)。
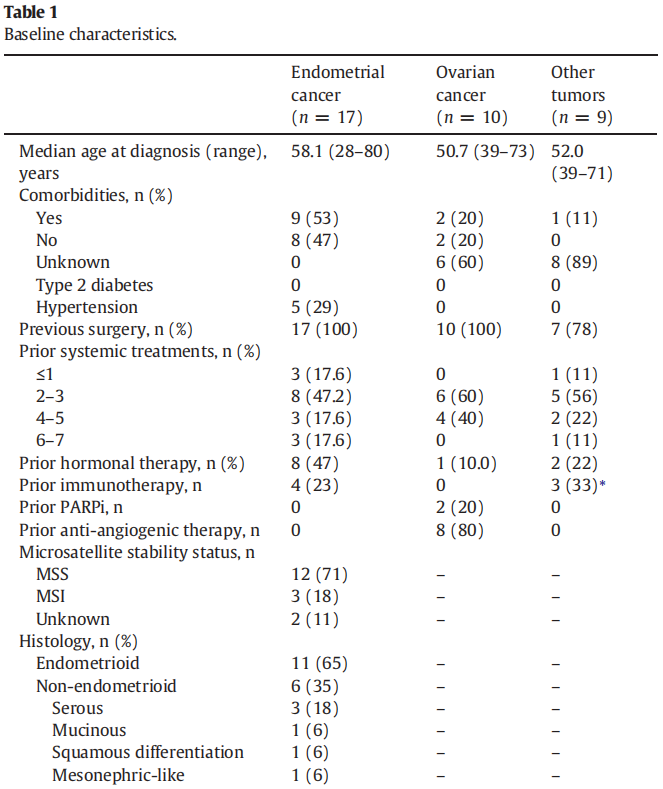
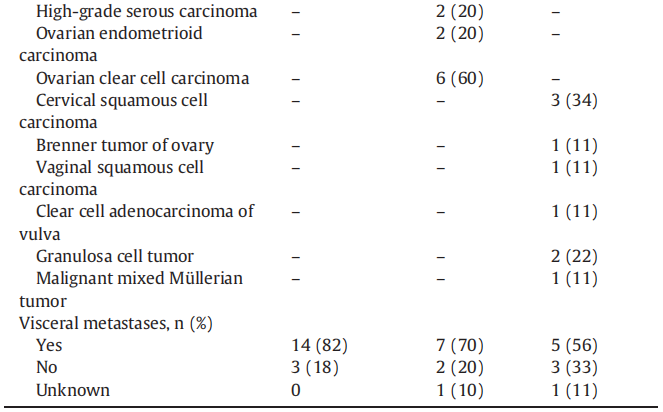
表1
在所有三组中,既往接受过治疗的患者均有很好的代表性。既往治疗线数的中位数为3。在EC(子宫内膜癌)组中,47.2%的患者既往接受过2-3线治疗,值得注意的是,17.6%的患者既往接受过6-7线治疗。特别是EC组有23%的患者既往接受过免疫治疗。同样,在卵巢癌组中,所有患者在阿培利司治疗前均接受了≥2线治疗(2-3,60%;4-5,40%),而在其他癌症类型组中,56%的患者既往接受过2-3线全身治疗,22%既往接受过4-5线治疗。在OC(卵巢癌)组中,20%的患者既往接受过PARP抑制剂治疗,80%的患者接受过抗血管生成治疗。所有患者均未出现BRCA基因的体细胞突变。大多数患者在基线时有内脏转移(子宫内膜,82%;卵巢,70%;其他癌症,56%)。
疗效:
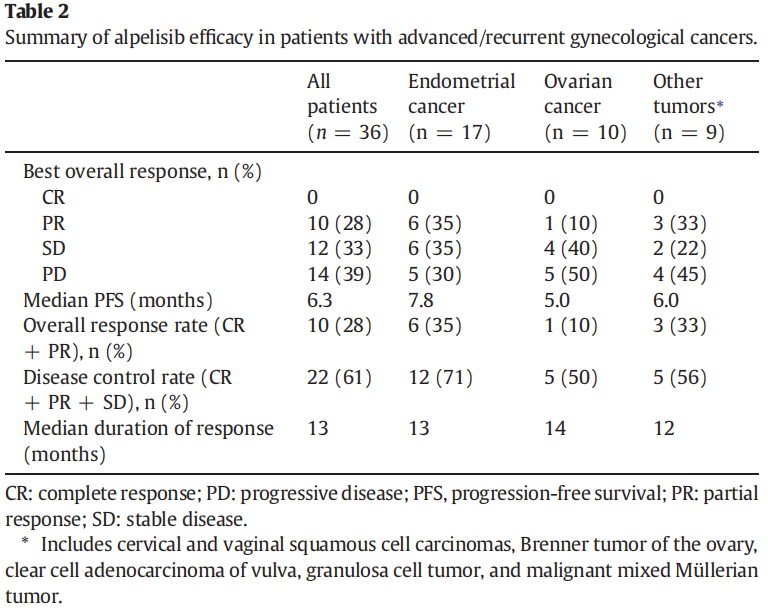
在总体人群和特定肿瘤亚组中进行了疗效分析。在总体患者人群中,ORR为28%,DCR为61%。总体而言,阿培利司治疗后,10例患者(28%)达到了PR(部分缓解),12例患者(33%)达到了SD(疾病稳定)。阿培利司的最大获益见于子宫内膜癌组,DCR为71%。OC组卵巢透明细胞癌患者DCR为50%(2例SD;1例PR)。
总体而言,阿培利司的中位缓解持续时间为13个月(表2)。总体人群的中位PFS(无进展生存期)为6.3个月,观察到的PFS获益最大的是子宫内膜癌组(7.8个月;表2)。此外,在子宫内膜癌患者中,8例患者报告的PFS持续时间≥6个月,其中4例患者PFS≥12个月,1例患者PFS≥24个月。卵巢癌组和其他癌症组的中位PFS分别为5.0个月和6个月。
表2
分子分析:
共观察到16种不同的PIK3CA突变(表3),其中5例患者存在不同的PIK3CA突变共表达。总体人群中约一半(19/36[53%])在激酶结构域携带PIK3CA突变,其中H1047R(c.3140A>G)是最常见的突变(14/36[39%])。36%(13/36)的患者存在PIK3CA螺旋结构域突变,其中最常见的突变为E545K(c.1633G>A)。仅考虑疾病控制的患者(22/36),22例患者中有19例(86%)存在激酶区或螺旋结构域突变;具体来说激酶结构域区和螺旋结构域区分别占63%(12/19)和37%(7/19)。
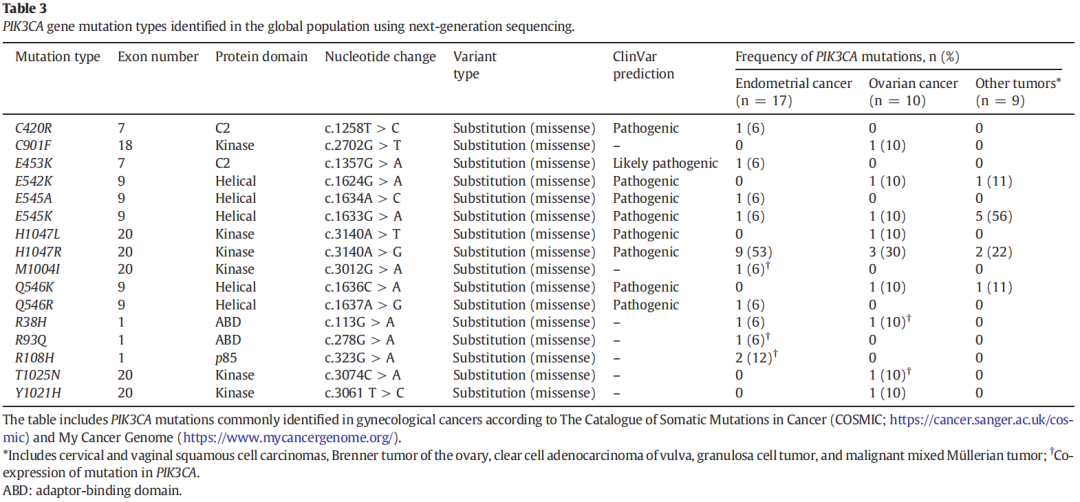
表3
在子宫内膜癌组中,53%(9/17)的患者携带H1047R突变(c.3140A>G),其中78%(7/9)在阿培利司治疗后达到疾病控制。在其他肿瘤类型组中,56%(5/9)的患者携带E545K(c.1633G>A)突变。值得注意的是,其中4例患者患阴道或宫颈鳞状细胞癌,使用阿培利司后,75%(3/4)的患者达到了疾病控制。
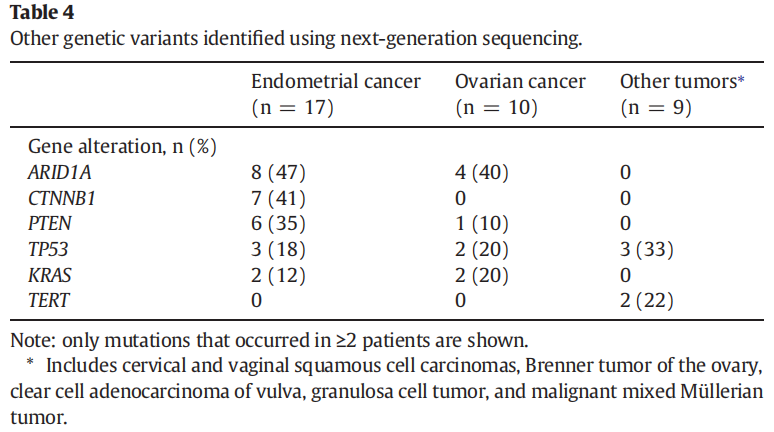
在肿瘤样本中也发现了其他基因变异(表4)。值得注意的是,ARID1A突变发生于67%(4/6)的卵巢透明细胞癌。虽然样本量较小(7/36),但子宫内膜癌患者的PTEN缺失似乎与对阿培利司的反应无关。另一方面,在子宫内膜癌组中,35%(6/17)的患者发生了与PIK3CA变异相关的PTEN突变,其中50%(3/6)的患者达到疾病控制。
表4
安全性:
总体患者人群的安全性(表5)符合阿培利司的已知安全性。观察到的最常见的2级毒性为腹泻(14%)、疲劳(11%)、高血糖(11%)和皮疹(8%)。3-4级不良反应发生率为31%:高血糖11%;皮疹8%;疲劳3%;高血压3%;口腔炎3%;败血症3%;腹泻3%。
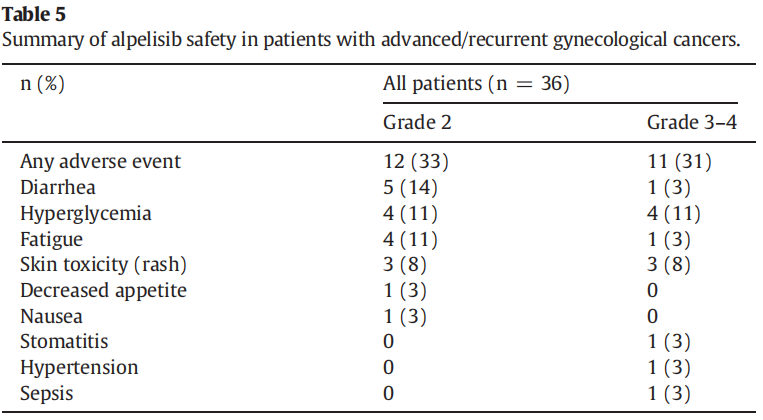
表5
5例患者(14%)因发生2级(腹泻、高血糖、疲劳、食欲下降)和3级不良事件(高血糖、高血压、皮疹)而停止阿培利司治疗。此外,13例患者(36%)至少减量1次。至首次减量的中位时间约为34.3日。
讨 论
在这项大型病例系列中,首次报告了支持阿培利司对PIK3CA突变妇科癌症(尤其是子宫内膜、卵巢和宫颈肿瘤)患者有活性的有力证据。在大约20个月内,阿培利司管理入组计划纳入了37例妇科癌症患者,这表明有大量患者正在接受肿瘤基因组分析,希望在标准治疗发生疾病进展后有资格接受靶向治疗。值得注意的是,在本研究中,37例患者中有7例患透明细胞肿瘤,这是一种罕见的组织学类型,以其化疗耐药闻名,并且似乎因PIK3CA突变而富集。考虑到研究人群既往接受过大量治疗,报告的ORR为28%(子宫内膜,35%;卵巢,10%;其他癌症,33%)、中位PFS为6.3个月(子宫内膜癌,7.8个月)以及4例患者≥12个月的长期疾病控制是值得关注。此外,阿培利司治疗的耐受性一般良好,2-4级不良事件主要为高血糖、皮疹、腹泻或乏力。
PTEN-PI3K-AKT通路变异在妇科癌症中很常见,尤其是在53%的子宫内膜癌病例中发现了PIK3CA突变,这使子宫内膜癌成为PI3K抑制剂评估的理想候选对象。尽管如此,PI3K抑制剂(如阿培利司或其他分子)的活性和疗效仍缺乏有力证据。本研究在既往接受过大量治疗的妇科癌症患者中报道了阿培利司的疗效,这与阿培利司在妇科癌症患者中的其他研究一致。事实上,在之前发表的一份病例报告中,在1例既往接受过广泛治疗的PIK3CA突变的晚期子宫内膜样子宫内膜癌患者中,阿培利司治疗后出现了良好缓解,即7个月时仍持续的部分缓解。此外,在一项回顾性系列研究中,6例既往接受过≥2线治疗的携带PIK3CA突变的晚期/复发性宫颈癌患者接受了阿培利司治疗,研究者判定的经证实ORR为33%,DCR为100%。同样,在一项泛癌症I期试验中,阿培利司的DCR为58%(78/134),包括5名宫颈癌患者中的5名。在这项小型研究中,入组的3例晚期子宫内膜癌患者、14例卵巢癌患者和5例宫颈癌患者。有趣的是,唯一的完全缓解发生于1例子宫内膜癌患者。其他部分缓解见于1例EC和3例宫颈癌患者。
此外,在复发性OC人群中,数项临床研究已将阿培利司作为单药治疗和联合治疗进行了研究,包括在一项Ib期研究中将其与奥拉帕利联合治疗。在这项研究中,接受阿培利司和奥拉帕利联合治疗的胚系BRCA野生型复发性OC患者的ORR为31%(95%CI:11-59;n=16),这一结果优于在BRCA阴性或未知患者中奥拉帕利单药治疗的ORR(4%)。在这方面,一项III期、多中心、开放标签、随机EPIK-O/ENGOT-OV61试验正在无胚系BRCA突变的铂类耐药或难治性高级别浆液性卵巢癌患者中比较阿培利司联合奥拉帕利与标准化疗的疗效(NCT04729387)。
此外,在乳腺癌和妇科恶性肿瘤患者中,一项回顾性I期临床试验报告,PIK3CA突变癌症患者(30%)接受PI3K/AKT/mTOR抑制剂单药治疗或与替代疗法联合治疗后,缓解率显著高于非PIK3CA突变肿瘤患者(10%)。仅考虑EC患者时,缓解率为33%。
本研究关于PIK3CA突变分布的研究结果也与预期一致,即大多数PIK3CA突变发生于螺旋结构域(外显子9)和激酶结构域(外显子20),在53%的患者中观察到激酶结构域突变,在36%的患者中观察到螺旋结构域突变。重要的是,在本研究中,9例H1047R突变子宫内膜癌患者中有78%的患者在阿培利司治疗后实现了疾病控制,4例E545K突变阴道或宫颈鳞状细胞癌患者中有75%的患者在阿培利司治疗后实现了疾病控制。这些结果与1期泛癌研究的结果一致,1期泛癌研究报告了PIK3CA螺旋结构域突变(E545K或E542K)或异常激酶突变(例如T1052K)患者的临床缓解情况。
近期治疗方法的改善改变了晚期子宫内膜癌和卵巢癌的治疗。对于子宫内膜癌,帕博利珠单抗和多塔利单抗(dostarlimab)这两种抗程序性死亡受体-1单克隆抗体在既往接受过治疗的dMMR肿瘤患者中显示出了显著的单药缓解率(分别为48%和42%)。此外,免疫检查点抑制剂与铂类化疗联合应用时,在一线治疗中已证实可延长PFS,尤其是在dMMR人群中,这正在成为新的标准治疗。同样,卵巢癌的治疗也因PARP抑制剂的出现而发生了革命性的变化。在一线治疗中,得益于SOLO-1、PRIMA和PAOLA-1试验的结果,对铂类药物有应答的乳腺癌患者可根据BRCA和HRD状态接受PARP抑制剂维持治疗。
尽管妇科肿瘤学界希望通过免疫疗法和PARP抑制剂治愈越来越多的子宫内膜癌或卵巢癌患者,但复发性子宫内膜癌仍是一个主要问题,原因是卵巢癌患者中PARP抑制剂和铂盐之间存在交叉耐药,并且免疫检查点抑制剂治疗后复发性子宫内膜癌尚无标准治疗方案。此外,透明细胞癌等组织类型被排除在PARP抑制剂等治疗创新之外。
由于这些原因,新的治疗策略和与靶向药物相匹配的新分子靶点仍有待探索。利用NGS对肿瘤基因组谱的评估为靶向治疗提供了可能,正如本研究中阿培利司治疗PIK3CA突变的晚期妇科恶性肿瘤患者所证明的那样。在这种情况下,分子肿瘤委员会在确保将患者转诊到适当靶向治疗的试验中至关重要。
为此,一些值得关注的II期篮子试验如TAPISTRY(NCT04589845)和ROME试验(NCT04591431)正在进行中,也在既往接受过治疗的妇科肿瘤中评估基于分子肿瘤谱的特异性靶向药物。具体而言,TAPISTRY和ROME试验分别评估了inavolisib和ipatasertib作为PI3K/AKT/mTOR通路抑制剂的应用。值得关注的是,另一项II期研究(即BOUQUET,NCT04931342)正在持续性或复发性罕见上皮性卵巢、输卵管或原发性腹膜肿瘤患者中评估多种生物标志物选择疗法的疗效和安全性。该试验包括不同治疗组,如ipatasertib(一种磷酸化AKT的高选择性抑制剂),用于PTEN、PIK3CA和/或AKT1基因发生变化的参与者,以及inavolisib(作为PIK3CA抑制剂),用于有PIK3CA突变的患者。
最后,尽管这项分析是迄今发表的最大的病例系列分析,但研究人群的小样本量和纳入患者的异质性是公认的研究局限性。
阿培利司似乎对携带PIK3CA突变的复发性妇科癌症患者有活性。阿培利司的有效性是有前景的,值得在随机对照试验中进一步验证。最终,本研究证明,当靶向药物在临床实践或临床试验中可获得时,肿瘤基因组图谱可以打开治疗格局,促进精准医疗。
参考文献:
Passarelli A, Carbone V, Pignata S, et al. Alpelisib for PIK3CA-mutated advanced gynecological cancers: First clues of clinical activity. Gynecol Oncol. Published online March 21, 2024. doi:10.1016/j.ygyno.2024.02.029



