Mol. Psychiatry:通过靶向 GPR55 调节神经炎症和氧化应激——治疗精神疾病的新方法
时间:2024-06-11 18:00:55 热度:37.1℃ 作者:网络
精神疾病的药物治疗在临床、药理学和科学实践中仍然具有挑战性。即使建立了许多不同的物质来治疗不同的精神疾病,患者亚组也只对治疗表现出很小或没有反应。精神疾病起源的神经炎症假说可能解释了这些无反应者的潜在机制。出于这个原因,本综述探讨了最近的研究集中在神经炎症过程和氧化应激作为精神疾病的可能原因。

G蛋白偶联受体(GPCRs)是膜结合受体的最大超家族,在各种疾病中已经是众所周知的药理学靶点。G蛋白偶联受体55(GPR55)是一种被认为是内源性大麻素系统一部分的受体,它揭示了对神经炎症和氧化过程的有希望的调节。
不同的激动剂和拮抗剂可减少促炎细胞因子的释放,增强抗炎介质的合成,并保护细胞免受氧化损伤。出于这个原因,GPR55配体可能是治疗患有与神经炎症或氧化应激相关的精神疾病患者亚组的有前途的化合物。药物设计的新方法可能会导致仅在一个分子中针对这些疾病的不同病理机制的新化合物。
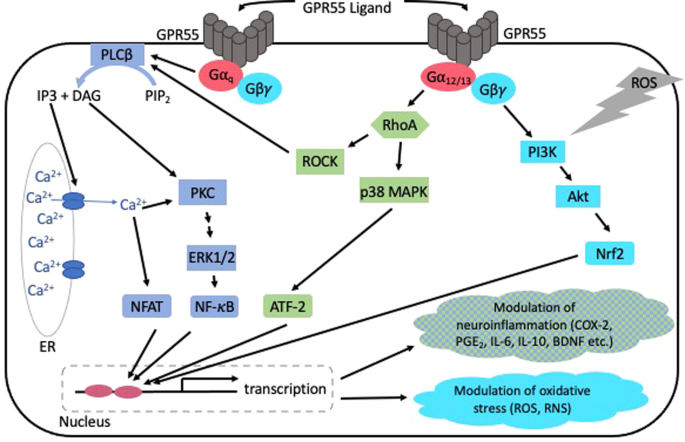
图1:GPR55依赖性信号通路及其效应的简化概述
对于 GPR55、Gα12,Gαq和 Gα13 依赖性信号转导,导致磷脂酶(PLC)和GPR55依赖性RhoA的激活。与GPR55偶联的Gα蛋白启动进一步的下游信号通路,例如与Erk1/2磷酸化的丝裂原活化蛋白激酶(MAPK)通路,激活转录因子,如Nrf2,并因此改变基因表达和蛋白质合成(图1)。然而,另一种细胞内信号传导可以被已知的GPR55激动剂和具有反向激动特性的拮抗剂激活。
表1 不同GPR55配体的促炎和抗炎作用

偏向激动导致理解已知拮抗剂在GPR55上的意外行为的新方法。LPI 和另一种 GPR55 激动剂 virodhamine 通过 GPR55 在 GPR55 转染的 HEK293 细胞中诱导细胞内钙释放。然而,LPI主要通过Gα起作用q和 PLCβ,而 virodhamine 的作用依赖于 Gα13、PLCε和Rho-/ROCK通路,在GPR55处显示出偏倚的激动作用。
在精神和神经精神疾病中,GPR55的作用仍然是正在进行的研究的重点。研究表明,O-1602通过调节炎症过程改善了小鼠慢性社交失败压力诱导的抑郁和焦虑样行为。对于精神分裂症,一些作者认为CBD通过抑制GPR55具有潜在的抗精神病作用。不仅GPR55的表达、合成和信号传导可能引起人们的兴趣,而且由于异二聚化引起的功能变化也可能发生,这应该是未来研究的一部分。
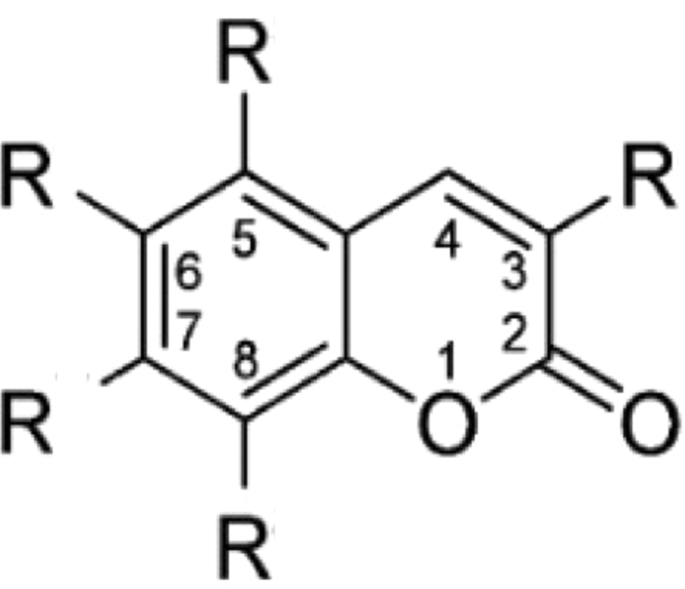
图2:具有可能残基的香豆素支架
除了神经炎症外,如果细胞的抗氧化机制耗尽,氧化应激也会损害细胞,导致神经退行性疾病,如AD。只有少数研究关注氧化应激中的GPR55。这些研究特别研究了NOS的影响。研究表明,在5xFAD小鼠中,iNOS合成与GPR55蛋白水平呈负相关。
表2 不同GPR55配体的促氧化和抗氧化作用
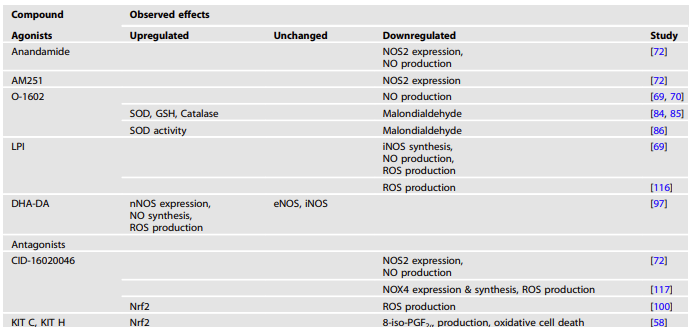
与神经炎症相反,没有研究专门关注GPR55在氧化应激中的作用,作为精神疾病的共同原因。这里介绍的研究表明,GPR55在氧化稳态的调节中具有调节作用;然而,GPR55激动剂和拮抗剂的抗氧化作用已被证明。需要注意的是,所研究的拮抗剂可能通过GPR55的反向激动活性来增强其抗氧化特性。因此,GPR55是与炎症和氧化失调相关的精神和神经精神疾病的一个有前途的靶点
原始出处:
Apweiler, M., Saliba, S.W., Sun, L. et al. Modulation of neuroinflammation and oxidative stress by targeting GPR55 – new approaches in the treatment of psychiatric disorders. Mol Psychiatry (2024). https://doi.org/10.1038/s41380-024-02614-5


