NAT MED | 博特利单抗加巴替利单抗治疗复发/难治性微卫星稳定转移性结直肠癌:1 期试验
时间:2024-06-20 14:00:32 热度:37.1℃ 作者:网络
结直肠癌 (CRC) 是美国癌症相关死亡的第二大原因,死亡率在年轻人中有所上升,虽然化疗和靶向治疗取得了一些进展,但晚期 CRC 患者的预后仍然很差,特别是对于微卫星稳定 (MSS) 的转移性结直肠癌 (mCRC) 患者,免疫检查点抑制剂 (ICB) 在多种癌症中取得了成功,但在 MSS mCRC 中的疗效却令人失望,这主要是因为 MSS mCRC 肿瘤微环境 (TME) 具有免疫抑制性,缺乏免疫原性,该研究旨在评估新型多功能 Fc 增强型抗 CTLA-4 抗体 博特利单抗 (BOT) 单药或与 PD-1 抑制剂 巴替利单抗 (BAL) 联合治疗 MSS mCRC 患者的安全性和耐受性。

方法
该研究是一项开放标签,I 期,多中心临床试验,评估 BOT 单药或与 BAL 联合治疗 MSS mCRC 患者的安全性、耐受性、药代动力学和药效学特征,并确定最大耐受剂量和推荐 II 期剂量,纳入的患者年龄 ≥ 18 岁,具有可测量的疾病,ECOG 体能状态为 0 或 1,既往接受过 ICB 治疗的患者也可入组,这些患者确诊为转移性或局部晚期实体瘤,且标准治疗无效或无标准治疗可用。
剂量递增阶段: BOT 单药:Q3W 或 Q6W,剂量范围为 0.1 mg/kg 至 3 mg/kg,静脉注射给药,最长 2 年。BOT + BAL 联合治疗:BOT Q3W 或 Q6W,剂量范围为 0.1 mg/kg 至 3 mg/kg;BAL Q2W,剂量为 3 mg/kg,静脉注射给药,最长 2 年。剂量扩展阶段:BOT 1 mg/kg 或 2 mg/kg Q6W + BAL 3 mg/kg Q2W。主要终点为剂量递增阶段单药和联合治疗队列患者在前 28 天内 DLT 的发生率,次要终点为所有剂量组治疗相关不良事件 (TEAE) 和实验室异常的严重程度和持续时间,BOT 和 BAL 的药代动力学和免疫原性,ORR、DOR、DCR 和 PFS。
研究结果
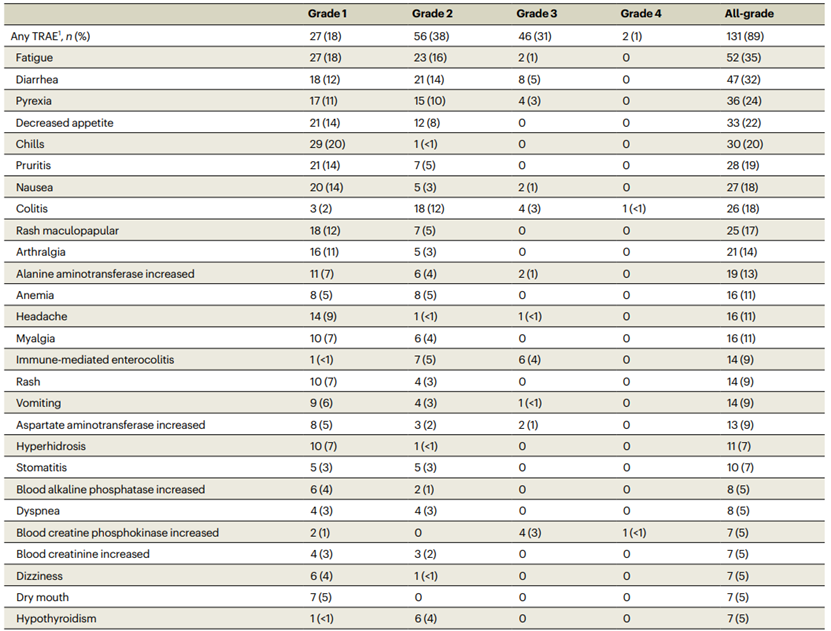
剂量递增阶段:未观察到剂量限制性毒性 (DLT)。剂量扩展阶段:在接受 BOT + BAL 联合治疗的 148 名 MSS mCRC 患者中,89% 出现了治疗相关不良事件 (TRAE),主要表现为疲劳、腹泻和发热,但安全性可控,49% 的患者出现了免疫介导的 TRAE,最常见的是腹泻/结肠炎 (33%),其次是皮肤反应 (18%) 和肝炎 (12%),35% 的患者出现了严重的 TRAE,22% 为 3 级,1% 为 4 级,32% 的患者因 TRAE 中断了研究药物,28% 的患者因 TRAE 停止了所有研究药物,没有治疗相关的死亡事件。
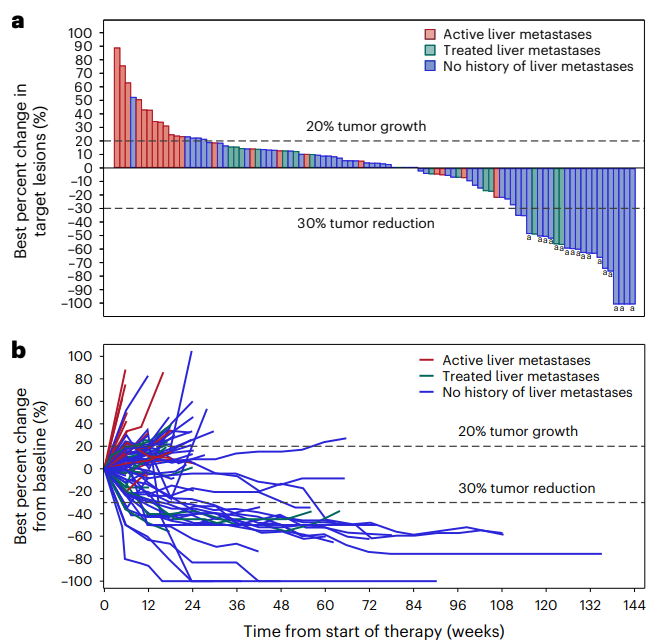
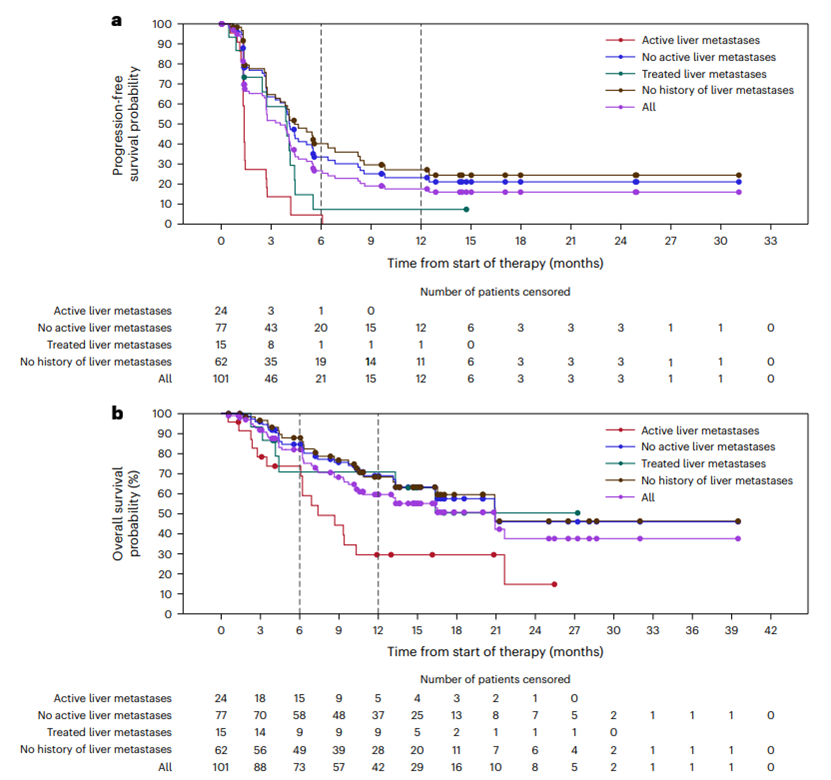
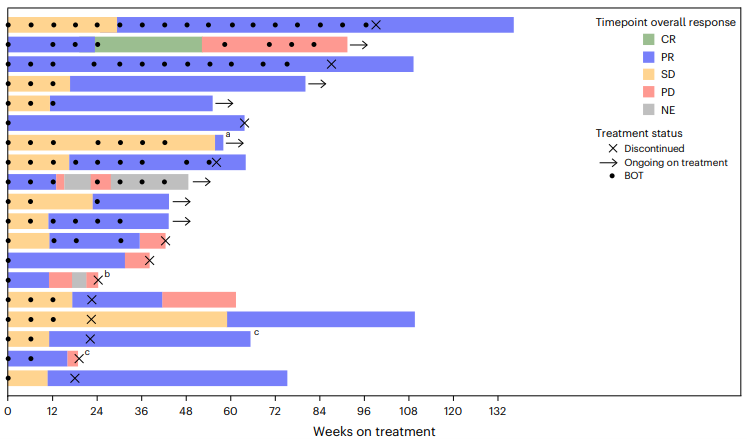
剂量递增阶段:在 83 名患者中,8 名 (10%) 出现了客观缓解,其中包括 3 名 MSS mCRC 患者。剂量扩展阶段:在 101 名可评估疗效的患者中,17 名 (17%) 出现了客观缓解,其中包括 1 名完全缓解 (CR),45 名患者 (45%) 出现了疾病稳定 (SD),DCR 为 61%,中位 DOR 未达到,95% CI 为 5.7 个月至未达到,中位 PFS 为 3.5 个月,95% CI 为 2.7-4.1 个月,中位 OS 为 20.9 个月,95% CI 为 10.6 个月至未达到。无肝转移患者的 ORR 为 22%,DCR 为 73%,中位 PFS 为 4.1 个月,中位 OS 为 20.9 个月。肝转移患者的 ORR 为 0%,DCR 为 25%,中位 PFS 为 1.4 个月,中位 OS 为 7.4 个月。
结论
BOT + BAL 组合在 MSS mCRC 患者中显示出可控的安全性和令人鼓舞的疗效,为治疗 MSS mCRC 提供了新的选择,无肝转移可能是一个重要的预测 ICB 治疗效力的生物标志物,需要进一步的研究来确认 BOT + BAL 组合的疗效,并探索克服肝转移患者免疫抑制 TME 的策略。
原始出处
Bullock, A.J., Schlechter, B.L., Fakih, M.G. et al. Botensilimab plus balstilimab in relapsed/refractory microsatellite stable metastatic colorectal cancer: a phase 1 trial. Nat Med (2024). https://doi.org/10.1038/s41591-024-03083-7.


