从试验数据到临床实战:贝福替尼II期最终总生存率见刊Lung Cancer
时间:2024-08-21 14:00:32 热度:37.1℃ 作者:网络
2019年,广东一名54岁男性患者叶某被确诊为IV期肺腺癌,伴随胸膜转移和恶性胸腔积液。作为非小细胞肺癌(NSCLC)的常见亚型,肺腺癌患者通常存在EGFR基因突变,该患者也不例外,并接受了一代EGFR-TKI一线治疗。然而,在随后的基因检测中,提示该患者合并T790M突变。
尽管第三代EGFR-TKI药物的开发和应用已经显著改善了T790M突变引起的一、二代EGFR-TKI耐药问题,患者的生存时间得到了延长,但对于晚期NSCLC患者而言,进一步延长总生存期仍是临床治疗的重要目标。奥希替尼作为首个获得批准的第三代EGFR-TKI,凭借AURA3 研究在二线治疗EGFR T790M突变的NSCLC患者中展现出显著的临床疗效,并在一线治疗中进一步获得认可。然而,尽管奥希替尼在延长患者总生存期和延缓疾病进展方面表现出色,但仍然存在一定的局限性。近年来,国内批准伏美替尼和阿美替尼用于EGFR突变阳性的NSCLC的治疗一、二线治疗,韩国也批准了拉泽替尼用于EGFR T790M突变的NSCLC患者,进一步扩展了针对EGFR突变阳性患者的治疗选项。
然而,在 EGFR 敏感突变患者中,脑转移的发生率高达48%~50%,远超普通NSCLC患者的25%。尽管上述药物在治疗EGFR T790M突变的NSCLC患者中提供了更多选择,但仍然无法切实解决脑转移的痛点,迫切需要具有改善中枢神经系统(CNS)活性的新型EGFR-TKI。在此背景下,贝福替尼应运而生。
从临床前到实战应用贝福替尼三项全能
作为新一代能够穿透血脑屏障的第三代EGFR-TKI,贝福替尼对EGFR激活突变和T790M耐药突变的患者具有高度选择性。临床前研究显示,贝福替尼对携带EGFR-19Del和T790M突变的NSCLC细胞株有显著抑制作用,而对野生型EGFR细胞的影响较弱,表明其对突变细胞的选择性更强;此外,贝福替尼在动物模型中展现出良好的脑部穿透能力,脑部浓度是血浆的十倍以上,这进一步证明了其在脑转移治疗中的潜力;在临床应用上,贝福替尼也经过实战验证:在本文开头便提到的典型病例中,这名EGFR T790M突变的IV期肺腺癌男性患者,在二线接受了一段时间的贝福替尼治疗后,患者的CEA水平明显下降,病灶缩小并趋于稳定。这一治疗策略的成功也为临床医生在类似病例中选择贝福替尼作为二线治疗方案提供了有力支持。
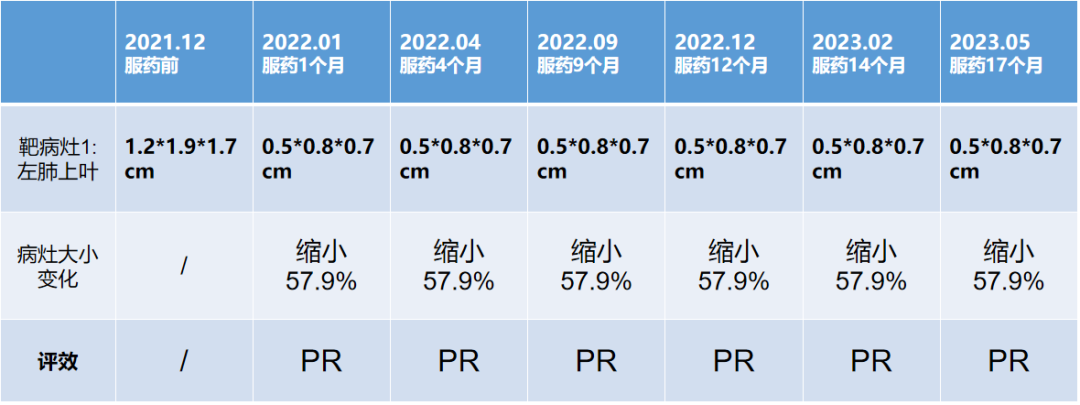
贝福替尼疗效评估
追溯至2023年,有关贝福替尼二线治疗经治EGFR T790M 阳性局部晚期或转移性非小细胞肺癌 (NSCLC)的研究便以Final overall survival (OS) results of befotertinib in patients with pretreated EGFR T790M-positive locally advanced or metastatic non-small cell lung cancer (NSCLC)的标题亮相欧洲肿瘤内科学会亚洲年会(ESMO Asia),引起了广泛关注——就在不久前,该研究于2024年7月26日正式被Lung Cancer收录。

研究设计与方法
该研究是一项单臂、开放标签、2 期研究,旨在评估贝福替尼在经治EGFR T790M突变阳性局部晚期或转移性非小细胞肺癌患者中的疗效和安全性。研究的主要终点是由独立审查委员会评估的客观缓解率(ORR),而次要终点则包括总生存期(OS)、颅内无进展生存期(iPFS)和安全性。此外,还评估了健康相关的生活质量(HRQoL)。
研究对象
研究纳入了EGFR T790M阳性且已接受过第一代或第二代EGFR-TKI治疗的局部晚期或转移性NSCLC成年患者。患者按两个不同的剂量方案分为两组:A组患者每日口服50 mg 贝福替尼,每日一次,21 天为一个周期;B组患者每日口服75 mg,如果第一个周期内没有发生2级或更高级别的不良事件,则剂量增加至100 mg,反之则维持每天75mg的剂量。研究期间,所有患者每6周进行一次肿瘤评估,直至疾病进展或治疗终止。截止2023年5月31日, A 组的中位治疗暴露时间为 9.8 个月(IQR:5.5-17.1),B组为 11.2 个月(IQR:5.5-18.1),其中78 名剂量未升级至 100 mg 的患者为 8.4 个月(IQR:3.0-13.9),而 212 名剂量升级至 100 mg 的患者为 12.5 个月(IQR:6.8-20.7)。
关键研究结果
1 不同剂量生存期均延长
研究表明,贝福替尼在治疗EGFR T790M突变的非小细胞肺癌(NSCLC)患者中表现出了显著的总生存期(OS)延长。在A组患者中,中位OS为23.9个月(95% CI: 21.1–27.2),而在B组患者中,中位OS则更长,达到31.5个月(95% CI: 26.8–35.3)。此外,12个月和24个月的预计生存率在A组分别为84.5%和49.0%,而在B组则为86.4%和60.5%。这些数据表明,贝福替尼在不同剂量下均能有效延长患者的生存期。
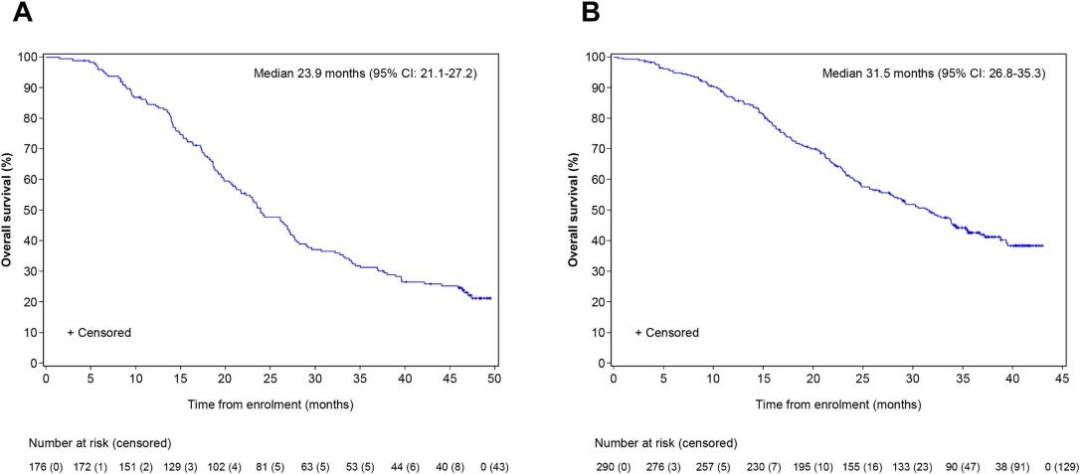
接受 Befotertinib 治疗的患者的总生存期
( A ) 队列 A 总生存率的 Kaplan-Meier 曲线
( B ) 队列 B 总生存率的 Kaplan-Meier 曲线
2 脑转移患者的获益
对于有脑转移的患者,贝福替尼同样展现了显著的治疗效果。在A组患者中,伴随脑转移的患者中位OS为18.6个月(95% CI: 14.9–26.3),而无脑转移的患者中位OS为26.4个月(95% CI: 23.0–29.0)。在B组中,这一获益更加明显,伴随脑转移的患者中位OS为23.0个月(95% CI: 18.6–29.1),而无脑转移的患者中位OS则延长至35.5个月(95% CI: 29.3–NE)。这些结果体现了贝福替尼给脑转移患者带来了治疗获益,而无脑转移患者的生存期更长。
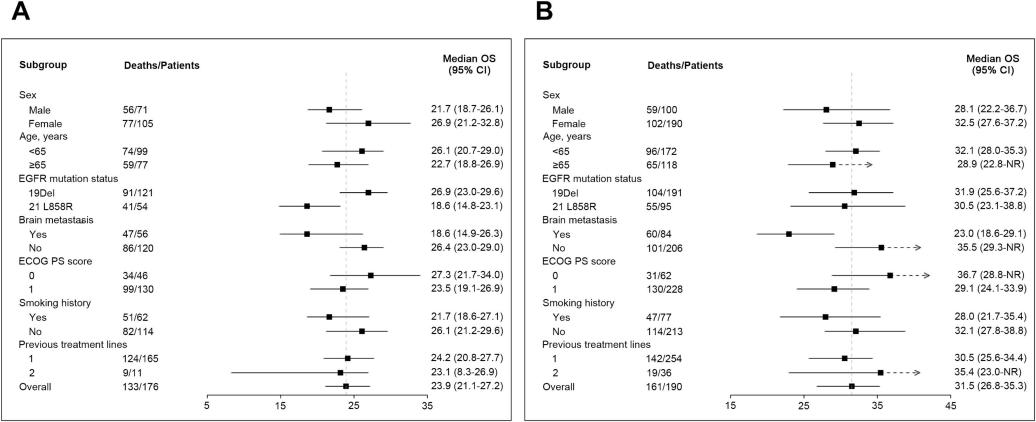
总生存期的亚组分析
( A ) 队列 A 中的森林图
( B ) 队列 B 中的森林图
3 安全性评估良好
在安全性方面,贝福替尼的耐受性总体良好,且与之前的研究数据一致。A组和B组的治疗相关不良事件(TRAEs)分别为85.8%和93.8%,其中3级或以上TRAEs的发生率分别为22.2%和31.7%。最常见的TRAEs包括血小板减少症、贫血和白细胞减少症,A组的发生率分别为52.8%、19.9%和19.9%;B组则为65.2%、25.2%和15.5%。尽管有部分患者出现了严重的不良事件(SAEs),但大多数情况下可以通过剂量调整和对症治疗来管理。大多数病例的严重程度为 1 级或 2 级,B 组中有两例 (0.7%) 报告为 3 级和 5 级。
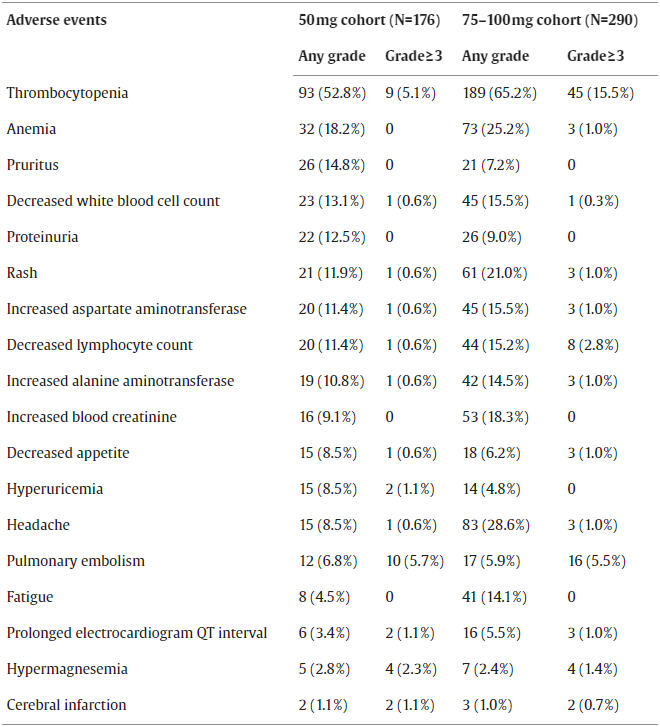
治疗相关的不良事件
4 生活质量改善
研究显示,贝福替尼在改善患者生活质量(HRQoL)方面也有积极作用。基于FACT-L、LCS和TOI的评估结果,A组和B组的患者在治疗的前33个周期中均显示出HRQoL的改善趋势。A组的TOI得分、LCS得分和总FACT-L得分分别有56.8%、61.9%和62.5%的患者得到改善,B组的相应数据则为42.1%、49.7%和47.2%。这些结果表明,贝福替尼不仅延长了患者的生存期,还在一定程度上提高了他们的生活质量。
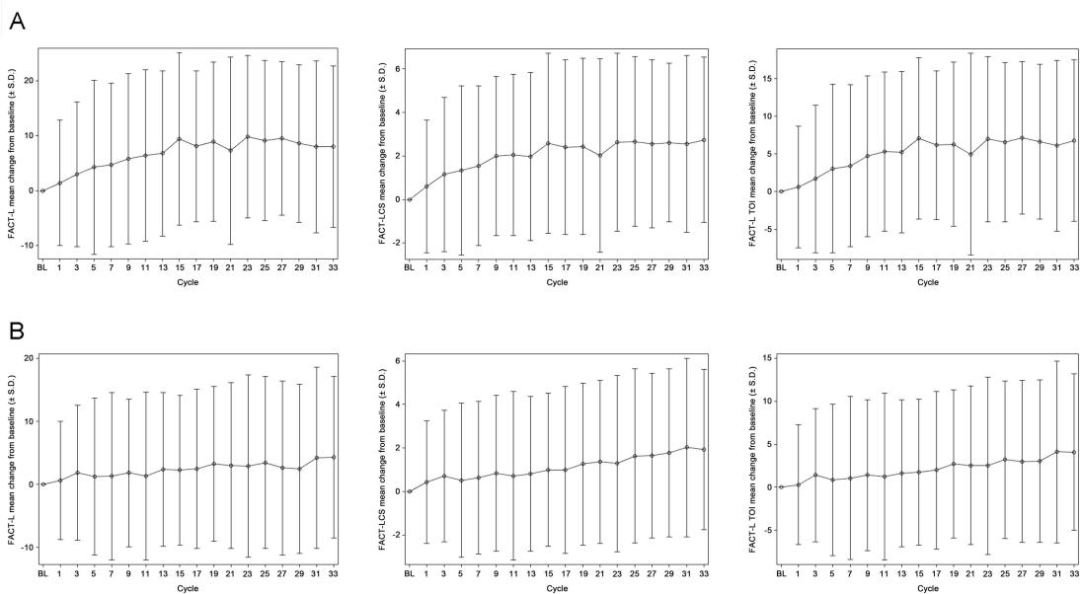
HRQoL 分数随时间相对于基线的平均变化
( A ) 队列 A 中的 FACT-L、LCS 和 TOI 评分
( B ) 队列 B 中的 FACT-L、LCS 和 TOI 评分
5 后续治疗
在最终 OS 分析的数据截止时,队列 A 中的 126 名患者和队列 B 中的 159 名患者接受了首次后续抗癌治疗,分别占各自队列中所有患者的 71.6% 和 54.8%。最常用的治疗是第三代 EGFR TKI,其中最常见的是奥希替尼。A 组的治疗持续时间为 4.1 个月,B 组的治疗持续时间为 6.1 个月。此外,队列 A 中的 60 名患者(34.1%)和队列 B 中的 60 名患者(20.7%)接受了第二次后续抗癌治疗。
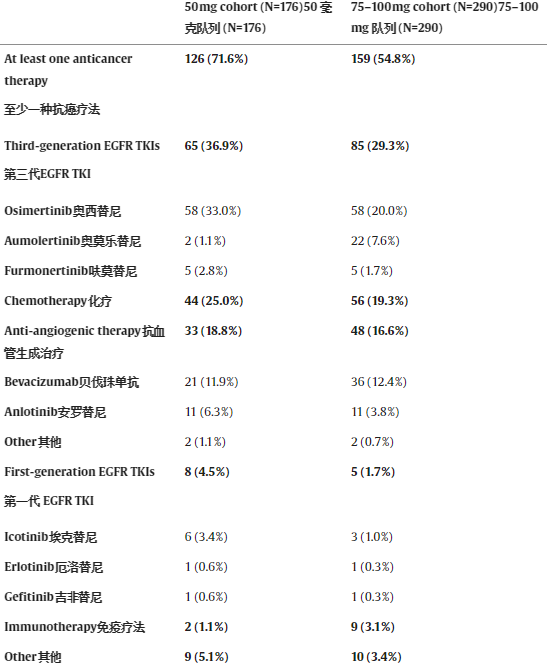
贝福替尼的首次后续抗癌治疗进展
结果进一步支持贝福替尼二线治疗中国非小细胞肺癌患者
本研究的最终分析结果表明,贝福替尼在EGFR T790M突变的局部晚期或转移性非小细胞肺癌(NSCLC)患者中,特别是在已经接受过第一代和第二代EGFR-TKI治疗后,无论患者的年龄、性别、组织学类型、EGFR 突变类型和是否存在脑转移,都展现出了显著的临床益处,且长期使用贝福替尼治疗的毒性通常也可控。
在两组患者中,贝福替尼均显著延长了总生存期(OS),其中A组(50 mg)的中位OS为23.9个月,B组(75-100 mg)的中位OS则达到了31.5个月,前者的中位 OS 与奥希替尼相当,而后者甚至超过了奥希替尼在相似患者群体中已发表的生存数据(AURA3研究中位 OS 为 26.8 个月;AURA Extension/AURA2中二线的中位 OS 为 26.5 个月;AURA17 研究中位 OS 为 23.2 个月)。
此外,不论是低剂量(50 mg)还是常规剂量(75-100 mg),两个队列的CNS活性都十分稳健,且在75-100 mg 时贝福替尼的CNS活性更优。对于脑转移患者,与低剂量相比,常规剂量贝福替尼的 OS 有所改善;而对于无脑转移的患者,常规剂量贝福替尼的 OS 明显长于低剂量。
这些结果不仅强调了贝福替尼作为第二代治疗药物的有效性,还进一步巩固了其在具有脑转移患者中的治疗优势。
未来展望
尽管研究主要在中国患者中进行,但这些数据为贝福替尼在全球范围内的广泛应用奠定了基础,特别是对于伴有脑转移或存在其他复杂临床背景的NSCLC患者。未来,相关研究应继续关注贝福替尼在不同种族群体中的疗效和安全性差异。其次,鉴于贝福替尼在不同EGFR突变类型(如19Del和21 L858R)患者中的生存获益存在差异,研究缺乏分子生物标志物分析,值得进一步的分子生物学研究探索可能的耐药机制,有助于优化患者的个体化治疗方案。
通过将个体病例与临床研究成果相结合,我们看到贝福替尼不仅在实验室和临床试验中取得了显著成果,更在实际的临床应用中为患者带来了切实的治疗获益。此外,在本次研究公布的数据中,贝福替尼展现出了在延长生存期、管理脑转移和改善生活质量方面的强大潜力,有望成为EGFR T790M突变阳性、晚期NSCLC患者新的标准治疗选择。


