Translational Psychiatry:锂反应与PI3K-Akt信号通路之间功能性连接的趋同证据
时间:2024-11-06 12:00:44 热度:37.1℃ 作者:网络

近年来,研究表明锂作为一种用于治疗双相情感障碍(BD)的药物,通过作用于PI3K-Akt信号通路调节神经元生长锥的形成和神经突的延伸。该机制首次通过全基因组关联研究(GWAS)、多组学分析和基因组网络分析发现,随后在模式生物秀丽隐杆线虫(Caenorhabditis elegans)中得到验证。PI3K-Akt信号通路不仅在胰岛素受体的作用下激活,还涉及多种生长因子,如神经生长因子(NGF)和脑源性神经营养因子(BDNF)。此外,锂的作用还与一系列钙通道的活性密切相关。研究通过对线虫的分子遗传学研究进一步证明了其在精神病学研究中的应用潜力。
在方法上,研究采用了C. elegans作为模式生物,利用分子遗传学技术探讨锂的作用机制。线虫的DAF-16转录因子(相当于人类的FOXO蛋白)在饥饿状态下进入细胞核,但锂通过PI3K-Akt信号通路的激活阻止了这一过程。实验通过分析不同基因突变株的表现,确定了G蛋白和PDK-1在锂诱导的Akt激活中的关键作用。尤其重要的是,锂对Akt的激活与β-arrestin和血清-糖皮质激酶(SGK-1)的功能相关,这一发现与先前的研究结果高度一致。图1展示了锂信号通路的主要组成部分和对DAF-16的作用,验证了秀丽隐杆线虫作为研究精神病学药物的有效性。
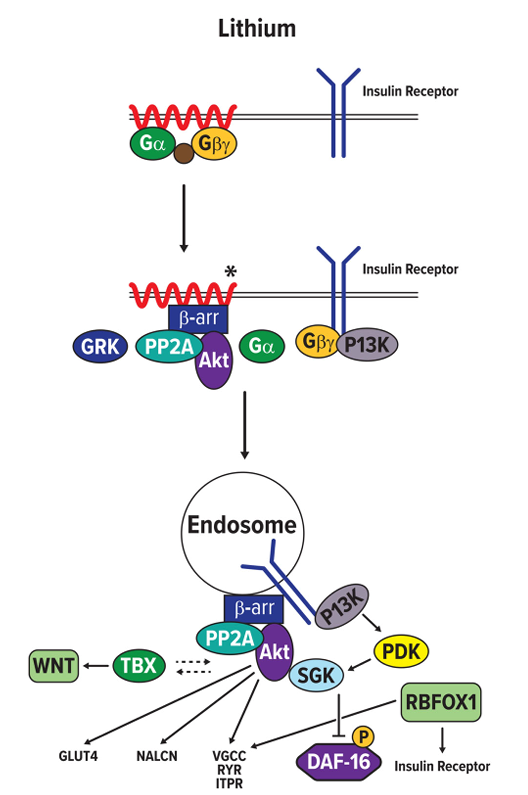
图1:锂信号通路及相关靶点在C. elegans中的作用示意图。锂通过胰岛素受体、G蛋白、β-arrestin、PDK-1、Akt和SGK-1作用于DAF-16转录因子的磷酸化,调节电压门控钙通道(VGCC)、Ryanodine受体(RYR)、NALCN钠漏通道及ITPR2受体的功能。TBX转录因子与Wnt和胰岛素信号通路交互,RNA结合蛋白RBFOX1调控VGCC和胰岛素受体基因的剪接
实验结果表明,锂的作用不仅限于常见的信号通路,还涉及钙相关通道的调节,包括钙通道CACNA1C、ITPR2及NALCN钠漏通道,这些基因已被识别为与BD相关的风险基因。此外,锂对某些线虫突变株的行为有正向作用,如提高目标导向行为,但对tbx-2突变株却产生相反作用。tbx-2是与自杀风险相关的人类TBX20转录因子的同源物。此突变影响线虫的特殊发育阶段(即dauer期),而此阶段与饥饿和环境压力密切相关,进一步说明了锂对胰岛素信号和pdk-1的依赖性。研究还揭示了RBFOX1基因的作用,其在人类中影响胰岛素受体和钙通道的剪接。
结果显示,锂作用的分子靶点仍需进一步研究,但现有数据支持其通过PI3K-Akt信号调控神经元的生长和存活。此外,锂的神经保护作用可能是通过调控钙稳态实现的,这在双相情感障碍中具有重要意义。尽管PI3K-Akt途径还受到其他信号分子的调控,如G蛋白偶联受体,但锂的作用显示了其独特的功能特性。通过与网络基因组学研究结果的结合,现有的多组学证据进一步增强了对PI3K-Akt通路在锂治疗中的作用的信心。
原出处处:
Dwyer DS. Converging evidence for functional connections between the lithium response and PI3K-Akt signaling. Transl Psychiatry. 2024;14:458. doi: 10.1038/s41398-024-03160-y


