Nature:肠道小卫士,抗癌大英雄 - 揭秘益生菌如何变身癌症克星!
时间:2024-11-07 06:00:23 热度:37.1℃ 作者:网络
癌症治疗领域正经历着一场革命,特别是在免疫治疗方面,科学家们正在探索利用肠道益生菌如大肠杆菌Nissle 1917(EcN)作为癌症疫苗的载体,以激活或增强患者自身的免疫系统来识别和攻击癌细胞。
这些益生菌因其在人体肠道中的共生特性和良好的安全性记录,被认为是理想的癌症疫苗载体,它们能够自然地定位到肿瘤部位并调节抗肿瘤免疫反应。随着基因工程改造技术的进步,益生菌能够被改造以携带和传递特定的治疗性蛋白或抗原,为开发新型癌症疫苗提供了新的可能性【1】。
2024年10月16日,Andrew Redenti 在国际顶尖学术期刊 Nature 上发表了题为 Probiotic neoantigen delivery vectors for precision cancer immunotherapy的研究论文【2】。
-
本研究旨在开发一种基于益生菌的新型癌症疫苗平台,通过工程化改造大肠杆菌Nissle 1917(EcN),使其能够增强产生和细胞内传递含有新表位的多肽阵列,从而提高疫苗的安全性和免疫原性。
-
研究成功构建了一种基于工程化益生菌的新型癌症疫苗平台,该平台能够有效控制或消除小鼠原发性和转移性实体肿瘤的生长,并延长生存期。

主要研究内容和结果
工程化益生菌的构建与优化:
-
研究者们通过合成生物学技术,对EcN进行了基因改造,以增强其生产和细胞内传递含有新抗原的多肽阵列的能力。
-
通过去除隐秘质粒和敲除Lon和OmpT蛋白酶,增加了新抗原的积累,提高了细菌对吞噬细胞的敏感性,从而增强了抗原呈递细胞(APCs)的吞噬和MHC类II限制性抗原的呈递。
-
表达listeriolysin O (LLO)以促进编码新抗原的细胞质内传递,增强TH1型免疫反应。
增强免疫原性和安全性:
工程化细菌EcNc Δlon/ΔompT比原始EcN株对血液清除的敏感性提高了1000倍,对吞噬细胞的敏感性提高了4倍,显著减少了生物膜形成,增强了治疗的安全性。
激活免疫反应:
在小鼠模型中,工程化细菌能够激活树突状细胞(DCs),引发新抗原特异性的CD4+和CD8+ T细胞的广泛激活,增强了T细胞和自然杀伤(NK)细胞的活性,并减少了肿瘤浸润的免疫抑制性髓系和调节性T细胞及B细胞。
抗肿瘤效果:
-
在CT26肿瘤模型中,单次肿瘤内注射EcNcΔlon/ΔompT/LLO+ nAg19(包含19个独特新抗原的疫苗)导致了3/7的肿瘤完全消失,显示出强大的抗肿瘤效果。
-
在B16F10黑色素瘤模型中,静脉注射EcNcΔlon/ΔompT/LLO+ nAg42(包含42个独特新抗原的疫苗)显著抑制了肿瘤生长,72%的nAg42治疗小鼠在肿瘤植入后50天仍然存活,而对照组小鼠在24或30天内全部死亡。
系统性抗肿瘤免疫:
-
通过单次肿瘤内注射或静脉注射,工程化细菌能够刺激产生系统性的抗肿瘤免疫反应,有效控制甚至消除远处未注射的肿瘤。
-
在CT26肿瘤模型中,单次肿瘤内注射EcNcΔlon/ΔompT/LLO+ nAg19后,2/6的注射和未注射肿瘤完全消退。
对转移性肿瘤的治疗效果:
-
在CT26-Luc肺转移模型中,静脉注射EcNcΔlon/ΔompT/LLO+ nAg19强烈抑制了转移性生长,100%的nAg19治疗小鼠在植入后45天存活,而对照组小鼠全部死于疾病。
上述研究结果提供了一种新的癌症免疫疗法的有力证据,即通过工程化益生菌传递肿瘤特异性新抗原,能够激活机体的免疫系统,有效对抗肿瘤的生长和转移。
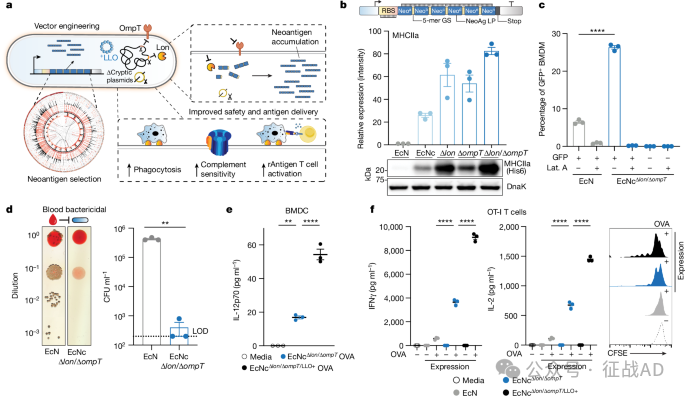
图1. 工程化活体微生物肿瘤新抗原疫苗的设计和构建
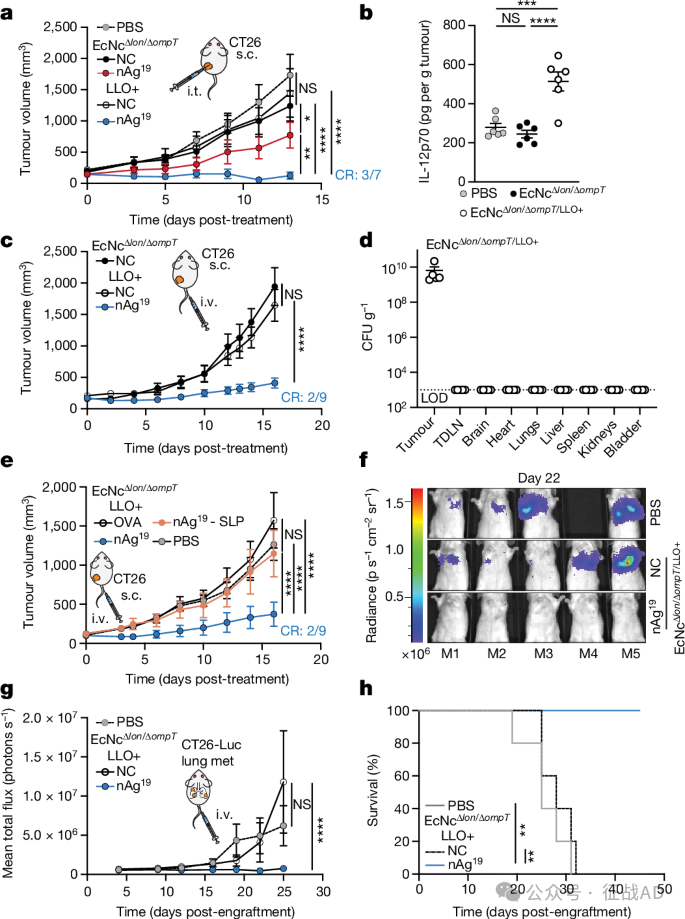
图2. 微生物肿瘤新抗原疫苗在原发性和转移性结直肠癌中的疗效
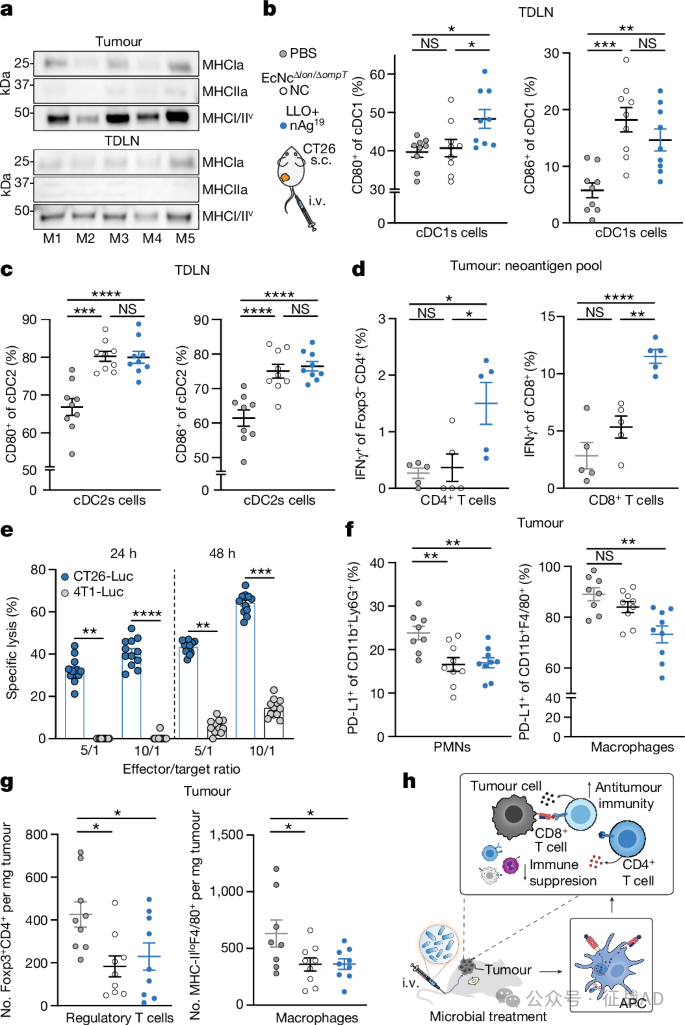
图3. 微生物肿瘤新抗原疫苗重塑肿瘤免疫微环境
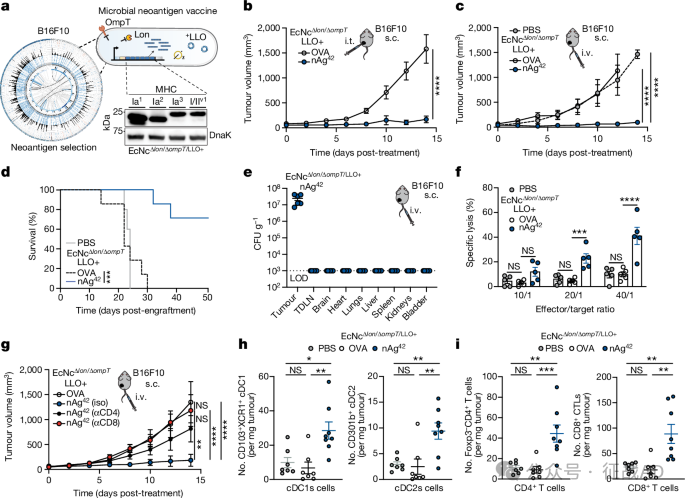
图4. 微生物抗肿瘤疫苗在黑色素瘤治疗中的疗效
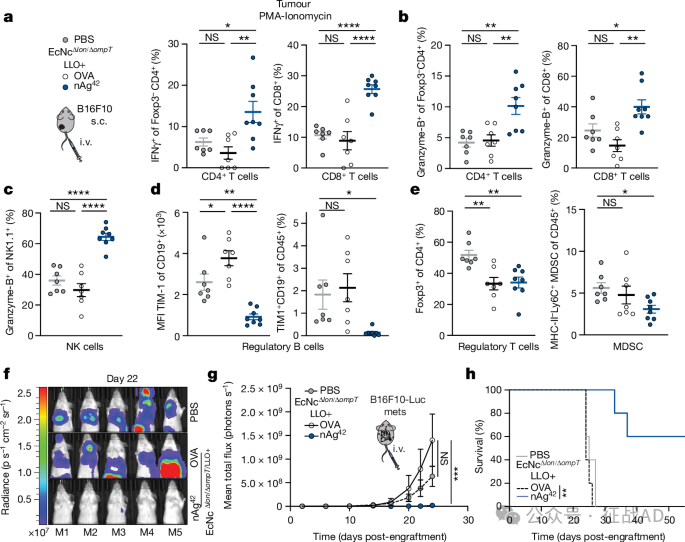
图5.微生物新抗原载体重塑肿瘤免疫微环境并抑制已建立的黑色素瘤转移
编者按:
临床意义和科研启示:
本研究提供了一种创新的癌症免疫疗法策略,通过工程化益生菌传递肿瘤特异性新抗原,激活患者自身的免疫系统来识别和攻击癌细胞。
这种方法具有精准靶向肿瘤、减少对正常组织的损害以及可能避免传统化疗和放疗副作用的潜力。
科研方面,
该研究展示了合成生物学在癌症治疗中的应用前景,强调了通过微生物系统工程化来开发新型疫苗和治疗方法的可能性。
此外,它还提示了未来研究的方向,包括优化新抗原的选择和递送、探索与其他免疫疗法的联合使用,以及在临床试验中验证这种疗法的安全性和有效性。
原文链接:
【1】Sellars, M. C., Wu, C. J. & Fritsch, E. F. Cancer vaccines: building a bridge over troubled waters. Cell 185, 2770–2788 (2022).
【2】https://doi.org/10.1038/s41586-024-08033-4


