中国科学院物理研究所焦放团队《自然∙通讯》:高分辨原子力显微镜揭示细胞死亡调控因子-1(RCD-1)的成孔和诱导细胞膜鼓包机制
时间:2025-02-14 12:11:37 热度:37.1℃ 作者:网络
真菌同种异体识别是一种关键的生物学机制,能够防止细胞质混合、抵御真菌寄生,并通过诱导细胞溶解性死亡维持种群健康和生态平衡。然而,其分子机制尚未完全阐明。前期研究表明,丝状真菌粗糙脉孢菌(Neurospora crassa)中的基因RCD-1在不同菌株中编码两种同源蛋白,即RCD-1-1和RCD-1-2。当不同菌株发生细胞融合时,这两种蛋白介导同种异体识别并触发细胞死亡。尽管RCD-1蛋白与哺乳动物Gasdermin(GSDM)家族的膜打孔结构域具有相似的结构特征,但其均缺乏自抑制功能的结构元件。因此,RCD-1蛋白如何诱导细胞溶解性死亡,是否通过类似于GSDM的膜打孔机制发挥作用,以及其具体分子机制,仍是亟待解决的科学问题。
2025年1月25号,中国科学院物理研究所/北京凝聚态物理国家研究中心焦放团队在Nature Communications杂志上发表了题为“Mechanisms of RCD-1 pore formation and membrane bending”的研究论文,该研究利用原子力显微镜(AFM)分析了RCD-1孔的高分辨结构,揭示了RCD-1-1与RCD-1-2必须形成异质二聚体才能被激活,进而在细胞膜表面形成14.5纳米直径的跨膜孔道结构。此外,发现RCD-1还可在特定条件下诱导细胞膜发生鼓包形变,这一现象在GSDM家族蛋白中尚属首次报道。通过设计一系列不同组分的人工磷脂膜实验,进一步证实RCD-1诱导的细胞膜鼓包现象与膜组分及其弯曲模量密切相关。

RCD-1的异源二聚体及组装形成跨膜孔道结构:通过AlphaFold预测,RCD-1-1和RCD-1-2形成异源二聚体,其β-发夹结构平行排列,类似于哺乳动物GSDM的二聚体结构。实验表明,RCD-1-1和RCD-1-2的混合物在脂质膜上形成弧状、缝隙状和环状寡聚体,最终形成稳定的跨膜孔道结构。RCD-1孔道由约10个异源二聚体组成,直径约为14.5纳米。通过高分辨率AFM成像,观察到RCD-1孔道的亚基结构,并确定了环状寡聚体中二聚体的数量。
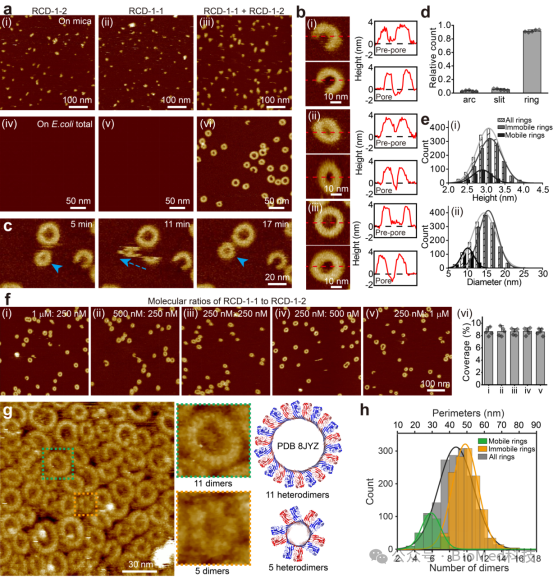
图1 RCD-1-1/RCD-1-2异质二聚体组装形成寡聚体及孔道结构
RCD-1跨膜孔道结构的形成机制:原位原子力显微镜揭示RCD-1孔道的存在两种不同的形成过程。一种RCD-1异质二聚体在细胞膜上吸附并寡聚形成环状孔前体结构,孔前体结构能在细胞膜上面进行移动,最终发生结构转变进行跨膜成孔。另一种RCD-1低聚体在细胞膜表面直接插膜形成弧状寡聚体结构,并进一步组装形成完整的孔道结构。
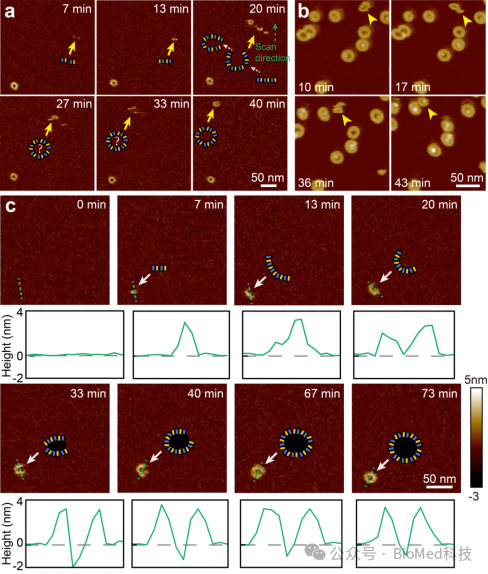
图2 RCD-1孔道形成过程的原位追踪
RCD-1诱导磷脂膜发生鼓包现象:RCD-1不仅形成孔道,还能诱导磷脂膜发生弯曲。实验表明,RCD-1在酸性脂质膜上形成孔道的同时,还会引起膜的局部弯曲,形成球形或不规则的膜形变。这种膜弯曲现象与膜的弯曲模量密切相关,弯曲模量较低的膜更容易发生弯曲。
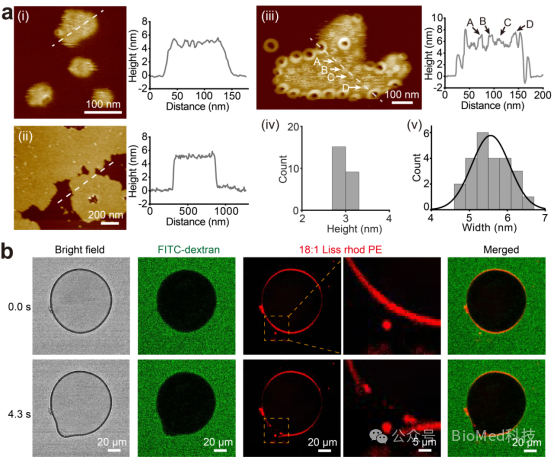
图3 RCD-1诱导磷脂膜发生弯曲形变
RCD-1诱导磷脂膜鼓包的分子机制:通过AFM实时成像,观察到RCD-1寡聚体在膜缺陷处引发膜弯曲,并随着RCD-1吸附浓度的增加,膜弯曲程度加剧。膜弯曲的最终形态取决于RCD-1的密度和膜的弯曲模量。

图4 RCD-1诱导磷脂膜发生弯曲形变的原位追踪
综上所述,该研究揭示了RCD-1蛋白的双重功能—膜打孔与膜弯曲调控,为理解真菌同种异体识别及细胞死亡机制提供了新的视角。中国科学院物理研究所博士后任克礼为第一作者,焦放为通讯作者,合作团队还包括中国科学院生物物理研究所丁璟珒研究员、中国科学院物理研究所叶方富研究员等。研究得到了国家自然科学基金委和中国科学院的大力支持。
焦放团队致力于开发和应用新型多功能高速原子力显微镜(HS-AFM, 水平分辨率~1 nm,垂直分辨率~0.1 nm,成像速度达20帧/秒)技术,研究生物大分子(如MACPF/CDC成孔蛋白、焦亡蛋白、多肽、骨架蛋白及光合蛋白复合物等)在准生理环境中的高分辨结构、动态行为、自组装及相互作用机制。团队常年招硕博连读生(或博士生)、联培学生及博士后,热忱欢迎感兴趣的同学联系 (http://www.iop.cas.cn/rcjy/tpyjy/?id=4432)!
原文链接:
https://www.nature.com/articles/s41467-025-56398-5


