Basic Res Cardiol 大连医科大学附属第一医院张波教授团队揭示Evolocumab保护心肌缺血/再灌注损伤的新机制
时间:2025-02-27 12:25:36 热度:37.1℃ 作者:网络
冠状动脉狭窄引起的急性心肌梗死(AMI)是世界范围内死亡的主要因素,影响人们生活质量和寿命。及时经皮冠状动脉介入治疗(PCI)是改善心肌梗死患者心肌缺血和生存率不可或缺的治疗策略,然而恢复血流引起的缺血/再灌注(I/R)损伤通常会加剧缺血性心肌损伤。因此,寻找缓解I/R损伤的策略仍是临床的迫切需要。
前蛋白转化酶枯草溶菌素9 (PCSK9)主要由肝脏产生,能够与低密度脂蛋白受体结合,竞争性抑制肝脏降解低密度脂蛋白。既往研究表明,PCSK9与动脉粥样硬化、缺血性心脏病、动脉瘤、房颤及心衰等疾病发生发展有关。然而,在I/R进程中,除了影响胆固醇的代谢,PCSK9还参与调节多种细胞死亡信号、免疫反应、炎症反应及心肌损伤的修复,这使其成为一个重要研究靶点。心脏I/R损伤过程中的病理生理机制较复杂,但最核心的事件之一仍然是心肌细胞死亡。铜死亡作为一种新型的程序性细胞死亡方式已在肿瘤细胞中得到验证,但PCSK9与铜死亡的相关性及其在心肌I/R损伤中的作用及分子机制尚不清楚。
2025年2月11日,大连医科大学附属第一医院张波教授、林秋月教授、李子卓博士和郭雷博士团队在Basic Research in Cardiology上在线发表了题为“Evolocumab attenuates myocardial ischemia/reperfusion injury by blocking PCSK9/LIAS-mediated cuproptosis of cardiomyocytes”的研究论文,揭示了Evolocumab通过阻断PCSK9/LIAS介导的心肌细胞铜死亡保护心肌缺血/再灌注损伤的新机制。

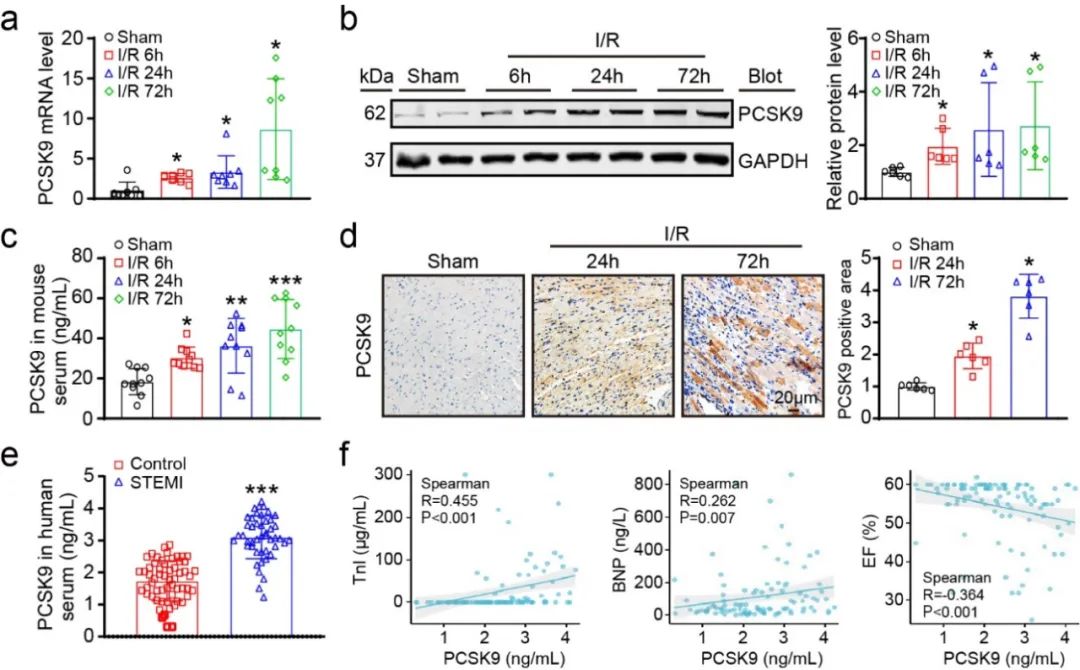
为了明确PCSK9是否与心脏I/R损伤有关,作者首先应用构建心肌I/R模型,在术后6、24和72h检测了小鼠心脏PCSK9表达水平,发现PCSK9时间依赖性地上调。同时检测I/R小鼠与心肌梗死患者血清PCSK9水平,发现PCSK9表达显著上调。多元logistic回归显示,PCSK9与心肌梗死呈正相关。Spearman相关检验显示,PCSK9与肌钙蛋白I和BNP呈显著正相关,且与LVEF呈显著负相关。
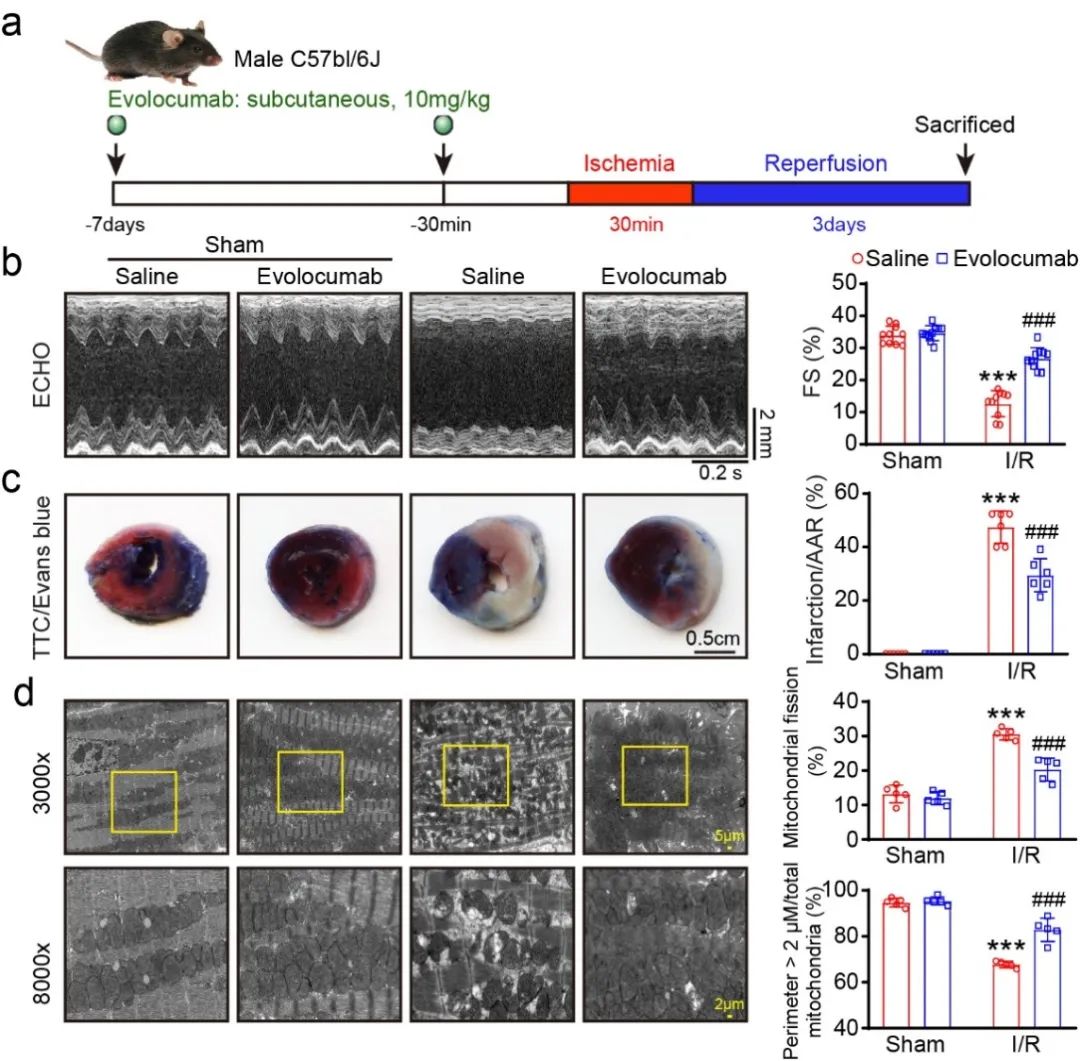
为进一步探究PCSK9在缺血再灌注中的作用,作者在I/R术前7天及半小时对小鼠皮下注射evolocumab (PCSK9单抗),剂量为10 mg/kg。结果显示,与对照组相比,阻断PCSK9可以缓解I/R导致的心功能障碍,改善心肌梗死面积、缓解炎症反应和氧化应激、改善I/R诱导的线粒体裂变和融合动力学失衡。
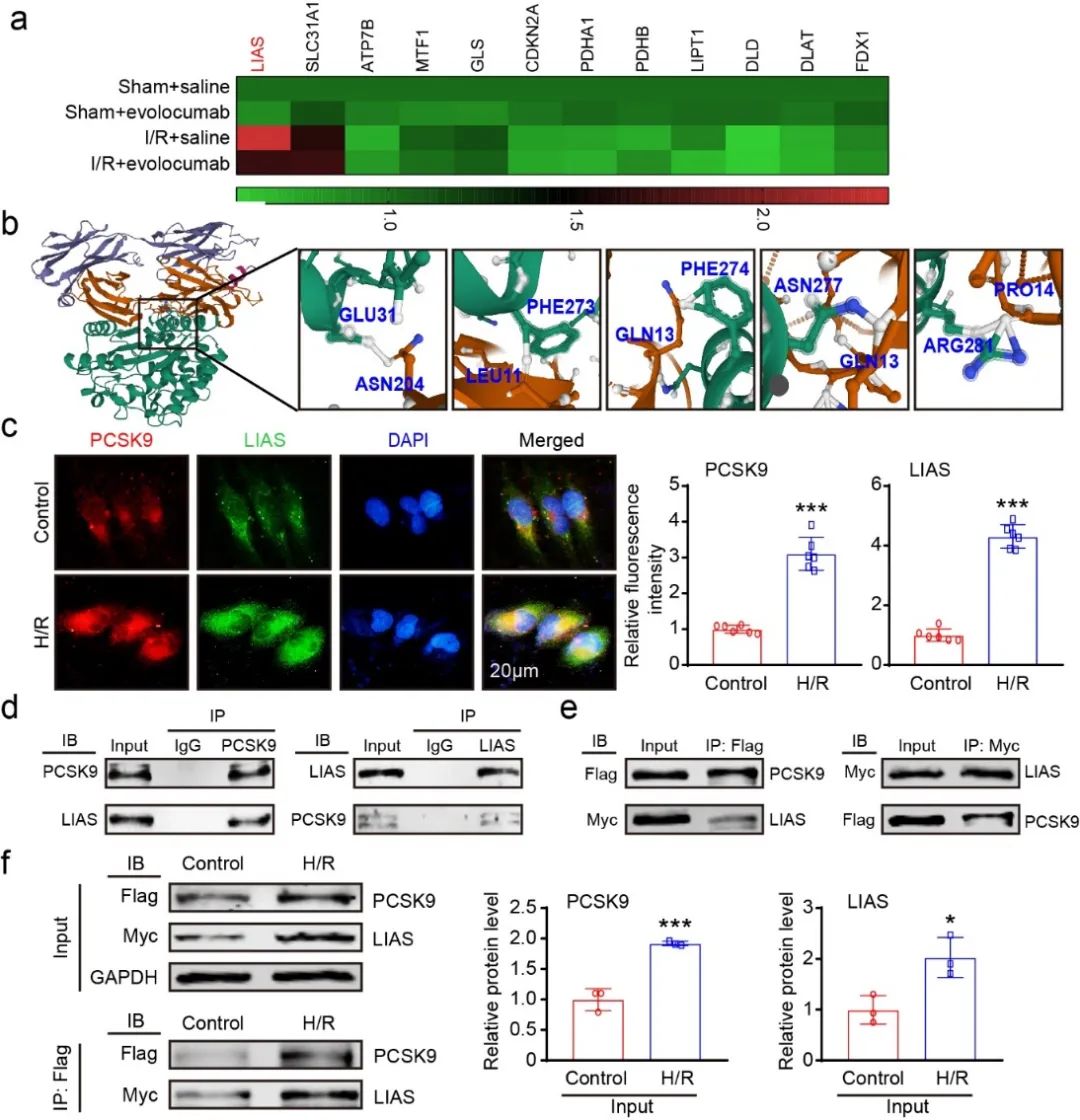
已有研究表明,心肌细胞中的铜过载会加重I/R损伤,而抑制铜死亡信号通路有潜在的治疗作用。为了进一步探索evolocumab在I/R中的作用机制,作者研究了evolocumab是否可以减轻I/R刺激的心肌细胞铜死亡。首先,作者检测了铜死亡相关的关键基因mRNA水平,qPCR分析鉴定出4个I/R后差异表达的基因,包括上调的LIAS和SLC31A1基因和下调的DLAT和DLD基因,而其他基因在统计学上没有显著变化。值得注意的是,心脏I/R损伤后,在12个铜死亡关键基因中只有LIAS被evolocumab治疗逆转。为探索具体机制,作者首先运用分子对接预测PCSK9与LIAS之间的结合模式,结果表明PCSK9与LIAS表现出强而持久的结合亲和力(-23.6 kcal/mol)。免疫荧光染色进一步分析PCSK9和LIAS能否在心肌细胞中共定位,结果显示,这两种蛋白在H/R后均上调,并共定位于细胞质。随后进行了免疫共沉淀(Co-IP),以确认内源性PCSK9与LIAS相互作用,结果显示PCSK9与LIAS均存在于免疫复合物中,并且分别与LIAS和PCSK9抗体共沉淀,Co-IP检测还发现,在H/R期间免疫复合物的结合增强。
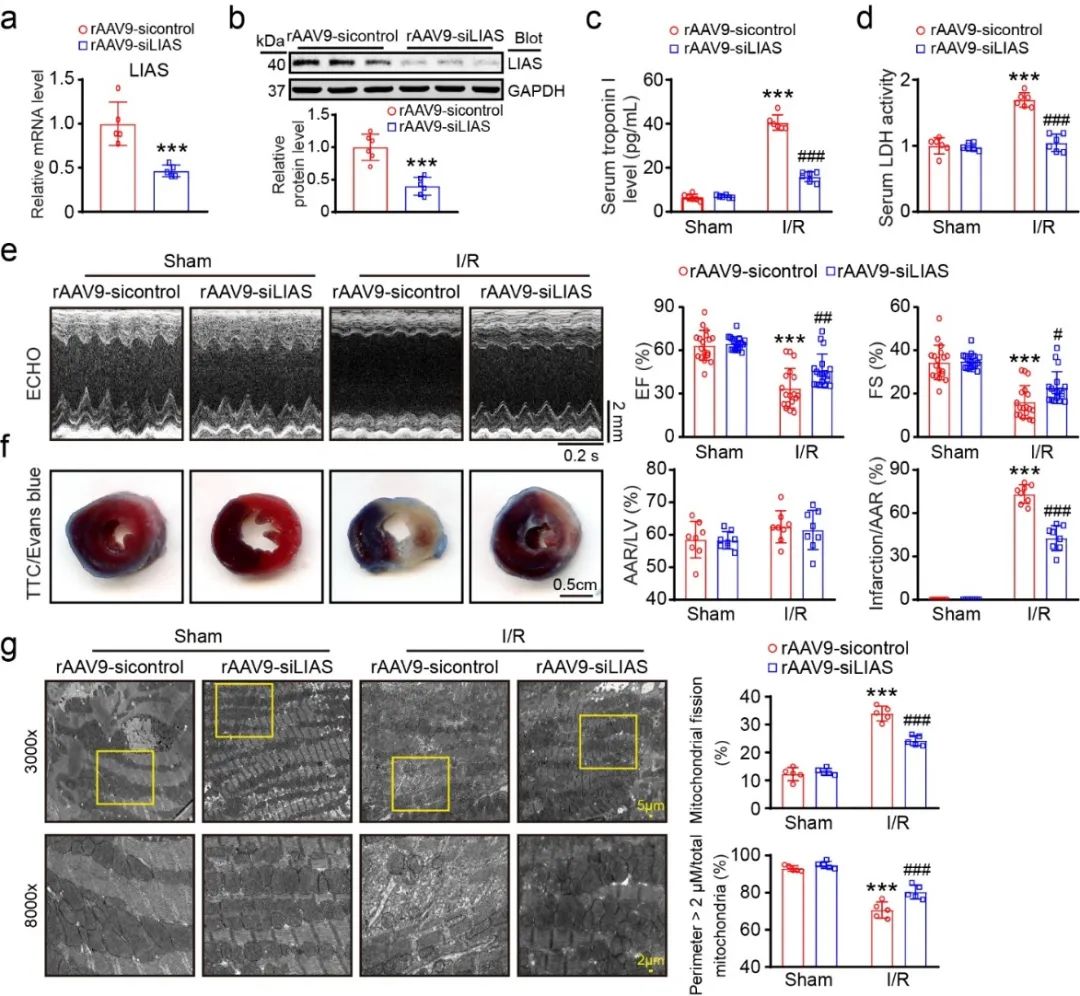
为了进一步证实LIAS促进心脏损伤的潜在机制,作者选择腺相关病毒rAAV9-siLIAS进行心肌特异性敲低LIAS。尾静脉注射rAAV9-siLIAS与rAAV9-sicontrol 3周后,小鼠进行I/R手术。结果显示,与对照组相比,LIAS敲低显著减轻了心功能障碍。TTC/Evans blue染色显示,LIAS敲低显著减小梗死面积。LIAS敲低明显抑制IL-1β、IL-6、NOX1和NOX4水平,改善炎症反应与氧化应激。透射电子显微镜显示,与rAAV9-siLIAS组相比,I/R显著增加了裂变的线粒体的比例,而敲低LIAS阻断了此效应。
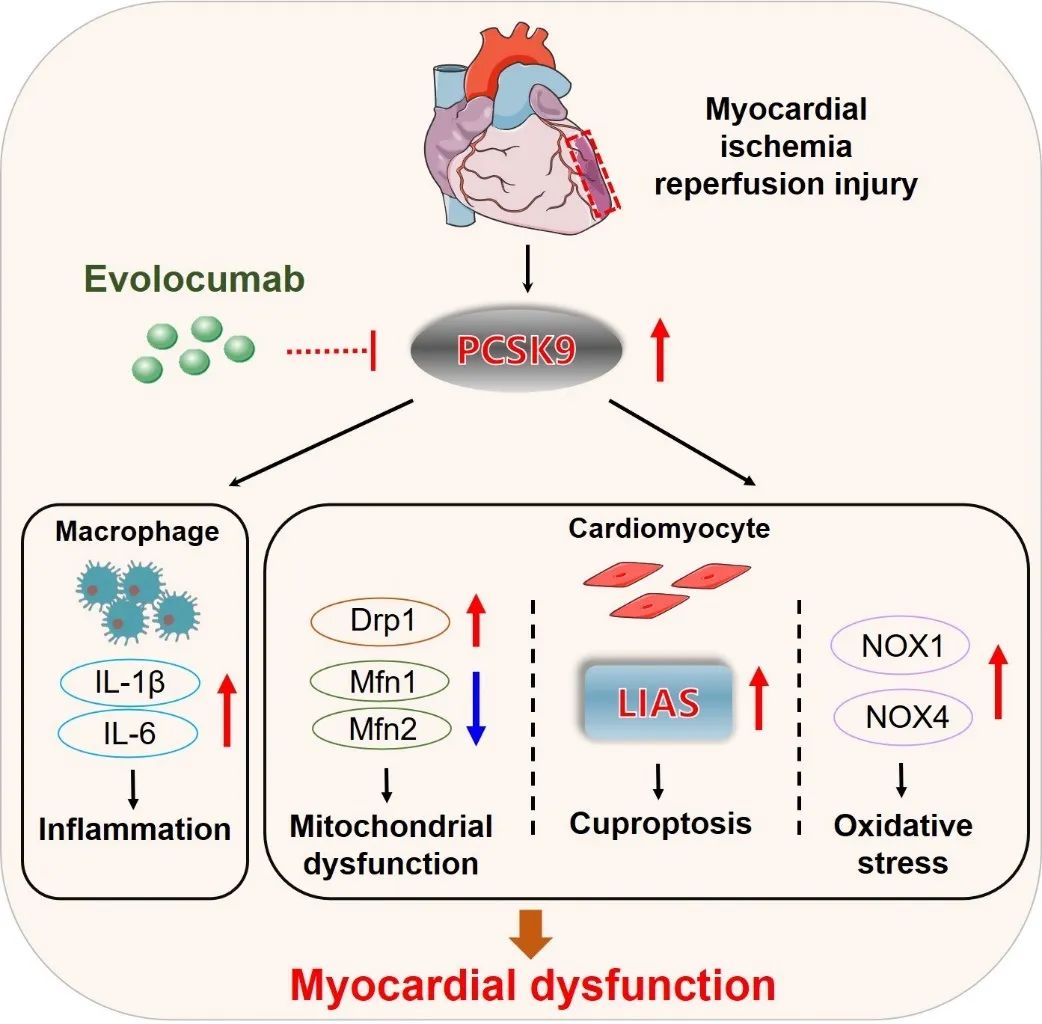
综上所述,抑制PCSK9可减轻I/R诱导的心脏损伤、炎症、氧化应激和线粒体功能障碍。此外,PCSK9可直接与LIAS结合,导致心肌细胞铜死亡通路的激活。当前研究首次揭示了evolocumab通过直接下调LIAS表达来减轻心肌缺血/再灌注损伤导致的心肌细胞铜死亡的新机制。本研究突出了铜死亡在I/R发病机制中的作用,为evolocumab预防缺血/再灌注损伤,保护心脏重构提供了新的证据,并提出了一种治疗缺血性心肌病和心力衰竭的新方法。
大连医科大学附属第一医院张波教授和林秋月教授为本文的共同通讯作者,大连医科大学附属第一医院李子卓博士和郭雷博士为本文的共同第一作者。该项研究获得辽宁省重点研发项目、辽宁省教育厅项目和大连市优秀青年科技人才项目的资助。
原文链接:
https://link.springer.com/article/10.1007/s00395-025-01100-5


