重塑诊断模式,推动药物研发,全基因组测序和转录组测序助力罕见病诊疗
时间:2025-02-28 12:31:58 热度:37.1℃ 作者:网络
一名7岁罕见病患者,症状为进行性肌无力,肌酸激酶增高,既往各种遗传检测均显示阴性结果。通过全基因组测序(WGS)和转录组测序(RNA-seq)分析,在该患者肌病相关基因和常染色体隐性遗传基因中发现了127个非编码区变异,其中86个变异可以进行剪接识别。此外,在患者的LMNA基因内含子区域发现一个新发26bp深度缺失,导致6号内含子滞留。LMNA基因与多种肌病相关,这些疾病与该患者的表型一致[1]。
这只是测序技术帮助罕见病患者实现精准诊疗的众多案例中的一个。
罕见病由于发病率极低,且临床表现复杂多样,通常诊断困难。传统的临床诊断方法不仅耗时费力,且准确性较低。测序技术作为精准医学的核心支柱,为罕见病的精准诊疗带来了革命性改变,使人们对罕见病分子机制的认知达到了前所未有的深度。基于WGS、RNA-seq等测序技术,研究人员不仅可以提高罕见病的诊断效率和准确性,还能鉴别疾病亚型,指导个性化治疗和预后评估,并推动药物研发进展。
罕见病诊断中的测序策略
上述案例中使用了WGS和RNA-seq,是罕见病诊疗中常用的测序策略,此外还包括全外显子测序(WES)、靶向测序、单细胞测序等。不同测序策略的靶标区域、类型和适用场景各不相同,本文将着重探讨WGS和RNA-seq在罕见病诊疗中的应用。
01 WES:有效诊断罕见病,但仍存在局限性
WES是对编码序列的外显子区域进行测序,是临床中应用较多的罕见病诊断手段,在已知致病基因变异和新致病基因挖掘方面均发挥着重要作用。目前WES的平均罕见病诊断率约在25%-50%[2]。但WES很难检测结构变异(SV)、重复扩增和深度内含子区变异等,导致很多通过其他方法诊断(肌肉活检、代谢检测等)的案例无法得到明确分子诊断。
02 WGS:提高罕见病诊断率,做为一线检测具成本效益
理论上,WGS能够检测基因组的所有潜在变异,包括单核苷酸多态性(SNP)、插入缺失(Indel)和SV。基于目前的回顾性研究分析,WGS的诊断率在19.1%-68.3%之间[3]。一项荟萃分析显示,在罕见病患者的基因检测中,WGS诊断率比WES高1.2倍,WGS发现了更多的新基因,且临床效用高于WES[4]。
2021年10月,BMJ期刊报道了第一次在国民医疗服务体系(NHS)中验证WGS的罕见病诊断有效性的结果[5]。通过对疑似线粒体疾病患者的外周血DNA进行WGS分析(Illumina TruSeq、HiSeq 2500和HiSeq X),31%获得了明确或可能的基因诊断,证实WGS在疑似线粒体病患者中是一种有用的诊断方法。
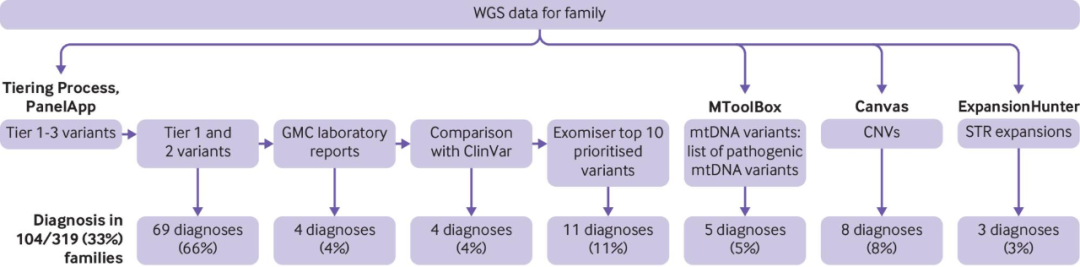
图:NHS研究分析概述和诊断信息。来源:BMJ
英国国家医疗系统13,037名参与者(9802人患有罕见病)的WGS分析(Illumina TruSeq,HiSeq2500)结果显示[6],WGS为1138名广泛表型参与者提供了遗传诊断,并发现了4种新的非编码变异,证实在常规医疗保健中,使用WGS可以简化诊断并发现基因组编码区和非编码区未知的致病变异。
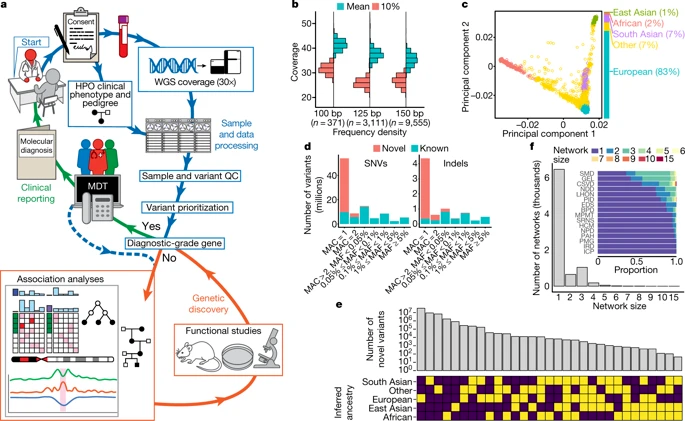
图:英国国家医疗系统研究概述。来源:Nature
在临床中,除了诊断率外,成本效益也是需要考虑的重要因素。WGS、WES与常规标准检测在疑似罕见遗传病儿童中的成本效益评估结果显示,与WES和标准检测相比,将WGS作为一线诊断检测更具成本效益[7]。
03 RNA-seq:WES/WGS的有效补充手段
对于部分无法确诊的患者,RNA-seq可以作为WES/WGS的有效补充手段,快速准确地进行基因表达量的测定,识别未知转录本、SV、可变剪接、基因融合等,从而得到全面的遗传信息,可提高罕见病诊断率和发现新候选基因。RNA-seq在许多肌病及线粒体疾病中已有许多成功应用案例。
例如,在一项将RNA-seq用于罕见病诊断的研究中,利用RNA-seq从遗传学角度诊断罕见肌肉疾病,检测骨骼肌样本RNA,表明RNA-seq能有效鉴别位于外显子区或深内含子区的有害剪接位点变异,总体诊断率可达35%[3]。Yépez, V.A.等利用皮肤成纤维细胞RNA-seq,帮助205例WES未诊断的病例中16%(32例)的患者获得了诊断[2]。
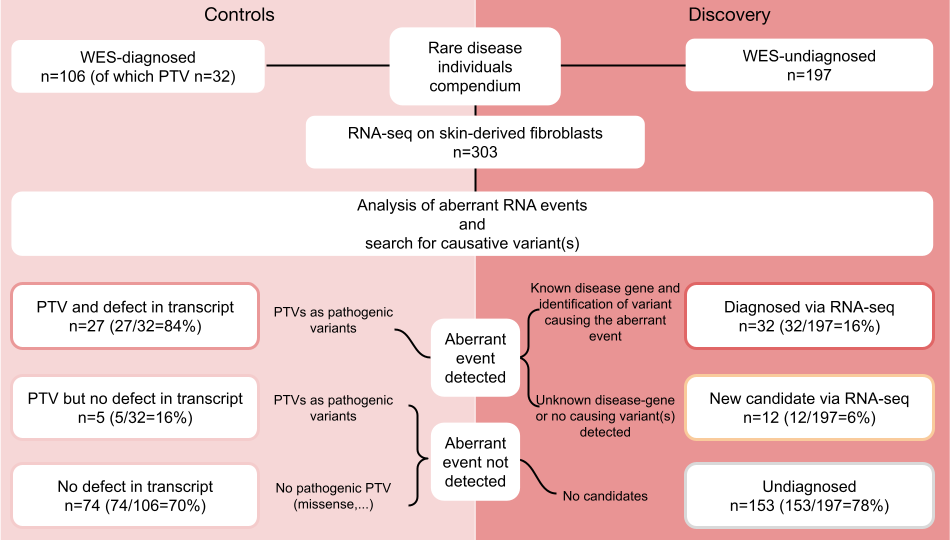
图:RNA-seq在孟德尔遗传病诊断中的临床应用。来源:Genome Med
在临床环境下,部分患者的疾病相关组织(如肌肉活检)和成纤维细胞都较难获得,这限制了组织特异性RNA-seq的应用范围。因此,基于外周血的RNA-seq在样本获取受限的未诊断罕见病患者的遗传诊断中得以广泛探索。
Frésard等评估了血液RNA-seq作为罕见疾病诊断手段的效用[8]。血液RNA-seq在6例未诊断患者(7.5%)中识别并验证了致病基因,提高了16.7%患者候选基因的诊断效力。值得注意的是,对于神经系统相关疾病,虽然血液并不是代表性的组织样本,但RNA-seq仍在5例神经系统异常患者发现了候选基因。此外,基于血液的bulk-RNA-seq能够评估71%的意义不明变异(VUS),对于DNA测序中没有候选VUS的患者或候选VUS不影响剪接的患者,SpliceAI(Illumina)联合RNA-seq还可检测到新的发育障碍相关候选基因[9]。
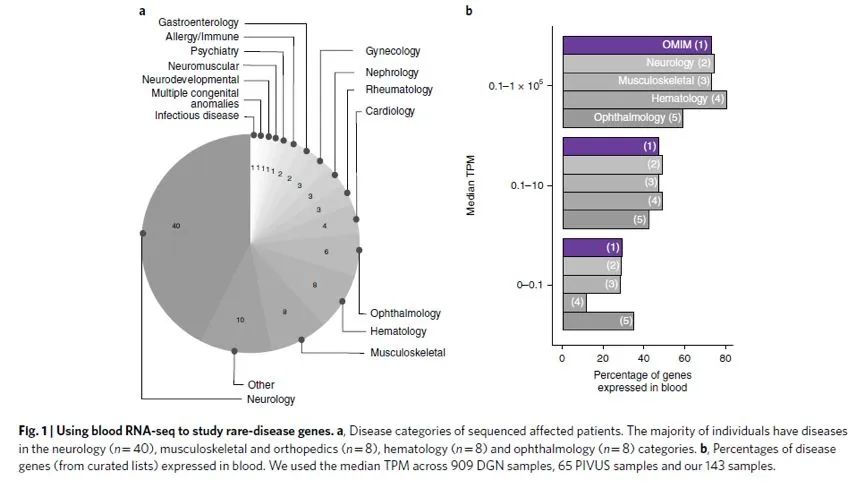
图:利用血液RNA-seq分析罕见病基因。来源:Natrue Medicine
04 WGS+RNA-seq:助力罕见病诊断更上一层楼
在实际临床应用中,需要综合考虑患者的临床表现、家族遗传史、检测成本、时间等因素来选择合适的测序策略。对于疑难复杂的罕见病,可能需要多种测序策略的联合应用。近年来,许多团队在尝试WGS与RNA-seq联合应用,以获得不同程度的分子诊断率提高。
Genetics in Medcine报道了WGS联合RNA-seq的测序策略在罕见孟德尔遗传病诊断中的临床应用[1]。研究显示,WGS联合RNA-seq可以将阳性诊断率从31%提高到38%,同时RNA-seq帮助18%的病例提高了致病性证据等级。
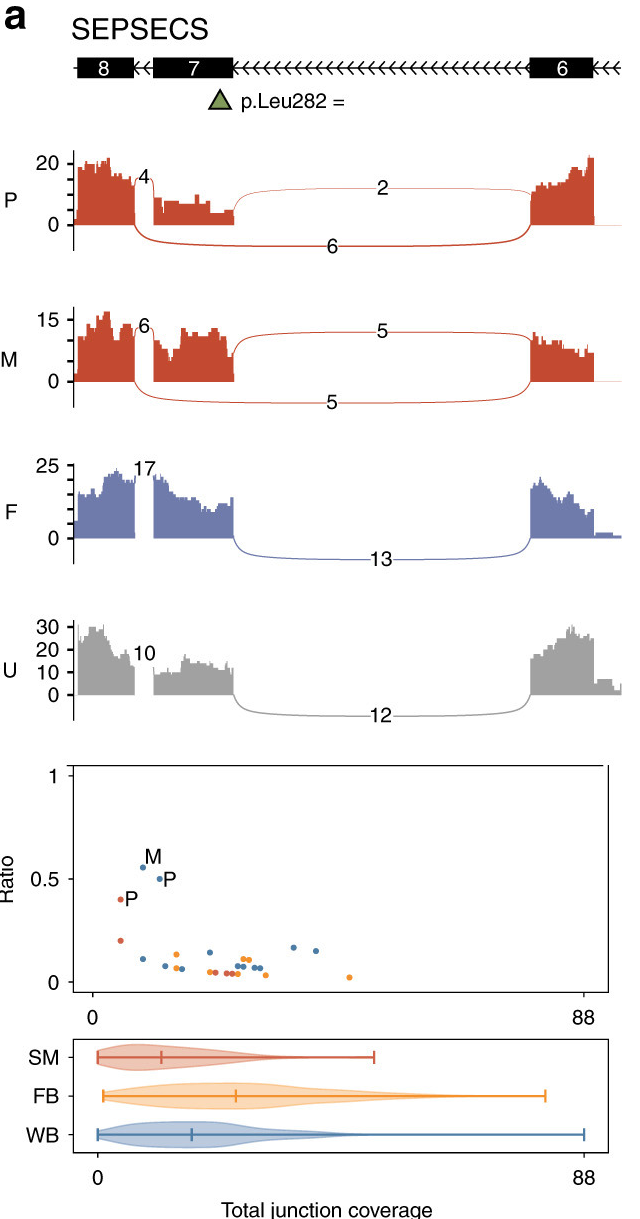
图:WGS联合RNA-seq检测到SEPSECS外显子跳跃。来源:Genetics in Medcine
罕见病治疗及药物开发中的测序应用
2019年,顶级医学期刊NEJM发文报道了罕见病患者Mila Makovec经WGS和RNA-seq成功找到致病基因突变[10]。研究团队基于该突变快速研发靶向药物,使Mila得到了有效治疗。
Mila患有致命性的极罕见Batten病。美国波士顿儿童医院团队利用trio WGS,发现在CLN7基因内,Mila及其母亲同时携带一个特殊的插入序列SVA(SINE - VNTR - Alu)结构,并通过RNA-seq证实SVA结构会干扰正常的基因剪接功能。基于此,研究团队研发了一款针对Mila特定突变的新药“milasen”,并经过了临床试验和FDA的批准。经过一年的milasen治疗,Mila的症状得到明显改善,且没有不良反应发生。
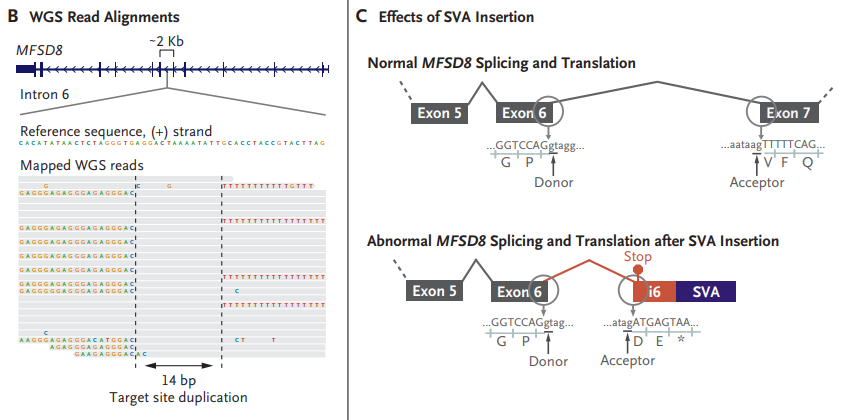
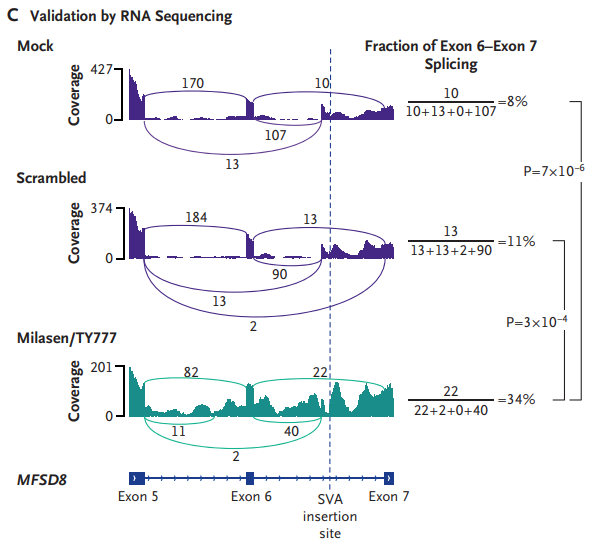
图:Mila的基因诊断,来源:NEJM
在Mila的诊疗案例中,药物研发在WGS和RNA-seq的帮助下加速进行。传统的药物研发过程需要进行大量的试验和筛选,耗时费力,而且成功率较低。测序技术的进步打破了传统药物研发过程中的技术瓶颈,不仅可以快速找到药物靶点,还能筛选适合某种药物治疗的患者亚群,监测药物不良反应,降低成本,提高研发成功率。
总体而言,测序技术主要从以下几个方面促进罕见病药物研发:
01 药物靶点发现与筛选应用:
测序技术可以对罕见病相关基因进行全面分析,帮助研究人员发现新的药物靶点并进行筛选,以及探索药物与基因之间的作用关系,进而开发出更加精准、高效的药物治疗方案。PCSK9抑制剂是展示基因测序促进药物研发的经典案例。2003年,研究人员利用基因测序在家族性高胆固醇血症患者的PCSK9基因中发现了功能获得性突变[11]。12年后,美国FDA年批准了第一个PCSK9抑制剂Evolocumab,用于家族性高胆固醇血症的治疗。
02 临床前研究应用:
传统的罕见病药物临床前评估所需时间和成本过高,测序技术可帮助快速识别生物标记物、阐明药物的作用机制或耐药性,加速体外细胞实验和动物模型实验,验证药物的有效性和安全性。例如利用罕见病患者来源的类器官模型评估个性化反义寡核苷酸(ASO)疗法。在针对两位DMD患者的个性化ASO设计和类器官检测分析中,RNA-seq确认了剪接恢复正常[12]。
03 临床试验应用:
测序技术还可用于优化临床试验设计,提高罕见病药物研发效率和成功率。在测序技术的帮助下,研发人员可以筛选出适合某种治疗方案的患者亚群,并预测可能出现的副作用。此外,测序技术还可以帮助识别患者分层的生物标记物、监测药物反应和疾病进展。在抗体偶联寡核苷酸疗法DYNE-101治疗1型肌强直性营养不良(DM1)的临床试验中,利用RNA-seq发现接受DYNE-101治疗患者的DMPK基因RNA水平显著下降[13]。
展 望
目前,罕见病诊疗仍面临着诸多挑战。随着测序技术的不断发展,相信罕见病的精准诊断能力将进一步提升,相关药物研究也将取得突飞猛进的发展。据不完全统计,仅2024年,全球批准了近200个罕见病药或新适应症[14],中国全年批准罕见病药39个,覆盖34种罕见病[15]。
除本文探讨的WGS和RNA-seq外,其它测序及分析技术对促进罕见病诊疗和药物研发也有巨大的潜力。长读长测序技术可以克服短读长测序在检测复杂SV方面的局限性;多组学分析可将基因组学、转录组学、蛋白质组学、代谢组学等结合,获得更全面的疾病信息。人工智能技术可以帮助提高测序数据的挖掘分析和解读效率,减少漏诊和假阳性。此外,研究机构与企业、医疗机构之间的合作,可通过共享数据和专业知识,使整个研究过程更加协同高效。期望未来能有更多罕见病患者获得有效治疗,改善预后。
参考资料
[1] Hane Lee, PhD, Alden Y. Huang, PhD, Lee-kai Wang, et al. Diagnostic utility of transcriptome sequencing for rare Mendelian diseases. Genetics in Medcine, Volume 22, Issue 3, March 2020, Pages 490-499. https://doi.org/10.1038/s41436-019-0672-1
[2] Yépez, V.A., Gusic, M., Kopajtich, R. et al. Clinical implementation of RNA sequencing for Mendelian disease diagnostics. Genome Med 14, 38 (2022). https://doi.org/10.1186/s13073-022-01019-9
[3] Jaramillo Oquendo, C., Wai, H.A., Rich, W.I. et al. Identification of diagnostic candidates in Mendelian disorders using an RNA sequencing-centric approach. Genome Med, 2024 Sep 9; 16; https://doi.org/10.1186/s13073-024-01381-w
[4] Claudia Ching Yan Chung,Shirley Pik Ying Hue, Nicole Ying Ting Ng, et al. Meta-analysis of the diagnostic and clinical utility of exome and genome sequencing in pediatric and adult patients with rare diseases across diverse populations. Genetics in Medicine, 13 May 2023. https://www.gimjournal.org/article/S1098-3600(23)00909-7/pdf
[5] Katherine R Schon, Wei Wei, Arianna Tucci, et al. Use of whole genome sequencing to determine genetic basis of suspected mitochondrial disorders: cohort study. BMJ 2021; 375 doi: https://doi.org/10.1136/bmj-2021-066288
[6]Turro, E., Astle, W.J., Megy, K. et al. Whole-genome sequencing of patients with rare diseases in a national health system. Nature 583, 96–102 (2020). https://doi.org/10.1038/s41586-020-2434-2
[7] Mario Cesare Nurchis, Francesca Clementina Radio, Luca Salmasi, et al. Cost-Effectiveness of Whole-Genome vs Whole-Exome Sequencing Among Children With Suspected Genetic Disorders. JAMA Netw Open. 2024;7(1):e2353514. doi:10.1001/jamanetworkopen.2023.53514
[8]Frésard, L., Smail, C., Ferraro, N.M. et al. Identification of rare-disease genes using blood transcriptome sequencing and large control cohorts. Nat Med 25, 911–919 (2019). https://doi.org/10.1038/s41591-019-0457-8
[9] Jaramillo Oquendo, C., Wai, H.A., Rich, W.I. et al. Identification of diagnostic candidates in Mendelian disorders using an RNA sequencing-centric approach. Genome Med, 2024 Sep 9; 16; https://doi.org/10.1186/s13073-024-01381-w
[10] Kim J, Hu C, Moufawad El Achkar C, et al. Patient-Customized Oligonucleotide Therapy for a Rare Genetic Disease. N Engl J Med. 2019; 381(17): 1644-1652. doi:10.1056/NEJMoa1813279 https://www.nejm.org/doi/full/10.1056/NEJMoa1813279
[11] Abifadel M, Varret M, Rabes JP, et al. Mutations in PCSK9 cause autosomal dominant hypercholesterolemia. Nat Genet, 2003, 34(2): 154-156.
[12] Means, J.C., Martinez-Bengochea, A.L., Louiselle, D.A. et al. Rapid and scalable personalized ASO screening in patient-derived organoids. Nature (2025). https://doi.org/10.1038/s41586-024-08462-1
[13] https://mp.weixin.qq.com/s/7qLN49y-rOlbADypHKYoPA
[14] https://mp.weixin.qq.com/s/qkNzZYLAWPOIBq_N0d-VqA
[15] https://mp.weixin.qq.com/s/vhnsiVRswEudAJzhKe4ozw


