Immunity:天津医科大学周洁团队揭示了胆汁酸受体FXR在促进新生儿坏死性小肠结肠炎中的重要作用!
时间:2025-03-05 12:08:39 热度:37.1℃ 作者:网络
坏死性小肠结肠炎(NEC)是一种常见的儿科急症,主要影响早产儿,但其机制仍有待充分了解。
2025年2月28日,天津医科大学周洁团队在Immunity在线发表题为“Bile acid receptor FXR promotes intestinal epithelial ferroptosis and subsequent ILC3 dysfunction in neonatal necrotizing enterocolitis”的研究论文,该研究表明胆汁酸受体FXR促进新生儿坏死性小肠结肠炎肠上皮细胞铁死亡和随后的ILC3功能障碍。
该研究发现血浆成纤维细胞生长因子(FGF)19,一种法尼类X受体(FXR)的靶标,与NEC的临床参数呈正相关。NEC患者和NEC小鼠模型在肠上皮细胞(IECs)中显示出丰富的FXR,其在稳态下受到微生物来源的短链脂肪酸(SCFAs)的限制。IECs中FXR基因缺陷导致NEC缓解。在机制上,FXR通过靶向酰基辅酶A合成酶长链家族成员4 (Acsl4)促进IECs的铁死亡。铁死亡IECs释放的脂质过氧化物抑制3型先天淋巴细胞(ILC3s)分泌白细胞介素(IL)-22,从而加重NEC。肠道FXR拮抗剂、ACSL4抑制剂和铁死亡抑制剂可改善小鼠NEC。此外,NEC患者体内脂质过氧化物的升高与FGF19和疾病参数呈正相关。这些观察证明了在NEC治疗中针对肠道FXR和铁死亡的治疗价值。

坏死性小肠结肠炎(NEC)是一种常见的儿科急症,其特点是由过度炎症引起的肠道缺血和坏死的突然发作。荟萃分析报告称,2020年,全球极低出生体重儿(小于1500g)的NEC发病率约为7%。长期以来的总死亡率已超过30%。在需要立即手术切除坏死肠道的病例中,NEC的死亡率可能高达80%。NEC的病因复杂,涉及多种因素,包括遗传易感性。在临床实践中,尽管NEC没有特定的治疗方法,但最初的治疗通常包括停止肠内喂养、提供血液动力学支持和使用广谱抗生素。
不成熟的粘膜免疫、微生物群的生态失调和肠上皮中Toll样受体4 (TLR4)信号的过度激活在NEC的发展中起着重要作用。母乳喂养可以通过调节肠道微生物群和提供抗体来增强新生儿免疫系统,从而提供针对感染和炎症性疾病(如NEC)的保护。微生物群、肠上皮 和粘膜免疫是在出生后阶段建立肠道稳态不可或缺的组成部分。然而,NEC发病机理的确切机制仍未充分了解。
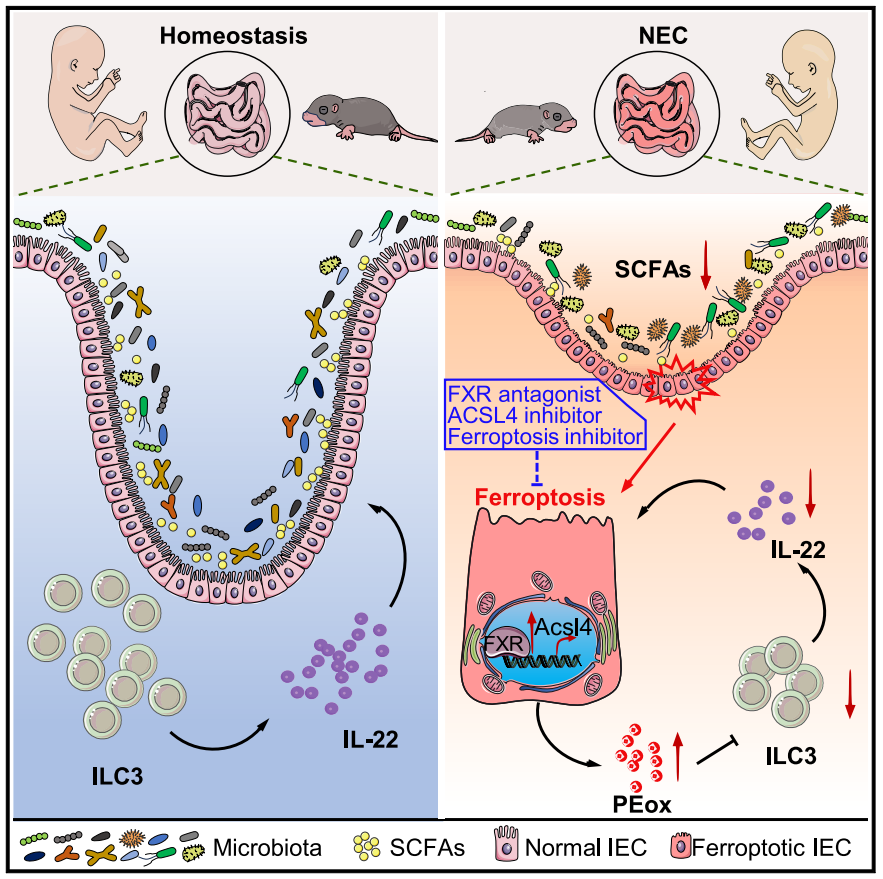
机理模式图(图源自Immunity)
铁死亡是一种铁依赖性程序性细胞死亡的形式,其特征在于脂质过氧化和活性氧(ROS)的积累。研究表明,早产儿的胃肠系统内胰酶分泌不足,导致脂肪消化不完全,随后在远端肠道内氧化和积累脂质。此外, 由于围产期酸中毒、反复缺氧缺血和未发育完全的抗氧化系统,新生儿易于积累非转铁蛋白结合的铁。这种细胞外铁的积累可导致细胞内铁水平升高,进而引发氧化应激和脂质过氧化,最终导致铁死亡的诱发。尽管铁死亡可能与NEC的发展有关,但这种相关性的确切机制仍有待阐明。
在这项研究中,研究人员发现FXR在人类NEC患者和NEC鼠模型的iec中高度表达。来自NEC患者的微生物群诱导IECs中FXR的表达,这可通过补充丁酸盐(一种主要的短链脂肪酸)来逆转。通过对小鼠NEC模型的遗传和药理学干预,证明了FXR促进了肠上皮细胞的铁死亡,抑制了3型先天淋巴细胞(ILC3s)的增殖,并抑制了肠内ILC3s分泌白细胞介素(IL)-22。Acsl4被确定为IECs中FXR的转录靶标。用肠特异性FXR拮抗剂甘氨酸-β-鼠李胆酸(Gly-β-MCA)、ACSL4抑制剂PRGL493和铁死亡抑制剂liproxtatin-1治疗小鼠NEC显示了疗效。在临床环境中,NEC患者表现出脂质过氧化物升高,这与FXR靶成纤维细胞生长因子(FGF)19和疾病参数呈正相关。总之,这些发现阐明了新生儿肠道中微生物群-上皮细胞-ILC3s轴的复杂相互作用,突出了针对肠道FXR和铁死亡治疗NEC的潜在治疗价值。
参考消息:
https://www.cell.com/immunity/fulltext/S1074-7613(25)00070-6


