陈敏山教授:HCC辅助治疗的未来,路在何方?
时间:2025-03-07 12:08:34 热度:37.1℃ 作者:网络
前言
手术切除仍然是肝细胞癌(HCC)最广泛使用的根治性治疗方法,但术后复发率可高达50%-70%。从2015年的STORM试验到最近的IMbrave050研究,众多研究对HCC的辅助治疗进行了探索。然而,这些研究中只有少数取得了阳性结果。
随着肿瘤学免疫治疗时代的到来,研究人员对基于免疫治疗的HCC辅助疗法寄予厚望。IMbrave050研究作为首个探索抗血管生成联合免疫治疗用于HCC辅助治疗的全球试验,提供了目前最具说服力的证据。在IMbrave050研究中,手术切除或局部消融术后高复发风险的HCC患者被随机分配接受阿替利珠单抗联合贝伐珠单抗治疗或主动监测。
遗憾的是,在最近更新的分析中,阿替利珠单抗联合贝伐珠单抗初始所带来的无复发生存期(RFS)获益并未持续,辅助治疗组和主动监测组的中位RFS分别为33.2个月和36.0个月[风险比(HR)0.90 (95% CI, 0.72–1.12)]。这一结果打破了此前人们对该方案作为辅助治疗方式的乐观预期。

近日,发表于Journal of Clinical Oncology的一篇述评文章,探讨了过去十年辅助治疗研究阴性结果的潜在原因、启示,以及对HCC辅助治疗的展望。
HCC的复发模式
肿瘤学研究和指南都强调了辅助治疗的重要性,然而,HCC的复发模式与其他癌症明显不同。HCC患者可能在治疗后2年内出现早期复发(真正的肿瘤复发,源于已存在的肿瘤播散),或在2年后出现晚期复发(新发癌症,源于切除或消融2年后的肝硬化结节)。
在IMbrave050研究的RFS Kaplan-Meier曲线中,两条曲线在随机分组后3个月即出现早期分离,在9个月时达到最大差异,之后开始缓慢接近,并最终在2年左右重叠。这表明,尽管12个月的辅助治疗延迟了部分患者的复发,但最终并未减少总体复发数量。
此外,两组患者的复发部位没有差异,肝内和肝外复发的比例相似,并且两组中均有超过三分之一的患者在肿瘤复发后接受了二次根治性治疗(再次切除或再次消融)。
上述现象提示,阿替利珠单抗联合贝伐珠单抗对改变早期复发和新发复发的生物学特性作用不大。此外,一个更关键的问题出现了:预防早期复发和晚期复发哪个更重要?预防早期复发的措施是否会增加晚期复发的风险?目前尚难得出明确答案。
高危的定义
肿瘤直径、数量、血管侵犯和分化程度都是公认的复发危险因素。然而,东西方学术界对HCC可切除的定义有所不同——西方指南倾向于采用更严格的切除标准,而中国和日本等东方国家则采取相对更积极的方法。正是由于对可切除的定义不同,导致HCC辅助治疗研究的纳入标准存在差异(表1)。
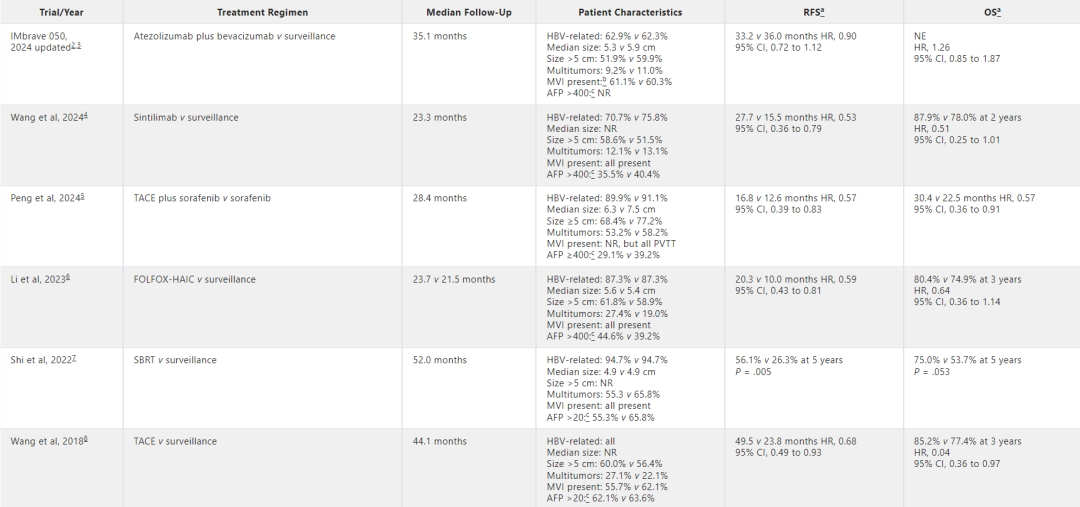
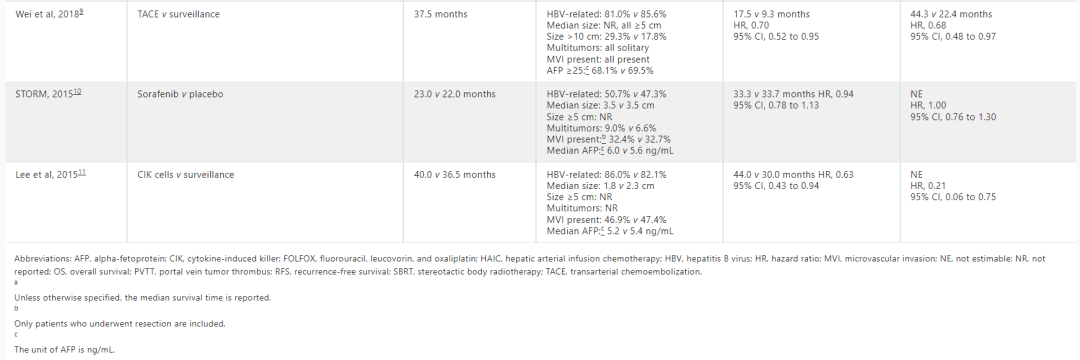
表1 近十年HCC辅助治疗的随机对照试验
总体而言,与STORM研究相比,IMbrave050研究纳入的患者复发风险更高,肿瘤体积更大、数量更多,微血管侵犯(MVI)比例更高,甚至有些患者还存在大血管侵犯。然而,不同因素对复发的影响程度不同,目前尚不清楚哪个因素起决定性作用。
此外,也不确定是肿瘤相关因素(如肿瘤数量、大小和分化程度)还是肝脏相关因素(如肝硬化和肝脏免疫微环境)在导致肿瘤复发中起着更主导的作用。因此,精准筛选辅助治疗的获益人群仍是亟待解决的难题。
亚组分析显示,阿替利珠单抗联合贝伐珠单抗辅助治疗对超出“up-to-7标准”的患者显示出RFS获益趋势,这表明肿瘤体积更大、病灶更多的患者可能是未来辅助治疗研究的合适对象。
从STORM研究到IMbrave050研究,术后高复发风险的定义仍局限于临床因素,许多患者仍未从辅助治疗中获益。新兴的分子水平风险标志物(如循环肿瘤DNA、微小残留病灶)可能为患者分层提供更精准的依据,应纳入未来辅助治疗研究的入组标准。
阿替利珠单抗联合贝伐珠单抗的疗效
抗血管生成治疗(特别是抑制血管内皮生长因子信号通路),通过血管正常化和修剪发挥治疗作用。然而,在肿瘤生长的早期阶段,由于促血管生成因子和血管抑制剂水平较低,肿瘤血管生成仍然有限,导致肿瘤内血管化程度较低。对于肝切除术后真正复发的微转移灶,其生长主要依赖异常肿瘤血管还是周围组织扩散来获取营养尚不明确。临床前研究也证实,长期使用抗血管生成药物会阻碍血管正常化。此外,贝伐珠单抗在肺癌、结直肠癌和乳腺癌的辅助治疗中并未显示出生存获益,提示其疗效可能依赖于原位肿瘤的存在。
对于阿替利珠单抗,手术切除大大降低了肿瘤负荷,从而减少了循环肿瘤抗原。在没有足够抗原刺激的情况下,细胞毒性CD8+T细胞无法完全激活,并且肿瘤切除后免疫抑制微环境也会随之减弱。
研究表明,与原发性HCC相比,早期复发的HCC具有固有样CD8+T细胞,其抗原呈递受损,由PD-L1或CTLA-4信号驱动。另有研究显示,真正复发的HCC表现出由GDF15/CD44轴介导的记忆样功能失调CD8+ T细胞,而新发复发的HCC则含有通过传统的PD-L1/PD-1轴与髓细胞相互作用的细胞毒性耗竭CD8+T细胞,这表明免疫治疗对新发复发的HCC可能更有效。
在此背景下,抗血管生成联合免疫治疗是否适合作为辅助治疗,以及术后的最佳用药时机和剂量,可能是决定阿替利珠单抗联合贝伐珠单抗在HCC辅助治疗中价值的关键因素。
鉴于其在辅助治疗中显示出有限的生存获益,人们不禁思考:是否有其他替代治疗方案能够超越IMbrave050研究的结果。答案无疑是令人沮丧的,因为我们可能无法在短期内开发出比阿替利珠单抗联合贝伐珠单抗更有效的疗法。
此外,阿替利珠单抗联合贝伐珠单抗作为晚期HCC一线治疗的客观缓解率仅为33.2%,完全缓解率为10.2%。那么,该方案在辅助治疗中对潜在微转移灶的清除率是多少呢?目前缺乏合适的评估方法。若辅助治疗使用一线系统治疗方案后复发,应继续原方案还是改用二线治疗,也需要进一步探索。
安全性和肝功能的保护
与晚期HCC的全身治疗不同,辅助治疗中药物的安全性和耐受性更值得关注。IMbrave050研究中,阿替利珠单抗联合贝伐珠单抗组36.1%的患者发生了3级或4级治疗相关不良事件(TRAEs),13.6%发生了严重TRAEs,其中包括2例5级TRAEs(食管静脉曲张出血和缺血性卒中)。
从总体人群来看,如果辅助治疗能降低28%的复发或死亡风险(首次中期分析结果),36.1%的≥3级TRAEs发生率或许可以接受;如果辅助治疗只是延迟了复发时间,而非降低总体复发率,那么不良事件带来的额外风险就需要谨慎考量。同时,47.6%的患者因不良事件中断了治疗,近18.7%的患者退出了研究,这凸显了联合治疗的耐受性并不理想。
阿替利珠单抗联合贝伐珠单抗引起的TRAEs,尤其是与贝伐珠单抗相关的不良事件,会不会是IMbrave050研究结果呈阴性的一个潜在原因呢?另一项II期辅助治疗研究探索了术后信迪利单抗用于合并MVI的HCC患者。尽管该研究纳入人群复发风险高于IMbrave050(对照组中位RFS为15.5个月vs. 36.0个月),但信迪利单抗辅助治疗显著改善RFS(HR 0.53,P=0.002)。
我们推测,该研究阳性结果可能与治疗方案更保守有关:仅使用免疫单药,并且将治疗时间限制在24周,使得3级或4级TRAEs发生率仅为12.4%,明显低于IMbrave050研究报告的36.1%。
另外,早期和中期HCC的整个治疗过程,从根本上来说,是一场与复发性肿瘤的反复斗争。剩余肝脏的体积和功能不仅影响肿瘤复发的可能性,还决定了疾病的严重程度,并指导治疗策略。这就是为什么对于肝炎病毒相关的HCC患者,根治性切除术后持续进行抗病毒治疗可以降低复发率、延长生存时间,这再次凸显了持续保护肝功能的重要性。因此,如何在有效治疗与保护肝功能之间找到平衡,是临床决策的关键。
关注总生存期(OS)而非RFS
大多数HCC辅助治疗研究表明,RFS的改善可能最终并无法转化为OS的获益(表1)。对于接受根治性切除或消融的HCC患者,主动监测并待复发时及时启动治疗并不会损害OS。相反,这种“等待观察”策略可避免不必要的TRAEs、心理压力及经济负担,事实证明这是可行的。
在精准医学理念日益普及的当代,过度强调辅助治疗似乎与这一理念相悖,因为目前预测复发风险和提供有效治疗的方法仍不完善。在没有明确证据表明哪些高危人群可能从辅助治疗中获益的情况下,我们应避免盲目推荐常规辅助治疗,尤其是要防止对低复发风险患者进行过度治疗。我们可能需要弱化对复发风险和严重程度的主观认知,转而强调对复发病灶的早期发现和及时、有效地治疗,从而实现OS的获益。
展望
总体而言,IMbrave050研究是探索HCC辅助治疗的一项重大进展。尽管研究结果显示,与主动监测相比,阿替利珠单抗联合贝伐珠单抗在生存获益方面没有统计学差异,但该研究至少证实了辅助治疗在延迟复发方面具有价值。要全面了解辅助治疗对HCC的作用,还需要继续进行研究并获取长期数据。
基于目前的证据,我们对HCC辅助治疗的研究提出以下建议:
1)探索更精确的复发高危人群预测模型,识别能够从辅助治疗中获益的患者;
2)弱化辅助治疗在HCC管理中的重要性,转而强调对复发病灶的早期发现和治疗,优先保护肝功能,以实现OS获益;
3)研究新辅助治疗方法,通过减少风险因素来降低术后复发的风险,如减少肿瘤大小和数量,降低MVI的发生率,并以病理完全缓解为目标(作为关键终点)。
4)推动东西方专家合作,统一关键定义(如可切除、可移植、转化治疗和复发高危因素),推动全球临床试验的开展并解决相关问题。
在这些关键挑战得到解决之前,建议谨慎将晚期HCC一线系统治疗方案用于辅助治疗。
参考文献:
Fu Y, Zhang Y, Hu D, et al. Where Is the Future of Adjuvant Therapy for Hepatocellular Carcinoma?[J]. Journal of Clinical Oncology, 2025: JCO-24-02615.


