【衡道丨病例】病理诊断——右下肺浸润性黏液腺癌
时间:2025-03-07 12:13:50 热度:37.1℃ 作者:网络
病史
男性,60岁,无吸烟史,因“体检发现右下肺结节”入院。
辅助检查
胸部CT平扫+3D(图1):
右肺下叶见一约1.2×1.1mm结节,呈分叶状,边缘见毛刺,内见空洞,气管及各叶支气管通畅,纵膈居中,纵膈及双肺门未见肿大淋巴结。
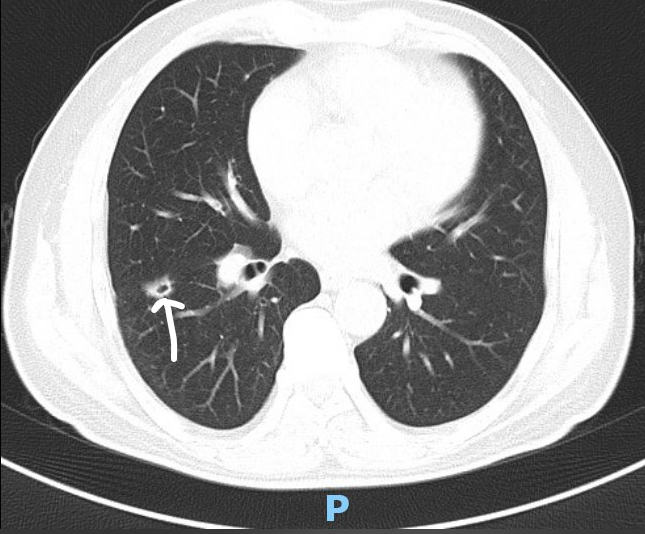
图1 胸部CT:右肺下叶囊实性结节(白色箭头所指)。
组织病理
1、大体肉眼观:
楔形肺组织,大小110×90×20mm,距肺切缘10mm处,距支气管残端20mm处切面见一结节,15×12×6mm,与周围分界欠清,切面灰白、实性、质中。
2、镜下观:(图2-图5)
低倍镜下见肿瘤中央见一囊腔,囊腔边缘肿瘤与周围肺组织界限清,中倍镜下腺管状区域呈腺泡状、花环状结构排列,周围组织细胞反应。高倍镜下腺管状区域肿瘤细胞高柱状、胞质嗜酸,细胞核小位于基底部。
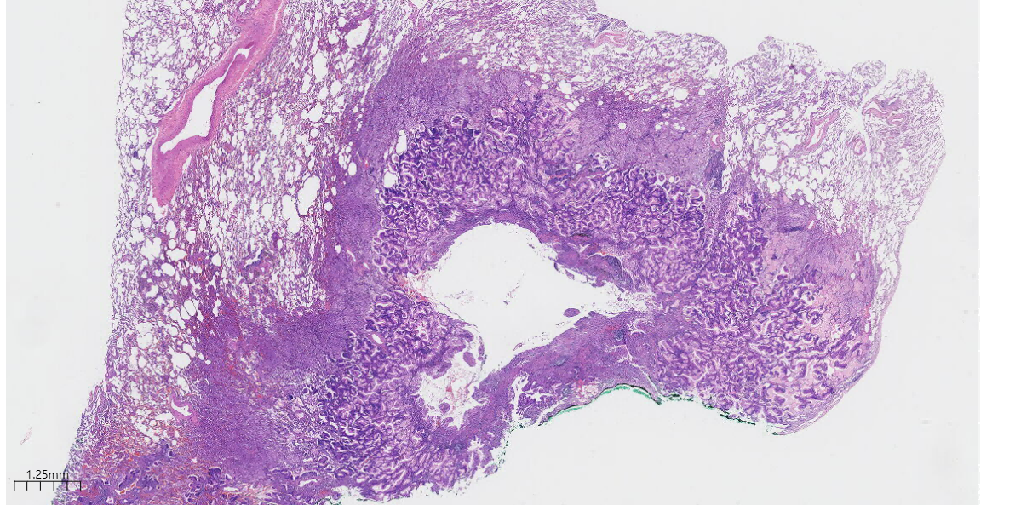
图2 低低倍镜下见肿瘤中央见一囊腔,囊腔边缘肿瘤与周围肺组织界限清。
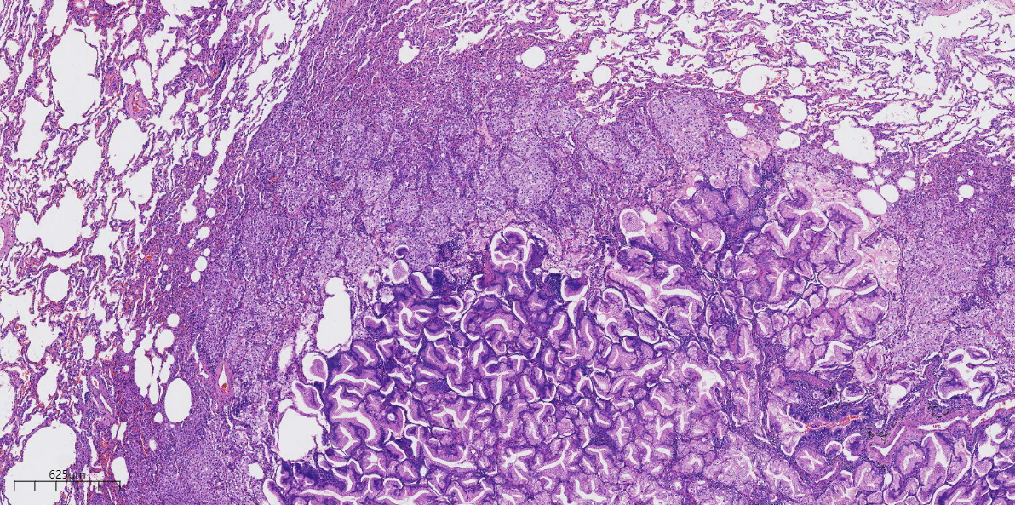
图3 低倍镜下肿瘤细胞呈腺管状排列,周围组织细胞反应。
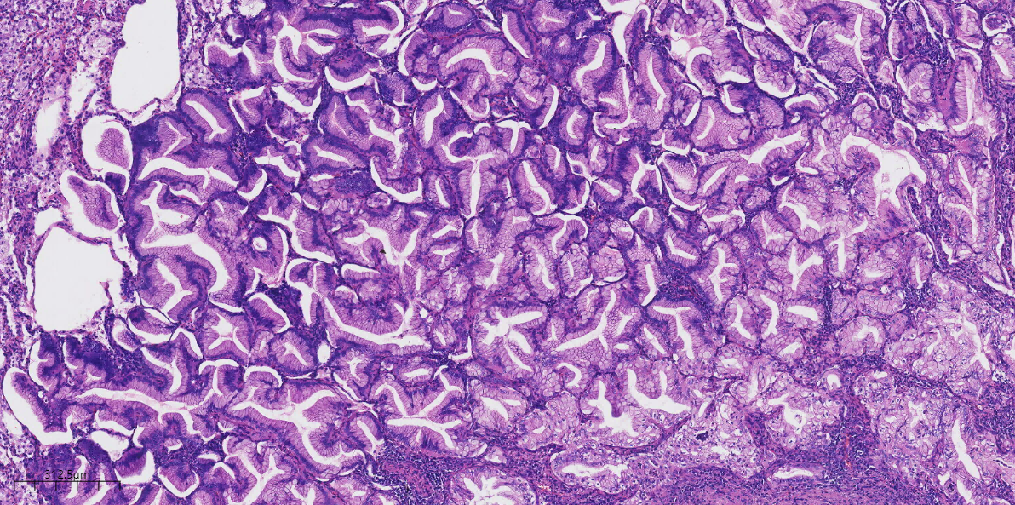
图4 中倍镜下肿瘤细胞呈腺管状、花环状结构排列。
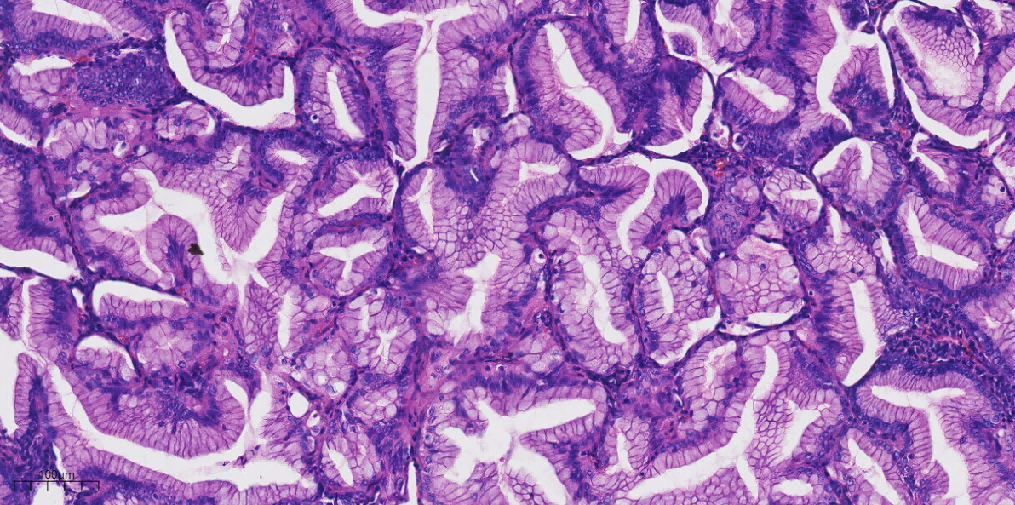
图5 高倍镜下肿瘤细胞形态温和,呈柱状、胞质嗜酸,细胞核小位于基底部。
3、免疫组化:
肿瘤细胞CK20(+)(图6),肿瘤细胞CK7(+)(图7),肿瘤细胞TTF1 (-)(图8),肿瘤细胞Napsin-A(-)(图9),P40 (-),P63示基底细胞缺失, CDX-2(-),Ki-67(约10%+)。
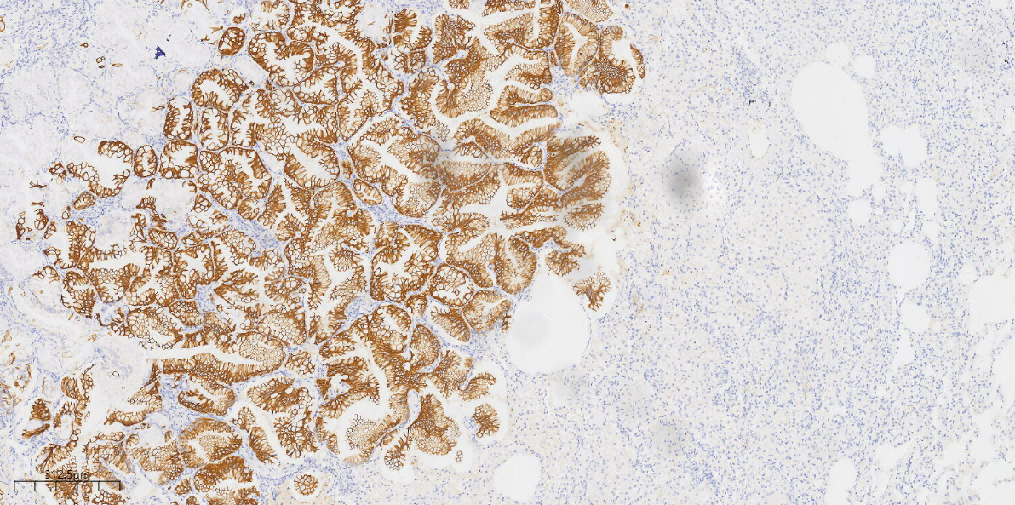
图6 免疫组化示肿瘤细胞CK20(+)。
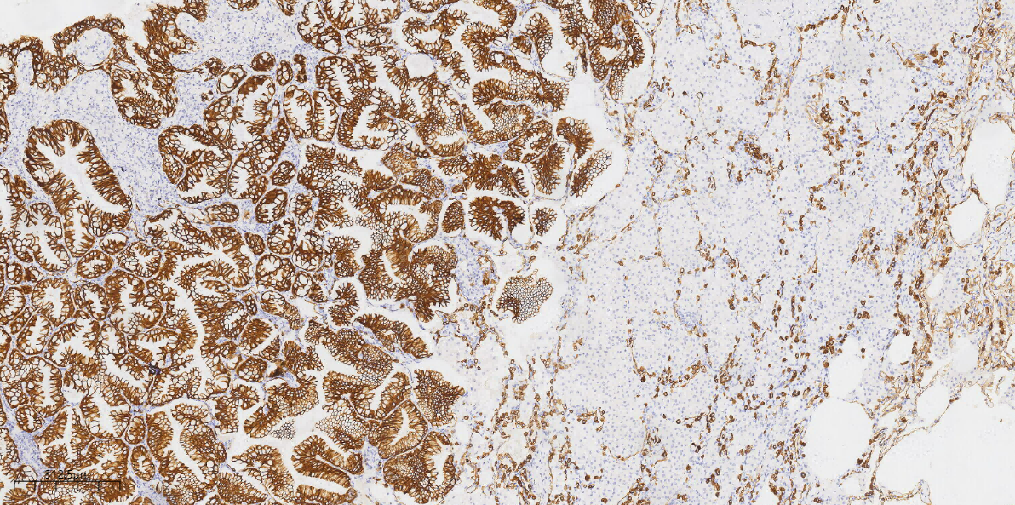
图7 免疫组化示肿瘤细胞CK7(+)。
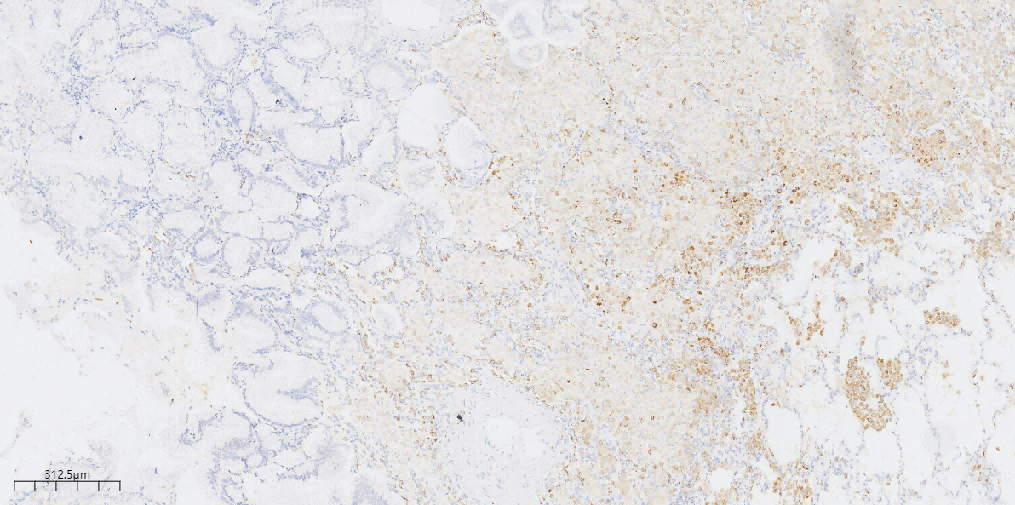
图8 免疫组化示肿瘤细胞TTF1 (-)。
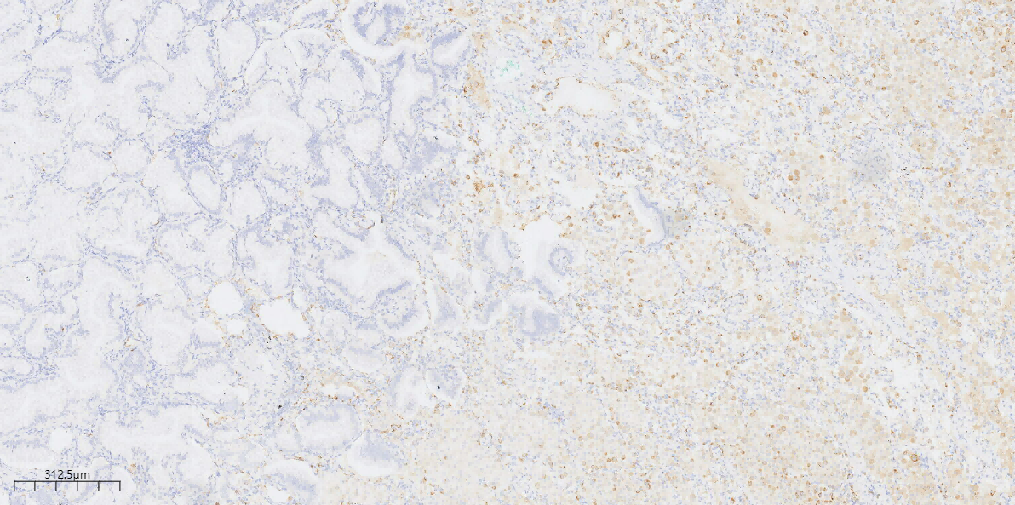
图9 免疫组化示肿瘤细胞Napsin-A(-)。
病理诊断
(右肺下叶)浸润性黏液型腺癌。
分子检测
KRAS G12D突变。
讨论
背景:
肺浸润性黏液腺癌(Invasive mucinous adenocarcinoma ,IMA)是浸润性腺癌的一种亚型,以前称为粘液支气管肺泡癌(BAC)。2011年,国际肺癌研究协会(IASLC)、美国胸科学会(ATS)和欧洲呼吸学会(ERS)更新了肺腺癌的分类,正式命名为IMA。2015年世界卫生组织(WHO)《肺肿瘤分类》中直接采用了“浸润性粘液腺癌”一词,从此在临床实践和研究中被广泛接受和使用。IMA发病率低,约占浸润性腺癌的3-10%。
临床病理特征
1、临床特点
肺黏液腺癌多发生于中老年人,60岁以上多见,男性多发,黏液腺癌患者与与非吸烟或轻度吸烟者相关,容易早期转移,多发生于右肺上叶,外周型多见。无特异临床症状,多表现为咳嗽、咳痰、咳血、呼吸困难、胸痛、体重下降等。手术后常常较早发生淋巴结等器官转移。
2、影像学
影像学特点:肺浸润性黏液腺癌的影像学表现通常为不规则肿块,伴随有腔隙或空洞形成。影像上可见到黏液积聚的区域,肿瘤可能呈多结节性,且肿瘤生长常呈外生性,突破肺组织。典型的胸部CT表现通常包括多中心混浊或实变、磨玻璃混浊和结节,通常位于肺下叶。
3、病理学特征
大体观:
肿瘤常呈结节状,可能为单个或多个结节,切面灰白,中央部分呈现透明或半透明的胶状物质, 边界不清。
镜下观:
肿瘤细胞沿肺泡壁生长,呈杯状细胞或柱状细胞形态,胞浆内黏蛋白丰富。
免疫表型:
肿瘤细胞通常共表达CK7和CK20,不到30%的病例中TTF1和Napsin-A呈阳性,而CDX2几乎总是呈阴性。
分子遗传学:
肺浸润性黏液腺癌常见KRAS突变G12D、G12S、G12V和Q61H,还有报道EGFR外显子19缺失突变、NRG1融合。
鉴别诊断
肺黏液腺癌主要与以下疾病进行鉴别:
1、经典浸润性肺腺癌:
两者都属于原发型肺腺癌,在形态学上相似,均可见腺样、筛状、乳头状结构,均可表达肺泡上皮标志物CK7、TTF-1、NapsinA等。不同之处在于,肺黏液癌镜下表现常为高柱状腺体,黏液丰富,表达CEA(癌胚抗原)、MUC1、MUC5AC。而经典浸润性肺腺癌极少呈高柱状假复层排列, 免疫组化MUC5AC阴性。
2、肺转移性黏液腺癌:
胃肠道、胰腺或卵巢来源的黏液性腺癌转移,需要结合临床和免疫组化标记物鉴别。
治疗及预后
肺浸润性黏液腺癌预后差,治疗以手术切除为主,术后辅助放、化疗、靶向治疗。
参考文献
1、Shen F, Wu X, Geng J, Guo W, Duan J. Prognostic factors for resected invasive mucinous lung adenocarcinoma: a systematic review and meta-analysis. BMC Cancer. 2024 Oct 25;24(1):1317. doi: 10.1186/s12885-024-13068-x. PMID: 39455981; PMCID: PMC11520044.
2、Zhao T, Yi J, Luo D, Liu J, Fan X, Wu Q, Wang W. Prognostic factors for invasive mucinous adenocarcinoma of the lung: systematic review and meta-analysis. World J Surg Oncol. 2024 Feb 2;22(1):41. doi: 10.1186/s12957-024-03326-4. PMID: 38303008; PMCID: PMC10835932.
3、Wakejima R, Inamura K, Ninomiya H, Nagano H, Mun M, Okumura S, Okubo K, Ishikawa Y. Mucinous lung adenocarcinoma, particularly referring to EGFR-mutated mucinous adenocarcinoma. Pathol Int. 2020 Feb;70(2):72-83. doi: 10.1111/pin.12879. Epub 2019 Dec 20. PMID: 31859434.
4、Buettner R. Invasive mucinous adenocarcinoma: genetic insights into a lung cancer entity with distinct clinical behavior and genomic features. Mod Pathol. 2022 Feb;35(2):138-139. doi: 10.1038/s41379-021-00945-0. Epub 2021 Nov 19. PMID: 34795416; PMCID: PMC8786656.


