Nature Medicine:CAR-T疗效“先知”:InflaMix模型精准预测,助力患者选择
时间:2025-04-04 12:09:12 热度:37.1℃ 作者:网络
引言
癌症治疗迎来新曙光,CAR-T疗法曾让无数血液肿瘤患者重获新生。这项通过改造患者自身免疫细胞来精准打击癌细胞的技术,一度被誉为“癌症治疗的未来”。然而,如同所有医学突破一样,CAR-T疗法也面临着挑战。并非所有患者都能幸运地从中获益,治疗失败的阴影依然笼罩着一部分家庭。面对复发或难治性非霍奇金淋巴瘤(NHL),临床医生和患者都迫切需要更精准的预测工具,以便在治疗前就能预判疗效,为患者选择最合适的方案,避免不必要的痛苦和经济负担。
4月1日一项发表在《Nature Medicine》上的重磅研究“An inflammatory biomarker signature of response to CAR-T cell therapy in non-Hodgkin lymphoma”,为我们带来了全新的希望。研究人员创新性地构建了一个名为“InflaMix”(炎症混合模型)的预测模型,它就像一位经验丰富的“预言家”,仅凭患者在CAR-T治疗前的14项关键指标,就能初步洞察治疗的成败。这项研究发现了一个令人震惊的关联:高炎症水平竟然预示着CAR-T疗法近三倍的复发或死亡风险!这究竟是如何实现的?为何治疗前的炎症状态如此重要?这项突破性的发现又将如何改写未来的癌症治疗策略?
更令人振奋的是,这项“InflaMix”模型并非纸上谈兵,它在来自不同医疗中心的多个患者群体中都得到了有效的验证,展现出强大的预测能力。即使在一些临床数据不完整的情况下,这个模型依然能够保持相当的准确性。这意味着,未来的临床医生或许能够借助这个简单易行的工具,更早地识别出那些可能治疗效果不佳的患者,从而为他们提供更个体化、更优化的治疗方案。这项研究的意义远不止于此,它也为我们深入理解CAR-T疗法的作用机制以及肿瘤微环境的复杂性提供了新的视角。

揭秘“InflaMix”:14项关键指标构建炎症预测模型
该研究创新性地提出了一个名为“InflaMix”(INFLAmmation MIXture Model,炎症混合模型)的无监督定量模型。该模型巧妙地整合了患者在接受CAR-T细胞输注前(pre-CAR-T infusion)采集的14项关键实验室指标和细胞因子检测数据,旨在全面、深入地评估患者在治疗前的炎症状态以及终末器官的功能状况。研究团队的初衷是希望能够通过这个精心构建的模型,精准地捕捉到与CAR-T治疗失败风险息息相关的“炎症信号”,从而在治疗前就为患者的预后提供有价值的参考。
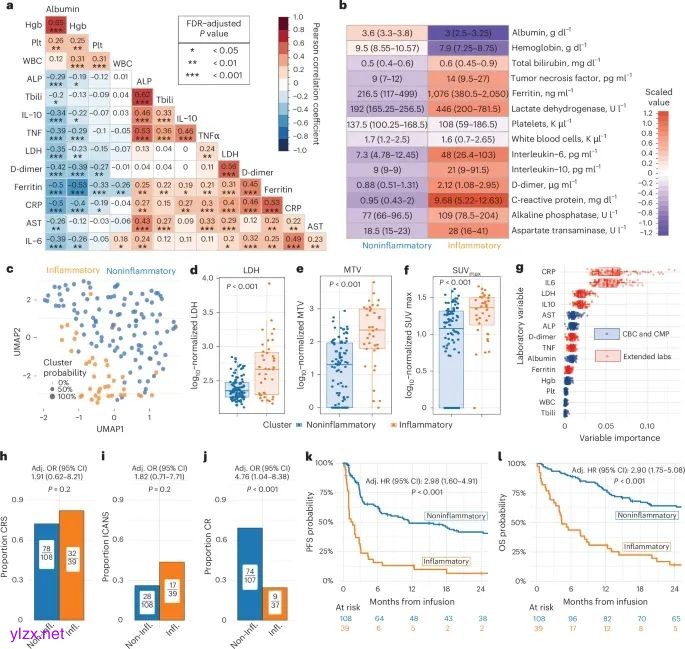
基于14项输注前实验室指标的InflaMix高斯混合模型能够识别出一种与高肿瘤负荷以及不良临床结局(包括较低的CR率、更差的PFS和OS)相关的炎症特征(炎症型聚类)(Credit: Nature Medicine)
相关性分析 (图a): 展示了模型推导队列(n=149)中,经过中心化和标准化处理的14项CAR-T输注前实验室指标和细胞因子之间的皮尔逊相关性。结果显示,一些炎症指标(如CRP、铁蛋白、IL-6、LDH)之间存在正相关,并与白蛋白(albumin)和血红蛋白(Hgb)呈负相关。这表明这些指标在一定程度上提供了冗余但也包含独特的信息。
聚类特征 (图b, c): 图b的热图显示了通过InflaMix模型划分出的两个聚类(炎症型 vs 非炎症型)中,各项实验室指标的中位数水平。炎症型聚类(n=39)的患者表现出更高的炎症标志物(如IL-6、CRP、LDH、铁蛋白、TNFα、D-dimer、AST、ALP)水平和更低的白蛋白、血红蛋白水平。图c使用UMAP降维可视化展示了这两个聚类在低维空间中的分布,显示模型能较好地区分这两组患者。点的不同大小代表了患者被分配到该聚类的概率。
肿瘤负荷关联 (图d-f): 比较了两个聚类之间的肿瘤负荷指标。结果显示,炎症型聚类的患者具有显著更高的LDH水平 (图d)、代谢肿瘤体积 (MTV, 图e) 和最大标准化摄取值 (SUVmax, 图f),表明该炎症特征与更高的肿瘤负荷相关 (P < 0.001)。
特征重要性 (图g): 通过随机森林模型分析了各项实验室指标在预测聚类分配中的重要性。IL-6、CRP、LDH、铁蛋白、D-dimer、AST、ALP等指标对于区分炎症型和非炎症型聚类最为重要。
临床结局关联 (图h-l): 毒性反应 (图h, i): 在调整了年龄、原发难治性疾病、共刺激域和LDH升高等因素后,两个聚类在2-4级细胞因子释放综合征 (CRS, 图h) 和免疫效应细胞相关神经毒性综合征 (ICANS, 图i) 的发生率上没有显著差异 (P = 0.2)。
治疗反应 (图j): 炎症型聚类的患者在第100天达到完全缓解 (CR) 的比例显著更低 (调整后的比值比OR for no CR = 4.76, P < 0.001)。
生存结局 (图k, l): Kaplan-Meier生存曲线显示,炎症型聚类的患者具有显著更差的无进展生存期 (PFS, 图k, 调整后的风险比HR = 2.98, P < 0.001) 和总生存期 (OS, 图l, 调整后的HR = 2.90, P < 0.001)。
炎症风暴前的宁静?治疗前炎症水平如何“剧透”CAR-T疗效
研究团队首先对来自美国纪念斯隆-凯特琳癌症中心(Memorial Sloan Kettering Cancer Center,MSK)的149名接受CAR-T治疗的复发难治性非霍奇金淋巴瘤患者的临床数据进行了细致的分析。通过对这些患者的治疗结果与他们在治疗前的各项实验室检测数据进行深入挖掘,研究人员观察到一个令人警醒的现象:那些在CAR-T治疗前就表现出较高炎症特征的患者,其治疗失败的风险也显著增加。更具体地说,研究结果通过严谨的统计分析揭示,与那些炎症特征较低的患者相比,高炎症特征患者在接受CAR-T治疗后,其疾病进展或死亡的风险竟然惊人地升高了2.98倍(风险比,hazard ratio,HR=2.98;95% CI:1.60-4.91;P<0.001)!这个具有高度统计学意义的结果,如同一个清晰的“预警信号”,强有力地提示我们,在CAR-T治疗的起跑线上,患者体内的炎症水平可能已经悄然地“剧透”了治疗的结局。这就像在暴风雨来临前,空气中往往会弥漫着一种特殊的压抑感,预示着即将到来的剧烈变化。
铁证如山:高炎症特征患者的CAR-T疗法失败风险显著升高
为了进一步增强这项研究发现的可信度和说服力,研究团队并没有满足于在单个中心的数据上得出的结论。他们又积极地联系了其他三个独立的医疗中心,并纳入了来自这些中心的共计688名接受CAR-T治疗的非霍奇金淋巴瘤患者的临床数据进行验证。这些患者来自不同的地域,接受了不同的CAR-T产品和治疗方案,这为评估InflaMix模型的普适性提供了宝贵的机会。令人振奋的是,在这些独立的验证队列中,InflaMix模型依然展现出了卓越的预测能力,能够持续且稳定地识别出那些具有更高疾病复发和死亡风险的患者。这一结果无疑为InflaMix模型的临床应用前景注入了强大的信心。
跨越地域与方案:多中心数据验证InflaMix模型的强大预测能力
更令人惊喜的是,研究团队还发现,InflaMix模型所提供的预后预测信息,甚至能够超越一些目前临床上已经广泛使用的预后标志物,例如肿瘤负荷(tumor burden)。肿瘤负荷通常被认为是影响CAR-T疗效的重要因素,肿瘤体积越大,治疗难度往往也越高。然而,InflaMix模型能够在此基础上提供额外的预测价值,这表明炎症状态可能在CAR-T疗效中扮演着比我们认识到的更为关键的角色。这就像在评估一场足球比赛的胜负时,不仅要看双方球队的实力对比,还要考虑比赛当天的天气、球员的状态等多种因素。InflaMix模型正是这样一种能够提供更全面评估的工具。
超越传统认知:InflaMix模型在预测CAR-T疗效方面展现独特优势
此外,研究人员还充分考虑到了临床实践中数据缺失的常见情况。在真实的医疗环境中,由于各种原因,患者的某些实验室检测结果可能会出现缺失。为了评估InflaMix模型在实际应用中的可行性,研究团队特意进行了一项重要的分析,即在仅使用六项最容易获得的常规实验室指标的情况下,评估模型的预测性能是否会受到显著影响。研究结果令人鼓舞,即使在数据不完全的情况下,InflaMix模型依然能够保持其良好的预测准确性。虽然研究摘要并未明确指出这六项关键指标具体是哪些,但我们可以推测它们很可能是临床上最常用、最容易获得的血液学和生化学指标。这一发现极大地提升了InflaMix模型在临床实践中的应用潜力,因为它意味着即使在一些医疗资源相对有限的地区或机构,医生也可以利用相对简单且易于获得的检测指标,对患者的CAR-T疗法预后进行初步的评估和风险分层。
InflaMix模型如何引领CAR-T疗法走向个体化治疗新时代
综上所述,这项关于InflaMix模型的研究成果,无疑为我们更深入地理解CAR-T疗法在非霍奇金淋巴瘤中的疗效预测打开了一扇新的大门。它不仅清晰地揭示了患者在接受CAR-T治疗前的炎症水平与治疗结果之间存在着密切的关联,更重要的是,它为临床医生提供了一个客观、量化的预测工具,有望在未来的临床实践中发挥至关重要的作用。通过InflaMix模型,医生可以更精准地识别出那些在治疗前就具有较高失败风险的患者,从而能够更加审慎地制定个体化的治疗策略,例如考虑在CAR-T治疗前采取积极的干预措施以降低患者的炎症水平,或者在治疗后实施更加严密的监测和随访,以便及时发现并处理可能出现的复发。
此外,这项研究也为未来的科学研究指明了新的方向,例如,我们可以进一步探索导致患者在CAR-T治疗前出现高炎症状态的具体机制,以及如何通过精准调控患者的免疫系统来更有效地提升CAR-T疗法的疗效。
随着未来更多研究的开展和InflaMix模型的进一步优化和验证,我们终将能够为更多的非霍奇金淋巴瘤患者提供更加精准、更加有效的CAR-T治疗方案,最终战胜癌症,迎接更加美好的明天。
参考文献
Raj, S.S., Fei, T., Fried, S. et al. An inflammatory biomarker signature of response to CAR-T cell therapy in non-Hodgkin lymphoma. Nat Med (2025). https://doi.org/10.1038/s41591-025-03532-x


