NEJM:曲妥珠ADC T-DXd用于HER2过表达的NSCLC的疗效与安全性(DESTINY-Lung01研究)
时间:2021-09-21 16:03:03 热度:37.1℃ 作者:网络
人表皮生长因子受体 2 (HER2) 靶向疗法尚未批准用于非小细胞肺癌 (NSCLC) 患者。曲妥珠单抗 deruxtecan(Trastuzumab Deruxtecan)(T-DXd,DS-8201)是一种新型的抗体偶联物(ADC),由抗HER2的人源抗体和Ⅰ型拓扑异构酶抑制剂组成。
一项多中心、国际、2 期研究,其中将曲妥珠单抗 deruxtecan(每公斤体重 6.4 毫克)用于标准治疗难治的转移性 HER2 突变 NSCLC 患者。主要终点为ICR(独立中央审查委员会)评估的ORR(客观缓解率;CR+PR)。次要结果包括缓解持续时间、无进展生存期、总生存期和安全性。评估了 HER2 改变的生物标志物。
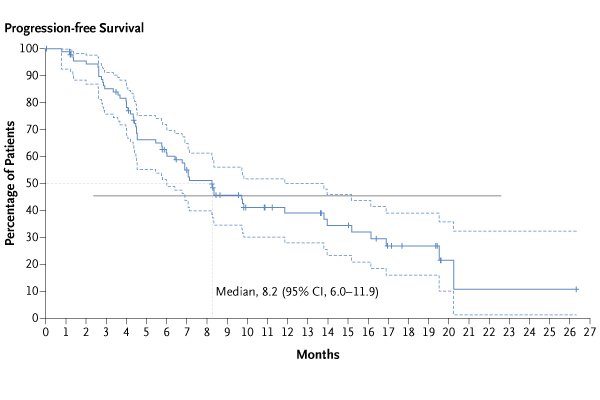
共招募了 91 名患者。中位随访时间为 13.1 个月(范围 0.7 至 29.1)。 55% 的患者出现集中确认的客观反应(95% 置信区间 [CI],44 至 65)。中位缓解持续时间为 9.3 个月(95% CI,5.7 至 14.7)。中位无进展生存期为 8.2 个月(95% CI,6.0 至 11.9),中位总生存期为 17.8 个月(95% CI,13.8 至 22.1)。安全性概况与先前研究的结果基本一致; 46% 的患者发生了 3 级或更高级别的药物相关不良事件,最常见的事件是中性粒细胞减少症(19%)。 26% 的患者发生与药物相关的间质性肺疾病,并导致 2 名患者死亡。在不同的 HER2 突变亚型以及未检测到 HER2 表达或 HER2 扩增的患者中观察到了反应。
HER2过表达队列
在数据截止日期(2020年5月31日),49名HER2过表达NSCLC患者接受了DS-8201(6.4mg/kg)治疗。中位年龄63岁,61.2%男性,34.7%患者入组时有中枢神经系统(CNS)转移。91.8%曾接受过铂类为基础的化疗,73.5%接受过抗PD-(L)1治疗;既往治疗方案的中位数为3种(1-8)。中位治疗时间为18.0周(3.0-57.1),22.4%的患者继续接受治疗。
ICR确认的ORR为24.5%(95% CI: 13.3%-38.9%); 中位DOR为6.0个月(95% CI: 3.2-NE); DCR(疾病控制率)为69.4%(95% CI: 54.6%-81.8%); 中位PFS为5.4个月(95% CI: 2.8-7.0); 所有患者均出现至少一种治疗紧急不良事件(TEAE);最常见的TEAEs是恶心(59.2%)、食欲下降(38.8%)和疲劳(32.7%)。8例患者由IRC判定出现药物相关性间质肺病。HER2激活突变队列
HER2激活突变的NSCLC患者每3周给予DS-8201(6.4mg/kg),截至2019年11月25日,42名患者(64.3%为女性)接受了DS-8201治疗,45.2%有CNS转移,大多数患者(90.5%)之前接受过铂类为基础的化疗,54.8%接受过抗PD-(L)1治疗。既往中位治疗线数为2(1-6),中位治疗时间为7.75个月,5.2%患者继续接受治疗。
ICR证实的ORR为61.9%(95% CI: 45.6%~76.4%); 中位DOR未达到,26名应答者中有16人仍在接受治疗; DCR为90.5%(95% CI: 77.4%-97.3%); 中位PFS为14.0个月(95% CI: 6.4-14.0); 所有患者(42/42)均出现TEAEs,64.3%出现≥3级(52.4%药物相关)AE,包括中性粒细胞计数下降(26.2%)和贫血(16.7%)。5例(11.9%)药物相关间质性肺病(均为2级),1例1级间质性肺病待审核。25例(59.5%)患者因TEAEs导致治疗中断,16例(38.1%)剂量减少,10例(23.8%)停止治疗。DS-8201后线治疗HER2过表达的转移性NSCLC患者,显示了初步的抗肿瘤活性,安全性总体上可接受,但间质肺病可能较为严重。DS-8201治疗HER2突变NSCLC患者表现出良好的临床活性,具有较高的ORR和持久的应答,安全性数据与既往报道基本一致。
HER2基因突变的发生率较低,在晚期非小细胞肺癌中只占2%左右,虽然是驱动基因,但是以前多次研究尝试都没有获得好的结果。近两年,新药不断涌现,其中针对HER2的ADC药物DS-8201得到了很好的客观缓解率,PFS达到14个月,安全性也可以接受。
HER2领域的药物研发关注由之前仅关注HER2突变,逐步扩展到HER2扩增或过表达。DS-8201后线治疗HER2过表达NSCLC的疗效并不显著,ORR为24.5% ,中位PFS为5.4个月,安全性总体上可接受,但间质肺病可能较为严重,需要及时监测和干预。
关于T-DXd(DS-8201)
T-DXd(DS-8201)是新一代靶向HER-2的抗体偶联药物,由人源化抗HER-2抗体trastuzumab通过一种四肽(GGFG)linker偶联拓扑异构酶-Ⅰ抑制剂喜树碱衍生物(DXd)构成。
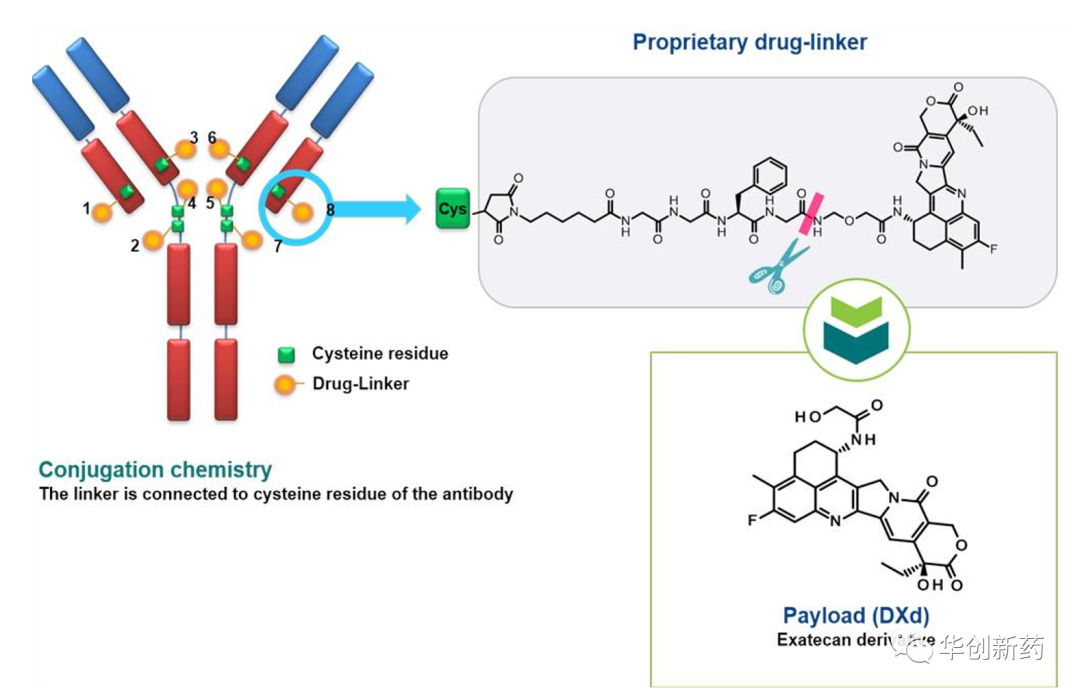
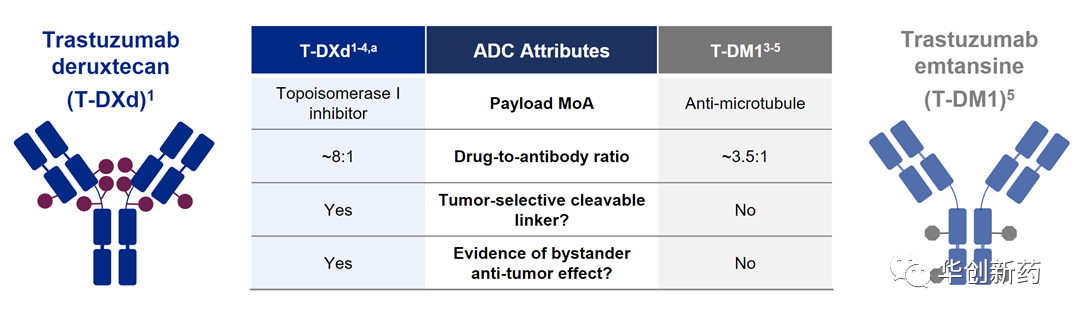
T-DXd具备以下几个优点:
1、更高的载药量:运用独特的疏水性连接子与半胱氨酸残基定点偶联技术,降低了ADC的疏水性,T-DXd每个抗体可以携带7-8个DXd分子。药物与抗体比率(DAR)高于T-DM1的3-4。
2、弹头选择:DXd与微管抑制剂相比,其毒性更强,半衰期更短,毒素在人体内存留的时间更短。
3、linker设计:T-DXd的疏水性四肽linker可以被肿瘤细胞中高表达的溶酶体酶降解从而释放DXd,并可避免药物聚合。
4、DXd具有较高的膜穿透性,释放后的DXd可以穿透至邻近肿瘤细胞,通过“旁观者效应”发挥杀伤作用。
T-DXd在多种实体瘤(乳腺癌、肺癌、胃癌)的临床研究中疗效卓越,有望颠覆HER-2阳性实体瘤诊疗指南。
原始出处:
Li BT, Smit EF, Goto Y, Nakagawa K, Udagawa H, Mazières J, Nagasaka M, Bazhenova L, Saltos AN, Felip E, Pacheco JM, Pérol M, Paz-Ares L, Saxena K, Shiga R, Cheng Y, Acharyya S, Vitazka P, Shahidi J, Planchard D, Jänne PA; DESTINY-Lung01 Trial Investigators.Trastuzumab Deruxtecan in HER2-Mutant Non-Small-Cell Lung Cancer.N Engl J Med. 2021 Sep 18. doi: 10.1056/NEJMoa2112431


