梅斯盘点:2021年度妇瘤领域十大进展
时间:2021-12-31 10:11:52 热度:37.1℃ 作者:网络
合集:2021年度十大进展
卵巢癌成为新的“癌王”,在2021年度,卵巢癌的精准诊断,治疗取得不错的进展。梅斯医学为您盘点2021年度肺癌领域的进展。
1、卵巢癌精准诊断和治疗取得进展
临床中,有10%的女性因附件肿块接受手术治疗,其中仅10%~30%的附件肿块是恶性,如果肿瘤有恶性肿瘤迹象,建议进行分期手术。多元指数分析MIA和MIA2G有助于指导临床决策,开发MIA3G有助于提高诊断特异性,提高临床应用价值。该研究收集了一些临床常用的参数,如CA125、转甲状腺素蛋白、HE4、B2M、FSH、ApoA1、年龄、转铁蛋白、绝经状态。采取MIA3G用于学习和构建诊断模型进行研究。研究结果显示,MIA3G诊断灵敏度比CA125高26.1%,特异性相当
循环肿瘤DNA(ctDNA)在卵巢癌诊断中的应用。卵巢癌通常在诊断时或新辅助化疗后,行腹腔镜探查以评估手术可切除性。目前没有临床或生物标志物可以正确预测肿瘤的可切除性,并且可以避免对最初无法切除的患者进行第二次腹腔镜探查。该研究将循环肿瘤DNA(ctDNA)作为卵巢癌可切除性的非侵入性生物标志物,入组了初诊的卵巢癌,评估需要行新辅助或辅助化疗的患者,手术前后、新辅助化疗前、后和随访中收集外周血和或组织样本,结合术前ctDNA阴性率、新辅助化疗后或术后ctDNA清除率分析ctDNA与完全切除或疾病复发之间的关系。结果显示,92.1%患者基线ctDNA阳性(43/47),基线VAF(突变丰度)与腹膜种植相关。新辅助化疗后ctDNA清除倾向与IDS完全切除相关。
在卵巢癌分子分型的基础上,根据临床用药指导意义分类的生物标志物包括同源重组修复基因(BRCA1/2和HRD)、错配修复基因(dMMR/MSI和TMB)、PI3K/mTOR、NTRK、FGFR信号通路上的基因以及非靶点基因变异(如CCNE1扩增)等。生物标志物的检测进一步指导了PARP抑制剂、免疫检查点抑制剂、靶向治疗药物、手术治疗、化疗、放疗、姑息治疗等治疗方式的选择。
2、PARP抑制剂在卵巢癌一线和维持治疗中获重要进展
近3年来,PARP抑制剂在卵巢癌一线维持治疗公布了多个研究结果:单药维持治疗研究—SOLO-1,PRIMA,PAOLA-1均显示出临床获益。同时,铂敏感复发卵巢癌同样可以受益于PARP抑制剂维持治疗—SOLO-2,Study19,OPINION,NOVA大型国际研究均可见临床获益。
PARP抑制剂在中国人群中的疗效与国际研究一致,2021年最新研究L-MOCA证实,不论BRCA状态如何,奥拉帕利在以中国人为主的亚洲人群中维持治疗有效且耐受性良好。中国NORA研究则发现,对于全人群、gBRCA突变患者和gBRCA野生型患者,与对照组相比,尼拉帕利维持治疗也可降低疾病进展或死亡风险。
OReO/ENGOT Ov-38试验—既往接受过PARP抑制剂的卵巢癌患者再次应用奥拉帕利维持治疗Ⅲb期研究也获得进展。结果显示,在BRCAm队列中观察到奥拉帕利具有统计学意义的无进展生存期(PFS)获益,一部分患者获得了临床相关的长期获益,在6个月的随访中,接受奥拉帕利治疗的患者无进展的数量是安慰剂的两倍多。而在非BRCAm队列中同样观察到奥拉帕利具有统计学意义的PFS获益,除一部分患者获得了临床相关的长期获益外,在6个月的随访中,接受奥拉帕利治疗的患者无进展的数量是安慰剂的四倍。
OReO/ENGOT Ov-38试验表明,在预先接受PARPi治疗的铂敏感复发卵巢癌患者中,与安慰剂相比,再次使用奥拉帕利维持治疗可显著改善PFS,无论BRCAm状态如何;在BRCAm和非BRCAm队列中,一部分患者从再次应用奥拉帕利维持治疗中获得了临床相关的长期获益;在非BRCAm队列中,无论HRD状态如何,治疗效果均出现一致性;且再次应用奥拉帕利的安全性和耐受性与首次使用时观察到的情况一致,该研究为医生在PARP抑制剂后的治疗方案提供了更多的选择。
NORA研究:尼拉帕利用于末次铂类化疗完全或部分缓解的铂敏感复发卵巢癌维持治疗的有效性及安全性
NORA研究共纳入265例患者,133例(50.2%)在末次铂类化疗获得完全缓解(尼拉帕利组86例,安慰剂组47例),131例(49.4%)获得部分缓解(尼拉帕利组90例,安慰剂组41例),另有1例患者化疗后疾病稳定,未纳入本次亚组分析。
与安慰剂组相比,尼拉帕利用于末次铂类化疗后出现完全或部分铂敏感复发卵巢癌的维持治疗,能够显著降低复发风险、延长无进展生存。并且这一生存获益与BRCA胚系突变(gBRCA突变)状态无关。
患者对尼拉帕利的耐受性较好,未出现新的安全问题。患者接受尼拉帕利治疗过程中,因治疗期间不良事件(TEAE)导致的治疗中断的比例很低。
3、帕博利珠单抗联合化疗加或不加贝伐珠单抗用于一线治疗宫颈癌的疗效(KEYNOTE-826)
Ⅲ期KEYNOTE-826研究探索了帕博利珠单抗联合化疗加或不加贝伐珠单抗用于一线治疗宫颈癌的疗效,且不考虑PD-L1表达状态。KEYNOTE-826试验是加速批准帕博利珠单抗治疗宫颈癌的验证性试验,2021年9月18日,新格兰杂志公布了KEYNOTE-826数据,成为第一个宫颈癌PD-1/PD-L1一线治疗获得阳性结果的Ⅲ期试验。
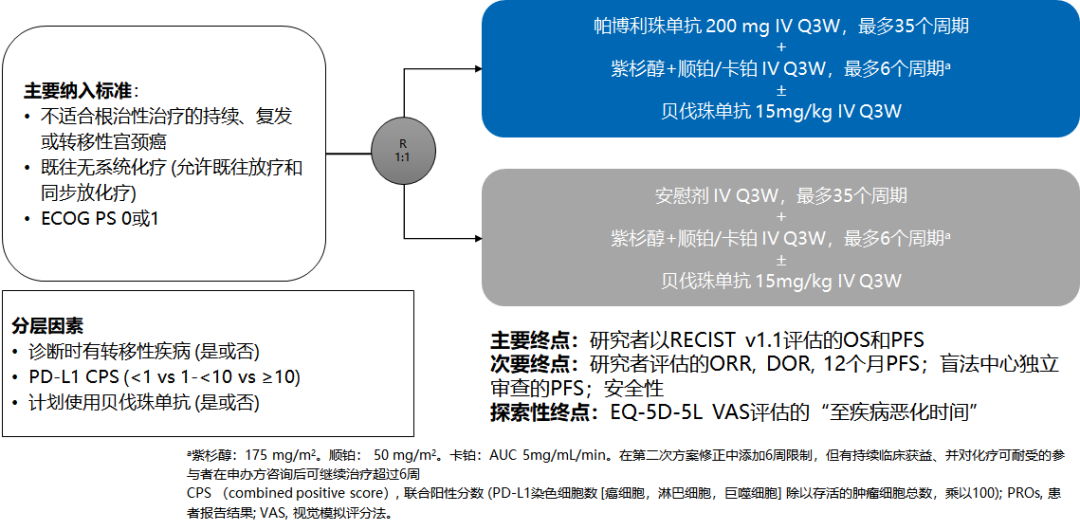
研究结果显示,在化疗±贝伐珠单抗方案中添加帕博利珠单抗具有统计学意义的显著PFS获益(P<0.001),中位PFS均高达10.4个月,不论PD-L1状态。
研究结果显示,在化疗±贝伐珠单抗方案中添加帕博利珠单抗具有统计学意义的显著PFS获益(P<0.001),中位PFS均高达10.4个月,不论PD-L1状态。
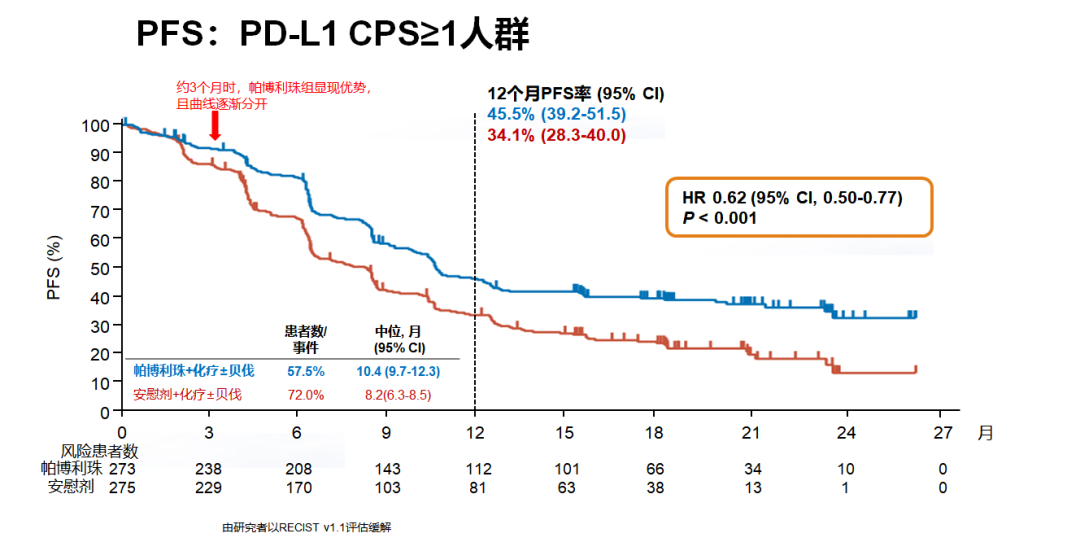
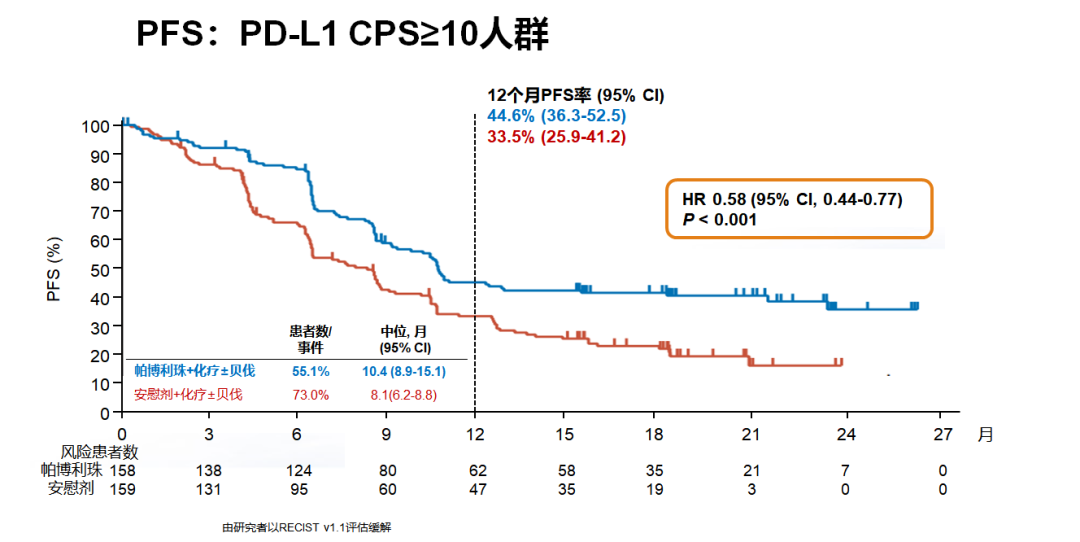
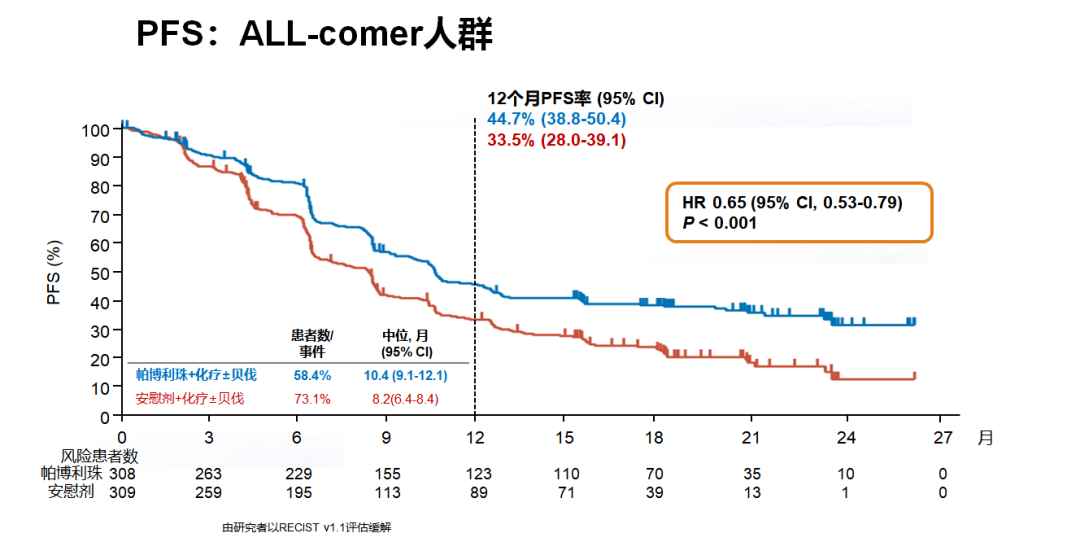
同样,在化疗±贝伐珠单抗方案中添加帕博利珠单抗也可获得显著OS获益(P<0.001),不论PD-L1状态。对于PD-L1 CPS≥1、PD-L1 CPS≥10和All-comer患者,其24个月OS率分别为53.0%、54.4%和50.4%。All-comer患者中位OS为24.4个月,PD-L1 CPS≥1和PD-L1 CPS≥10患者中位OS尚未达到。
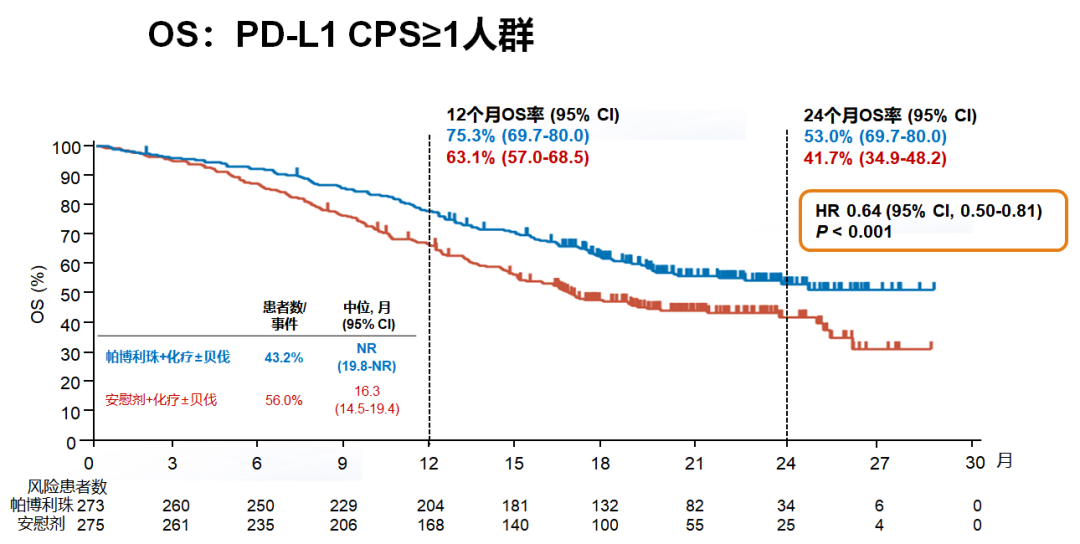
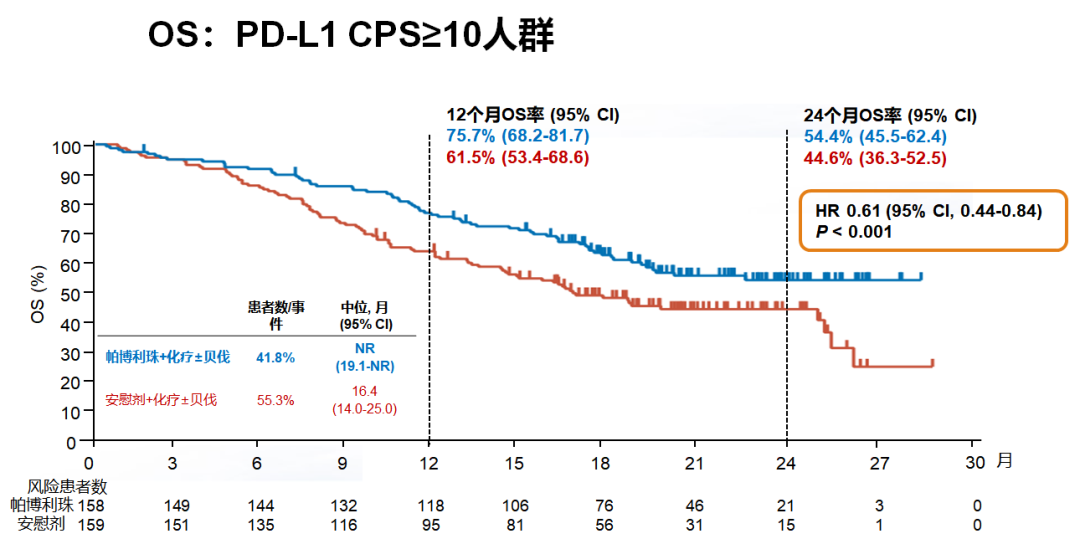
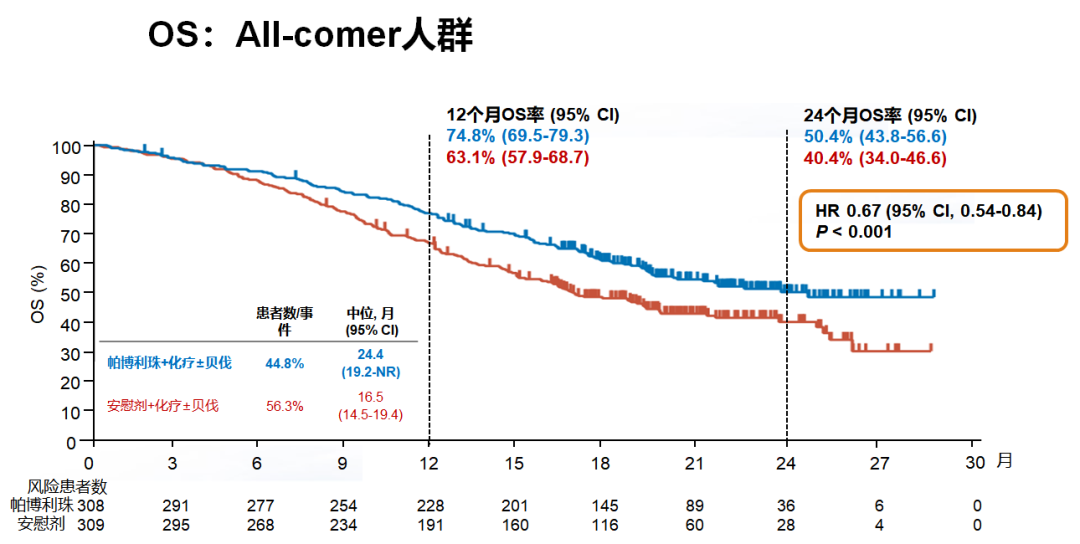
All-comer患者中预设亚组分析显示不同亚组中PFS和OS均有获益。
4、卡瑞利珠单抗联合阿帕替尼治疗妊娠滋养细胞肿瘤(GTN)(CAP 01研究)
由北京协和医院向阳教授牵头的一项卡瑞利珠单抗联合阿帕替尼治疗妊娠滋养细胞肿瘤(GTN)的CAP 01研究于国际顶级学术期刊《柳叶刀·肿瘤学》(The Lancet Oncology)全文发表,为高危耐药/复发GTN带来了国际领先的科研成果。
CAP 01研究共纳入20名至少经过两种及两种以上联合化疗方案失败的高危耐药/复发的高危GTN患者,给予卡瑞利珠单抗(200 mg,每2周一次)联合阿帕替尼(250 mg,每日一次)治疗(俗称“双艾”方案,下同)。
疗效数据显示,“双艾”方案组完全缓解(CR)率达50%,客观缓解率(ORR)为55%;同时,在疾病进展(PD)的患者中,71%的患者后续接受挽救性治疗再次达到CR。
5、氟唑帕利应用于铂敏感复发性卵巢癌维持治疗(FZOCUS-2研究)
我国自主研发的PARP抑制剂氟唑帕利立足中国人群数据,在FZOCUS系列研究中显示出良好的应用前景。FZOCUS-2研究是一项氟唑帕利应用于铂敏感复发性卵巢癌维持治疗的多中心、随机、双盲、安慰剂对照的Ⅲ期临床研究,研究结果显示,在中位PFS数据尚未成熟的情况下,氟唑帕利已显示出明显的疗效,可显著延长患者PFS,降低铂敏感复发人群75%疾病进展/死亡风险(HR=0.25),该研究被2021 SGO年会纳入LBA环节口头汇报。而在今年2月于《临床癌症研究》(Clin Cancer Res)全文发表的FZOCUS-3研究显示,氟唑帕利治疗经接受过2~4次含铂方案治疗的gBRCA1/2突变患者,经IRC评估的ORR仍高达69.9%,中位PFS长达12.0个月。
氟唑帕利的亮眼成绩持续得到国际妇瘤学界的高度关注与认可,基于FZOCUS-3和FZOUUS-2研究的出色结果,氟唑帕利已先后获批卵巢癌后线治疗和铂敏感复发卵巢癌维持治疗适应症,为中国卵巢癌患者提供了高效低毒的治疗新选择。
6、贝伐珠单抗 vs. 阿特珠单抗+贝伐珠单抗联合乙酰水杨酸或安慰剂治疗复发性铂类药物耐药卵巢、输卵管或原发性腹膜腺癌(EORTC-1508研究)
铂耐药卵巢癌(PROC)患者随机接受1、BEV(15 mg/kg q3w);2、ATE(1200 mg q3w)+ 安慰剂(P);3、ATE(1200 mg q3w)+ ASA(320 mg/日);4、BEV(15 mg/kg q3w)+ ATE(1200 mg q3w)+ P;5、BEV(15 mg/kg q3w)+ ATE(1200 mg q3w)+ ASA(320 mg/日)治疗,直至疾病进展或出现不可接受的毒性。组2和组3在III期研究结果表明PD-L1抑制剂单药治疗的疗效不佳后提前关闭。采集强制性活检(治疗前和第3周期前)和连续血样。主要终点为6个月时的无进展生存率(PFS-6)。次要终点包括耐受性、PFS、缓解率(RR)和至首次后续治疗的时间(TFST)。
122例患者接受随机化入组分配:BEV(33);ATE + P(11);ATE + ASA(13);BEV + ATE + P(32);BEV + ATE + ASA(33)。中位年龄63岁(36~82岁);84%≥3种既往治疗。39/52例(75%)接受治疗的患者(第1~3组)在进展时至BEV + ATE交叉。PFS-6率(ITT)分别为22%、9%、23%、25%和25%。中位PFS分别为2.3、2.1(HR 1.78,0.89~3.58)、2.2(HR 0.95,0.49~1.85)、4.1(0.84,0.50~1.38)和4.0个月(0.81,0.49~1.34)。RR:分别为10%、0%、9%、19%和15%。含BEV + ATE组的中位TFST最长(3.0、2.4、1.8、5.3和5.8个月;P < 0.001)。3/4级治疗相关不良事件分别为48%、10%、36%、32%和30%。
7、生物标志物分析:同源重组缺陷(HRD)与复发性铂敏感性卵巢癌(PSOC)患者接受奥拉帕利或西地尼布和奥拉帕利 vs铂类化疗的III期研究临床结果的相关性(NRG-GY004研究)
HRD与PARP抑制剂(PARPi)疗效改善相关,但HRD与抗血管生成药物联合PARPi之间的相互作用尚不清楚。我们探索了NRG-GY004中HRD和临床结果的几种指标
NRG-GY004是一项随机3期研究,旨在PSOC中评估奥拉帕利(olap)或西地尼布+奥拉帕利(ced/olap)对比铂类化疗(chemo)的有效性和安全性。BROCA-HR是一种靶向下一代测序检测方法,可识别生殖系和肿瘤DNA上88个DNA修复或相关基因的所有突变类别。使用单核苷酸多态性的等位基因比率计算杂合性缺失(LOH),作为亚染色体丢失的一部分。通过标准统计方法评价临床结果、同源重组修复(HRR)突变状态和LOH之间的相关性。
在565例随机化患者中,491例患者的BROCA-HR可评价。323例患者的核心HRR基因为野生型(HRRwt),147例为突变型(HRRmt),21例为不可评估(NA)。> 90%的HRRmt为BRCAmt。147例患者的LOH较低,79例较高,265例NA主要是由于肿瘤含量不足。在所有患者中,HRRmt具有预后性(中位PFS 13.7 vs 8.3个月HRRwt;HR 0.41,P< 0.0001)。在HRRmt患者中,化疗、olap和ced/olap的中位PFS分别为12.3、13.1和20.4个月,olap至化疗的HR为0.78(95%CI 0.48~1.27),ced/olap的HR为0.55(0.32~0.95)。在HRRwt患者中,化疗、olap和ced/olap的中位PFS分别为9.0、6.4和8.5个月,olap的HR为1.56(1.15~2.12),ced/olap的HR为0.93(0.68~1.27)。HRR状态可预测olap vs化疗的缓解情况(P=0.0176),但不能预测ced/olap vs化疗的缓解情况(P=0.1009)。校正BRCAmt后,LOH不是独立的预后因素。LOH高患者化疗、olap和ced/olap的中位PFS分别为10.6、8.5和12.2个月,LOH低患者分别为8.1、6.3和8.4个月;与化疗相比,LOH状态不能预测olap或ced/olap缓解。
在NRG-GY004研究的患者中,HRR状态由BRCAmt驱动,与总体预后相关,并可预测olap vs 化疗的缓解情况。
8、放化疗序贯辅助化疗与单纯放化疗比较作为局部晚期宫颈癌的初始治疗:随机、III期OUTBACK研究
OUTBACK研究纳入局部晚期宫颈癌(FIGO 2008 IB期&淋巴结阳性、IB2、II、IIIB或IVA期)患者,1:1随机分组。两组均接受标准放化疗(外照射XRT 40-50Gy,分20-25次,包括淋巴结补量及内照射;XRT期间同步顺铂40 mg/m2,每周一次),试验组在CRT后继续接受辅助化疗(卡铂AUC 5+紫杉醇155 mg/m2,每3周一次,共4周期)。研究的主要终点是5年总生存期(OS),次要终点包括无进展生存期(PFS)、不良事件(AE)和疾病复发模式等。
926例患者进行随机,919例符合条件的患者纳入初步分析。中位随访时间为60个月(IQR:45-65)。
OUTBACK试验的结果表明,标准顺铂放化疗后行辅助化疗并不能改善OS或PFS:5年OS分别为72% vs. 71%(HR=0.90; 95%CI:0.70-1.17;P=0.8);5年PFS分别为63% vs. 61%(HR=0.87;95%CI:0.69-1.07,P=0.61)。两组的疾病复发情况相似。
9、GEM维持治疗在同源重组修复正常(HRP)的初始晚期中的疗效评估(VITAL研究)
VITAL是一项随机、双盲、安慰剂对照、IIb期临床研究,纳入92例一线手术+铂类/紫杉类化疗后达到临床完全缓解的IIIb/IV期上皮性卵巢癌患者,评估了一种自体肿瘤细胞疫苗Gemogenovatucel-T(GEM)作为维持治疗的有效性与安全性。研究组的患者每4周皮内注射一次GEM疫苗(1x10e7细胞/剂)(最多12剂)。主要终点为根据RECIST 1.1评估的符合方案集(PP集)的无复发生存(RFS),次要终点为OS、安全性/毒性、根据BRCA及同源重组修复状态评估的RFS和OS。
总体人群:一线使用GEM免疫治疗作为III/IV期卵巢癌维持治疗的耐受性良好。研究组和对照组的中位RFS分别为11.5个月vs.8.4个月(HR=0.69; P=0.078),中位OS分别为NR vs. 16.0(HR=0.63; P=0.110)。
HRP亚组:本次ASCO会议报告了HRP亚组的分析结果:从随机分组开始,GEM治疗组中的HRP患者(n=25)较安慰剂组中的HRP患者(n=20)的中位RFS(10.6个月vs.5.7个月)与OS(NR vs.26.9个月)有显著改善。
更新的生存数据(2021.04)显示,GEM治疗组中HRP患者的2年OS率(92% vs 55%;P=0.002)及3年OS率(70% vs 40%;P=0.019)均显著优于安慰剂组。
10、仑伐替尼+帕博利珠单抗组合在晚期子宫内膜癌研究
入组患者按1:1随机接受仑伐替尼(20mg PO QD)+帕博利珠单抗(200mg IV Q3W)治疗或TPC(多柔比星 60mg/m2 IV Q3W或紫杉醇 80 mg/m2 IV QW [治疗3周,停药1周])。主要终点为PFS和OS。关键次要终点包括ORR和安全性。
入组的827例(pMMR[n=697],错配修复缺陷 [dMMR,n=130])患者被随机分配接受仑伐替尼+帕博利珠单抗(n=411)或TPC(n=416)治疗,截至2020年10月26日,两组的中位随访时间分别为12.2个月和10.7个月,在pMMR人群中,仑伐替尼+帕博利珠单抗组的中位PFS(6.6个月)明显优于TPC组(3.8个月)(HR=0.60);在总人群中,前者的中位PFS亦明显优于后者,仑伐替尼+帕博利珠单抗组和TPC组的中位PFS分别为7.2个月和3.8个月(HR=0.56)。
同样,在pMMR人群(17.4个月vs 12.0个月 HR=0.68)和总人群(18.3个月vs 11.4个月 HR=0.62)中,仑伐替尼+帕博利珠单抗组的中位OS均优于TPC组。
pMMR人群(30.3% vs 15.1%)和总人群(31.9% vs 14.7%)中,仑伐替尼+帕博利珠单抗组的ORR也优于TPC组。仑伐替尼+帕博利珠单抗组和TPC组的中位治疗持续时间分别为231天和104.5天。
不论MMR状态如何,与化疗相比,仑伐替尼+帕博利珠单抗可明显改善晚期子宫内膜癌患者的PFS、OS和ORR。仑伐替尼+帕博利珠单抗的安全性与既往研究保持一致。


