新型纳米材料可助力烧伤创面的愈合
时间:2022-02-10 13:18:59 热度:37.1℃ 作者:网络
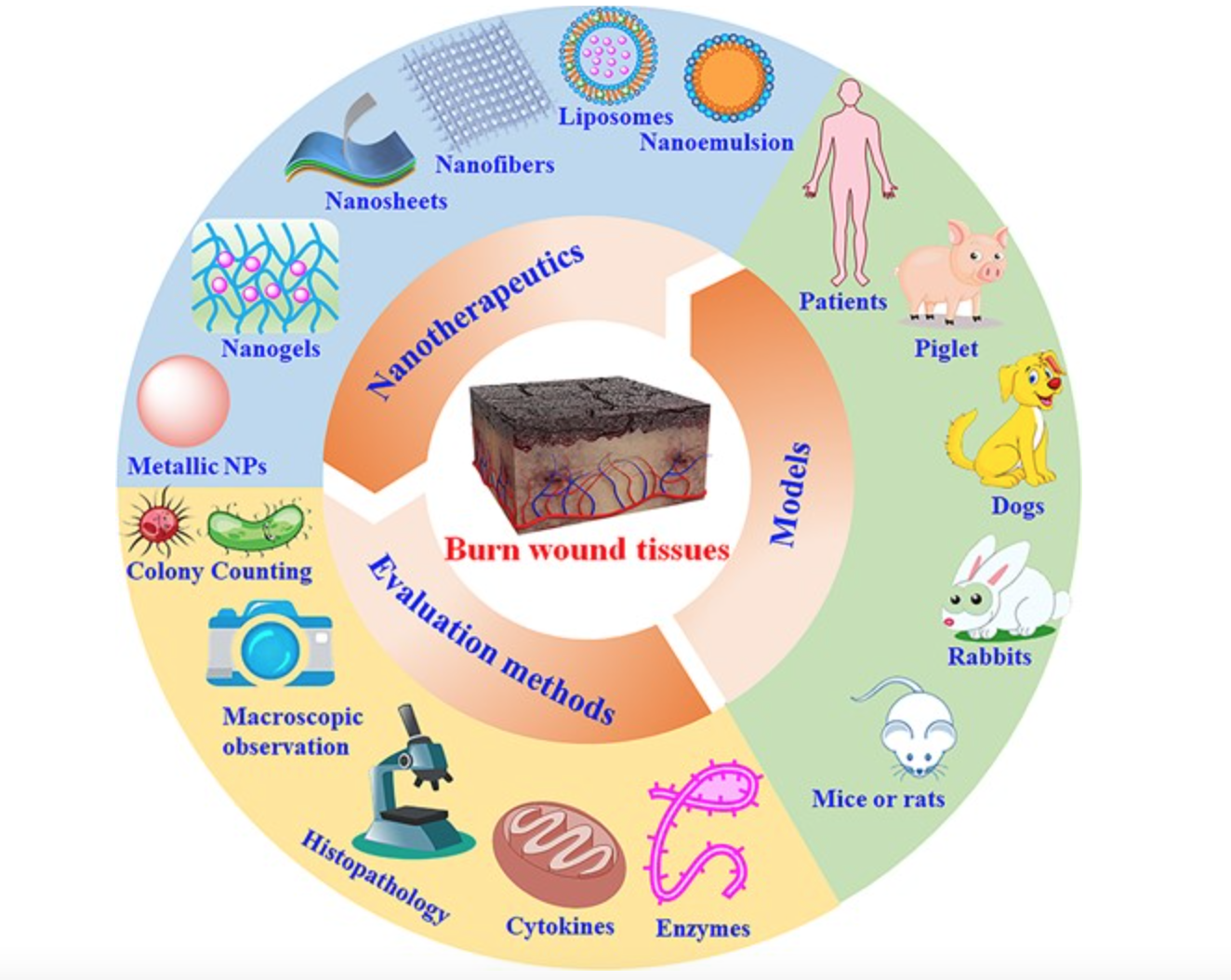
中度或重度烧伤是潜在的破坏性伤害,甚至可能导致死亡。感染预防、抗炎、疼痛管理和生长因子给药在烧伤创面的治疗中起着关键作用。正在开发的新型治疗策略,例如纳米疗法,为烧伤治疗带来了广阔的前景。纳米治疗剂,包括金属和聚合物纳米制剂,已被广泛开发用于治疗各种类型的烧伤。人类和动物研究都表明,纳米疗法在该应用中具有生物相容性和有效性。
纳米技术领域的重大突破为解决一些关键的医学问题提供了机会。

图1 文章来源
烧伤10分钟内:体内平衡发生在烧伤的早期阶段此时最大限度地减少损伤(图 2a)。在这个阶段,含有透明质、纤连蛋白 (FN)、纤维蛋白和凝血酶敏感蛋白 (TSP) 的血凝块形成支架样基质,用于成纤维细胞、白细胞、角质形成细胞和 ECs 的迁移以及由此产生的 GFs 聚集在伤口部位。
烧伤后 1-3 天:此时出现炎症反应。在这个阶段,中性粒细胞聚集在烧伤部位,释放炎症因子,如肿瘤坏死因子α(TNF-α)和白介素-1和-6(IL-1,IL-6);这会激活炎症反应并刺激 VEGF 和 IL-8 分泌以修复血管。此外,单核细胞被转化为活化的巨噬细胞,这些巨噬细胞在伤口部位积聚,产生各种 GFs,如 TGF-α、TGF-β、FGF、PDGF 和 VEGF,以刺激细胞增殖和迁移。
烧伤后3-10天,为肉芽组织的增生期。上皮再形成、新生血管形成和肉芽组织形成(图 2c)。在这个阶段,由活化的细胞因子诱导的上皮再形成导致伤口部位的角质形成细胞、EC、干细胞和成纤维细胞的扩张。此外,各种 GF 的高表达(例如该位点的 VEGF、PDGF、FGF-β 和 GM-CSF)可以促进 EC 的生长。或者,成纤维细胞、粒细胞和巨噬细胞可以形成肉芽组织,然后变成纤维组织,最终形成疤痕。
烧伤后的 2-3 周至 1 年内,伤口完全愈合,这被定义为组织可塑性期(图 2d)。
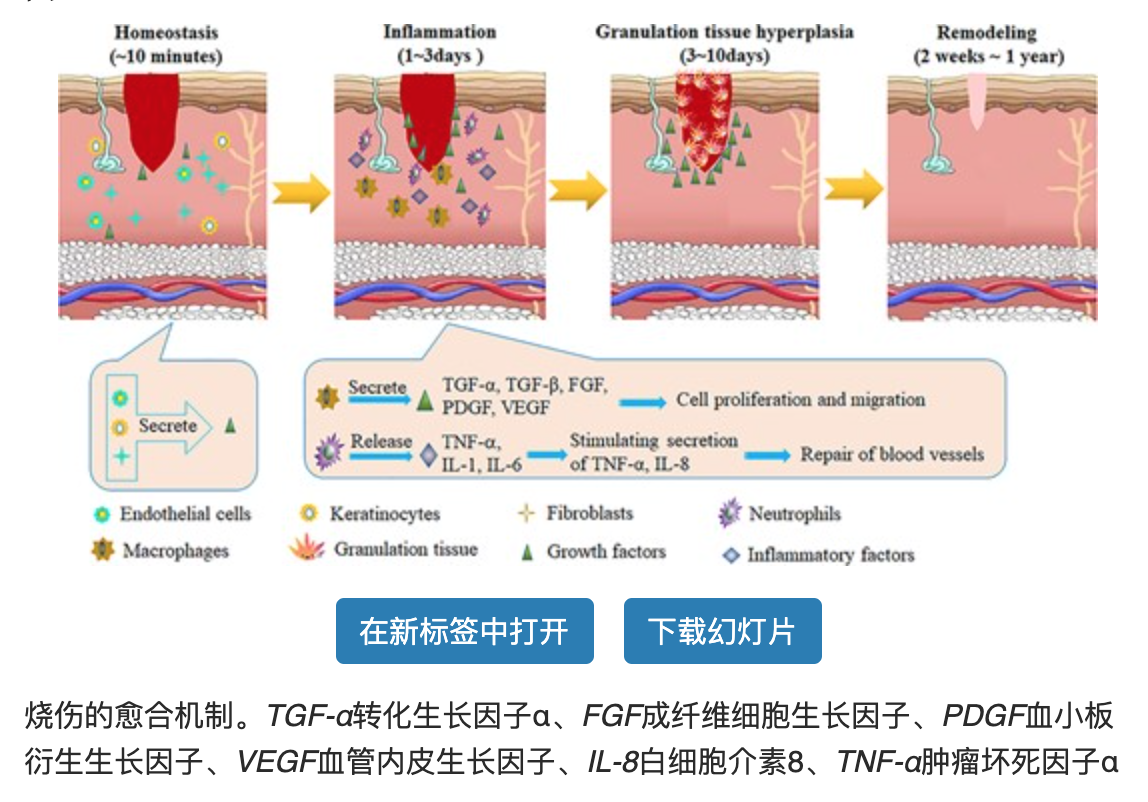
图2 烧伤各阶段
促进烧伤创面愈合的纳米疗法 近20年来纳米技术的快速发展为各种疾病的治疗提供了机遇。纳米治疗药物是药物、生物大分子(例如 DNA、肽、蛋白质)和治疗材料(例如一些金属/金属氧化物、壳聚糖),或在至少一个维度上具有纳米级结构的药物。
纳米疗法在治疗细菌感染方面具有多重优势:
增强药物与细菌之间的相互作用或改变药物的途径以提高其抗菌作用; 增加感染部位的药物浓度,有利于减少药物用量,减轻毒副作用; 提高药物对组织屏障和细菌生物膜的渗透,以克服细菌耐药性; 提高药物的稳定性和延长药物的半衰期。由于其上述优点,聚合物、金属、金属氧化物和其他纳米治疗剂已被广泛用于治疗烧伤创面。金属和金属氧化物纳米治疗剂(例如 Au、Ag 和 ZnO NPs)已被广泛用于治疗烧伤以及各种其他皮肤感染,因为它们具有广谱的抗菌特性。此外,这些纳米疗法可以通过多种方式克服细菌耐药性,例如 DNA 损伤、酶活性破坏、细胞壁破坏、质粒损伤、抑制生物膜形成和氧化应激。
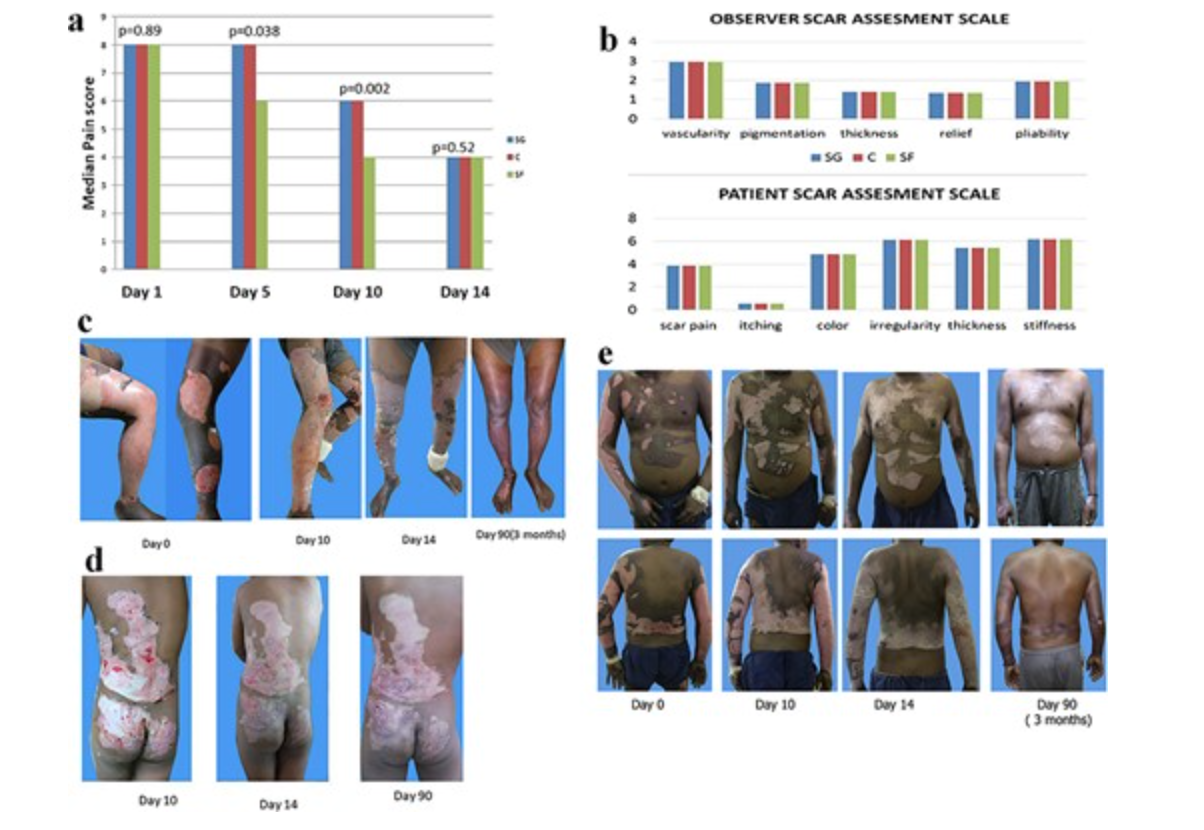
图3基于银的纳米疗法用于治疗 15-40% 部分厚度热烧伤患者的烧伤创面。( a ) 疼痛评估的比较;( b ) 评估 3 个月时的疤痕质量[银纳米颗粒凝胶 (SG)、纳米银泡沫 (SF)、胶原蛋白 (C)];( c-e ) 患者的临床照片评估
如前所述,聚合物纳米材料具有出色的生物相容性和生物降解性,已被广泛用于制造各种用于治疗烧伤伤口的纳米药物(NPs、纳米乳液、纳米凝胶、脂质体、纳米纤维和纳米片)。亲水/疏水药物或 GFs 都可以封装到聚合物纳米材料中,形成各种纳米治疗药物。多糖(例如壳聚糖、葡聚糖)、聚酯(例如 PLGA)、磷脂、透明质酸 (HA) 或聚乙烯醇可用作封装治疗剂的载体。
纳米凝胶作为敷料具有良好的生物相容性和生物降解性以及易于制备等优点。重要的是,这种敷料可以提供湿润、抗感染的愈合环境,并且可以在没有创伤的情况下轻松去除。因此,各种含有抗菌剂或 GFs 的纳米凝胶已成功用于治疗烧伤创面。
自组装短肽纳米纤维已被开发用于促进烧伤伤口的美学修复。纳米纤维是直径为 1-100 nm 的纤维。聚合物如聚氨酯、聚二甲基硅氧烷、聚对苯二甲酸乙二醇酯、聚醚砜、聚(丙烯酸)(PLA)和聚(甲基丙烯酸甲酯)已被用于制造纳米纤维。将抗菌剂(例如 Ag NPs、头孢噻肟)、植物提取物(例如Lawsonia inermis、薰衣草油)和肽加载到纳米纤维上,以治疗细菌感染的烧伤伤口并促进其愈合。

图4 用于处理烧伤伤口的纳米纤维
除此之外还有纳米片。几十纳米厚的纳米片具有独特的物理特性,如高柔韧性、强粘合性和高透明度,使其适合治疗烧伤。涂有纳米片的伤口不仅可以保护伤口免受环境影响,还可以为观察伤口恢复提供视野。因此,细菌纤维素和聚合物(例如 PLA、壳聚糖、聚环氧乙烷)纳米片负载了抗菌剂(例如 ZnO NPs、Ag NPs)、短干扰核糖核酸 (siRNA) 已广泛用于治疗各种类型的烧伤。例如,伊藤等人。制备了载有磺胺嘧啶银 (AgSD) 的 PLA 纳米片,并测试了它们的抗菌性能(图 5a)。
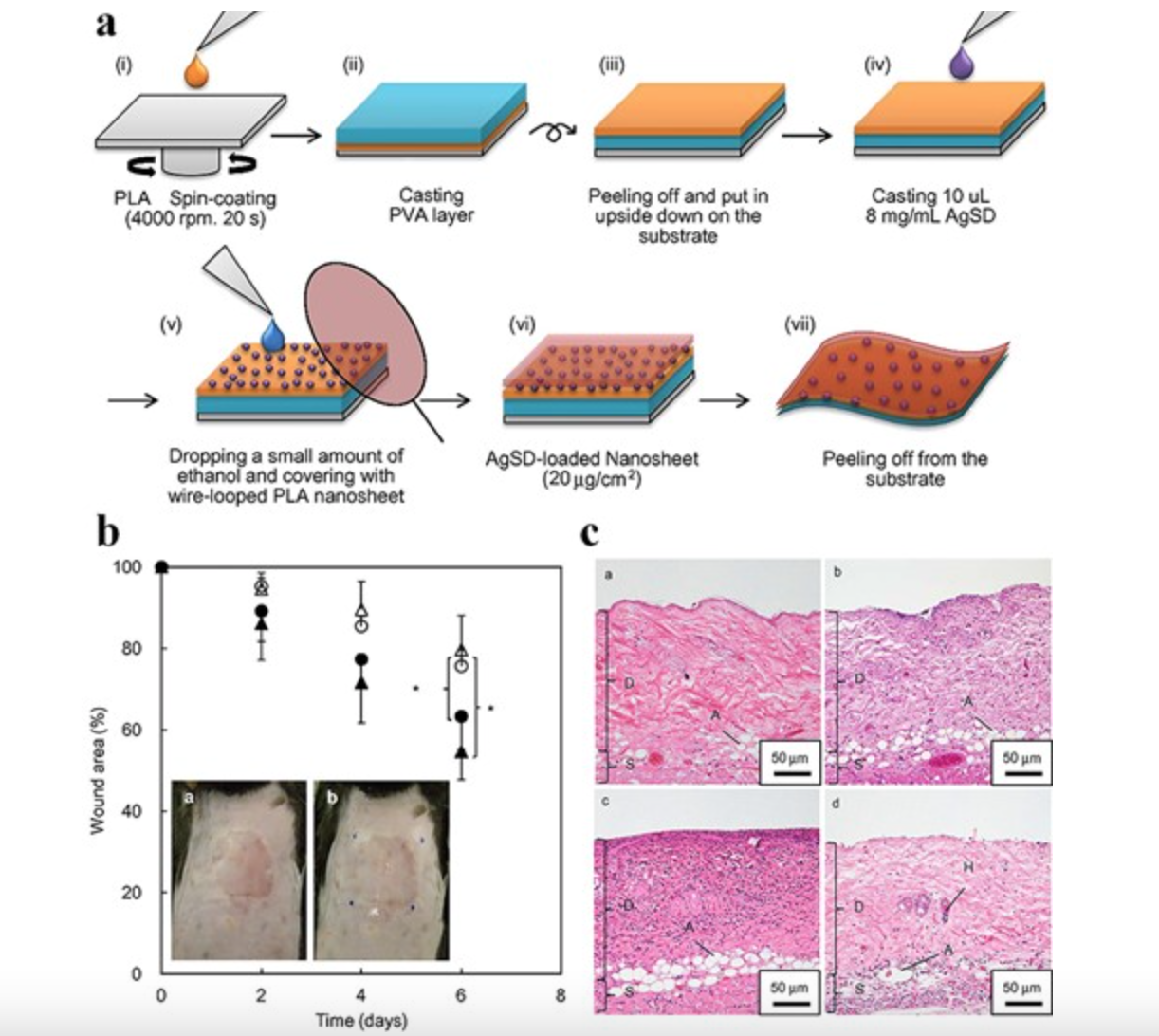
图5 磺胺嘧啶银 (AgSD) 纳米粒子 (NPs) 负载纳米片用于治疗小鼠烧伤创面
乳剂也有相应治疗载体。纳米乳液是热力学稳定的小尺寸载体系统,具有低多分散指数和高动力学稳定性,由水、油和表面活性剂自发形成。由具有抗菌特性的油类(例如Cleome viscosa精油;大蒜、肉桂和丁香油)形成的纳米乳液具有抗菌活性。纳米乳液中的油可以与微生物外膜的脂质物理融合,导致膜不稳定和病原体裂解。纳米乳剂配方已显示出广泛的抗菌特性,并被广泛用于治疗烧伤伤口。多项研究表明,纳米乳液比游离药物表现出更好的活性。总之,与常规给药相比,纳米乳表现出增强的抗菌活性,有利于加速烧伤创面的愈合。
脂质体和固体脂质 NPs脂质体是封闭的囊泡,具有一个或多个水性腔室,通过将不溶性磷脂和其他两亲性物质分散在水中而形成。多种天然和合成磷脂可用于制备脂质体,例如磷脂酰胆碱、神经酰胺胆固醇和磷脂酰乙醇胺。脂质体可以直接与细菌细胞膜融合,并将药物释放到其内部或膜内。它们还可以有效地用于覆盖伤口,在创面创造一个湿润的环境,非常有利于伤口愈合。脂质体能够有效封闭表皮细胞,促进创面愈合,可以在创面皮肤表面提供湿润的环境,因此被广泛应用治疗各种类型的烧伤。
总之,聚合物纳米药物因其优异的生物相容性、生物降解性和高治疗效果而被广泛研究作为各种烧伤创面的治疗方法。特别是,生物大分子和药物可以从聚合物纳米治疗剂中连续释放,以保持伤口中药物浓度一致,这可能会降低给药频率。此外,可以提高生物大分子和药物的生物利用度,因为 NP 可以通过内吞作用或胞吞作用被巨噬细胞和其他细胞内化。
使用纳米疗法治疗这些伤口具有一些优势,例如增加抗菌效果、克服细菌耐药性、促进细胞增殖和减少给药频率。纳米疗法的疗效已在各种动物模型中对不同类型和程度的烧伤进行了评估。一些纳米疗法在烧伤患者中表现出令人满意的治疗效果,使其成为进一步研究其在这些伤口管理中的作用的有希望的候选者。虽然已经取得了可喜的治疗效果,但纳米治疗药物由于其特殊的理化性质,其毒性不容忽视。如何制备具有良好生物相容性和疗效的多功能纳米药物来治疗烧伤尚需进一步研究。特别是,在进行患者应用之前,应在各种动物模型中研究纳米治疗药物的全身毒性。还必须考虑如何制备用于大规模临床实践的纳米治疗药物。尽管在此之前必须克服一些问题,但同样相信未来更多的烧伤患者可以从纳米治疗中获益。
原始文章:
Huang Rong,Hu Jun,Qian Wei et al. Recent advances in nanotherapeutics for the treatment of burn wounds.[J] .Burns Trauma, 2021, 9: tkab026.


