European Radiology:DWI和ASL放射组学特征在区分胶质瘤复发和辐射损伤中的应用
时间:2023-08-19 13:36:29 热度:37.1℃ 作者:网络
众所周知,弥漫性胶质瘤是成年后最常见的原发性颅内肿瘤。放疗和替莫唑胺化疗(TMZ)并结合6个周期的TMZ,是胶质瘤的标准术后治疗方法,但该方法伴随着辐射诱导的脑损伤(RIBI),包括假性进展(PsP)和辐射坏死(RN)。PsP通常发生在放疗后数周至数月内(通常在12周或更长的时间内),由于继发于辐射损伤的胶质细胞髓鞘合成的短暂中断,表现为增强的病灶范围扩大,已被多项研究证明是一个短暂的自我修复过程。RN是一种延迟的辐射引起的脑损伤,常在治疗后几个月或几年后发生。影像学表现是由血管损伤、血脑屏障(BBB)功能障碍和炎症反应引起的不规则边缘或地图状强化。据报道,RIBI的发生率在20.6%-36%之间。
在临床上,病理诊断是RIBI的金标准,但作为一种侵入性检查并不能普遍适用。根据神经肿瘤学反应评估(RANO)的建议,MRI是评价治疗后肿瘤反应的标准诊断方法。然而,由放疗引起的PsP和RN在常规MRI中都表现为增强病变,与肿瘤复发(TR)相似。因此,诊断和处理MRI上的可疑增强病变对临床医生来说是一个挑战。
先进的MRI技术,包括扩散和灌注加权成像,已经显示出区分TR和RIBI的潜力。动脉自旋标记(ASL)作为一种无创的MRI灌注成像方法,可以避免BBB破坏引起的渗漏效应,并提供更准确的量化,是基于造影剂的动态磁敏感对比增强(DSC)的替代方法。然而,很少有研究专注于使用ASL来区分真正的肿瘤进展和RIBI,而且这些研究的样本量通常很小。
放射组学是一种新兴的诊断方法,可从图像中提取大量的特征并将其转换为高维特征,可以全面反映T1WI、T2WI和对比增强T1WI(CE-T1WI)等常规MRI序列的肿瘤空间结构的异质性,并提供非放射组学单参数方法无法获得的隐藏信息。
近日,发表在European Radiology杂志的一项研究通过结合ADC和CBF图建立了一个多参数MRI放射组学模型,在独立验证集上验证了模型的稳健性,并进一步与传统MRI和单参数放射组学模型进行了比较,为临床提供了更多的肿瘤生物学信息,并提高了区分TR与RIBI的诊断准确性。
本项研究从常规MRI、表观弥散系数(ADC)和脑血流(CBF)图中共提取了4199个放射组学特征,这些特征来自96个经病理证实的WHO 2~4级胶质瘤,每个肿瘤都在标准治疗后有增强的表现。使用类内相关系数(ICC)来测试两位医生之间的分割稳定性。使用Mann-Whitney U检验、LASSO回归和RFE算法选择放射组学特征,采用四种机器学习分类器来建立放射组学模型,并使用曲线下面积(AUC)比较了多参数、常规和单参数MRI放射组学模型的诊断性能。这些模型在随后的独立验证组(n = 30)中进行了评估。
选择了8个重要的放射组学特征(3个来自常规MRI,1个来自ADC,4个来自CBF)。使用支持向量机(SVM)做为最佳分类器。数据显示,多参数MRI放射组学模型的诊断性能(AUC 0.96)高于常规MRI(AUC 0.88)、ADC(AUC 0.91)和CBF(AUC 0.95)放射组学模型。在亚组分析中,多参数MRI放射组学模型显示出类似的性能,在WHO 2~3级中AUC为0.98,在WHO 4级中为0.96。
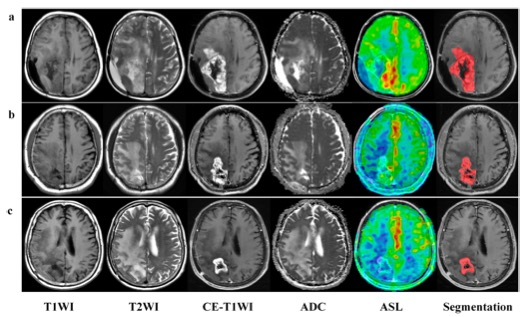
图 a 一位39岁的女性,右顶叶和枕叶有复发性IDH突变的少突胶质瘤。病变在T1WI上显示异质性低信号,在T2WI上显示高信号。CE-T1WI显示边缘强化,中心可见坏死。b 一位54岁的男性,右顶叶和枕叶有复发性IDH野生型胶质母细胞瘤。病变的特点是T1WI上的低信号和T2WI上的高信号,CE-T1WI上观察到环形强化,ASL上显示病变边缘有散在的点状高灌注。 C 82岁女性患者,右顶叶和枕叶IDH突变型星形细胞瘤的RIBI。病变在T1WI上显示异质性低信号,在T2WI上显示高信号,CE-T1WI显示边缘增强,中心无增强。ASL病变显示低灌注
本项研究表明,将无创的DWI和ASL纳入放射组学模型,特别是ASL序列,可显著提高区分RIBI和TR的诊断性能,其稳健性和准确性也在独立验证集上得到了验证。
原文出处:
Jun Zhang,Yue Wu,Yulin Wang,et al.Diffusion-weighted imaging and arterial spin labeling radiomics features may improve differentiation between radiation-induced brain injury and glioma recurrence.DOI:10.1007/s00330-022-09365-3


