【AJH】激素难治性急性GVHD的定义、机制和治疗
时间:2025-04-05 12:11:30 热度:37.1℃ 作者:网络
急性GVHD
激素难治性急性移植物抗宿主病 (Steroid-refractory acute graft-versus-host disease,SR-AGVHD) 是异基因造血细胞移植 (HCT) 的重要障碍,即使在 GVHD 预防和管理方面取得了进展。虽然芦可替尼治疗显示缓解率改善,但生存获益仍不明确。SR-AGVHD患者迫切需要更好的治疗方法。
《American Journal of Hematology》发表综述,重点关注SR-AGVHD的定义、独特病理生理学机制、预后因素以及成人治疗格局的演变。作者认为,新兴疗法具有潜力,但进一步的研究对于更好地定义激素难治性人群、通过生物标志物提高治疗精确度和克服耐药性仍至关重要,尤其是在芦可替尼难治性病例中。

SR-AGVHD的当代患病率和生存率:是否变得更好?
大剂量糖皮质激素(CS)仍是II至IV度急性GVHD患者的首选治疗。从历史上看,50%至65%的患者对这种治疗方法有反应,其余患者则发展为激素难治性急性GVHD,且预后不良。近期在GVHD预防方面的进展在降低严重急性GVHD方面是有效的,然而这是否转化为降低SR-AGVHD的风险仍存在争议,数据结果相互矛盾。
德克萨斯大学MD安德森癌症中心对HLA全相合供者进行的一项回顾性分析(n=964)并未发现在PTCY组(11%至13%)和传统预防组(10%至16%)之间的SR/SD-AGVHD发病率存在显著差异。相比之下,明尼苏达大学的一项研究(n=196)表明,使用PTCY的SR-AGVHD发病率为4.6%,而使用非PTCY预防的发病率为14.7%。值得注意的是,该研究整个人群中任何级别的AGVHD发病率为28%(n=54),只有32例患者发展为II至IV度,显著低于其他研究中超过50%的II-IV度发生率。值得注意的是,该研究包括了半相合供者(37%)、相合亲缘供者(MRD,35%)、相合非亲缘供者(MUD,24%)和不全相合非亲缘供者(MMUD,4%)。目前尚不清楚纳入不全相合供者(其可能从PTCY中获得更大获益)是否促成这些差异,或者是否还有其他因素参与其中。
与对糖皮质激素有反应的患者相比,患有SR-AGVHD的患者非复发死亡率(NRM)增加了两倍(与GVHD预防措施无关),18个月时的NRM率为63%。尽管在这种情况下,6个月总生存率(OS)可能接近50%,但随访时间更长的研究表明,18个月OS仅为20%,2年时仅为17%。在随机REACH-2试验中,芦可替尼达到主要终点,与接受最佳可用治疗(BAT)的患者相比,提高了SR-AGVHD患者的第28天反应率。然而并未转化为显著的生存获益,该研究也并未设计用于检测OS差异,且BAT组患者交叉至芦可替尼组可能导致无OS差异。此外,由于在发表时,芦可替尼组和BAT组的随访时间较短,分别为5.04个月和3.58个月,因此应谨慎解释长期结果。尽管如此,这些结果仍突显了持续研究和开发更有效治疗策略的必要性。
定义SR-AGVHD:优势和劣势
为SR-AGVHD建立一个广泛接受的定义对于比较治疗效果以及指导临床实践中的治疗决策至关重要。历史上,指南和专家意见已经确定了以下定义,这一定义最近在REACH-2研究中也被采用:
-
接受3天的充分治疗(每天2 mg/kg的泼尼松或甲泼尼龙)后器官分期仍进展;
-
接受7天充分的糖皮质激素治疗(每天2 mg/kg的泼尼松或甲泼尼龙)后,II至IV度GVHD仍未改善。
-
其他类别如下所述。
迄今为止,支持这一定义的最好证据来自西奈山急性GVHD国际联盟(“MAGIC”),他们研究了2001年至2016年间接受全身糖皮质激素治疗的任何级别AGVHD患者的治疗结果。大约一半的患者(测试和验证队列中分别为43%至48%)在第7天达到完全或部分缓解(CR或PR;第7天反应者),其余患者归类为第7天无反应者。第7天反应者更有可能在第28天维持其反应,与第7天无反应者相比,非复发死亡率(NRM)也显著降低,12个月生存率更高。这些发现表明,被归类为“难治”的患者预后更差。
然而,根据第7天的状态将患者标记为糖皮质激素难治性是远非完美的。例如,当根据预后生物标志物(REG3a和ST2)对糖皮质激素难治性患者进行进一步分层时,测试和验证队列中分别有48%至72%显示出与低危疾病一致的特征。该亚组的NRM较低,OS与第7天对糖皮质激素反应的患者相似。相比之下,其余比例的患者(28%至52%)具有高危生物标志物概率,似乎真正对糖皮质激素难治,预后极差(表1)。

这些数据表明,在临床上,根据3天后的进展或第7天无反应而被标记为糖皮质激素难治性的患者中,实际上可能有相当一部分应描述为“反应迟缓者”,他们需要超过7天的大剂量糖皮质激素才能实现反应。另一种解释是,这一组患者可能对后续治疗线有反应。支持这一点的是,MAGIC联盟最近进行的一项分析表明,接近二线治疗(包括芦可替尼)时抽取的生物标志物可以预测生存率。
这对接纳临床实践和解释试验数据都具有重要意义。在第7天评估糖皮质激素难治性可能为时过早,而从AGVHD诊断到下一次治疗的中位时间是解释临床试验时的一个重要考虑因素。此外,不同器官(皮肤比肝脏和胃肠道反应更快)以及不同患者对治疗反应的时间可能有所不同。这种复杂性突显了在决定何时开始二线治疗时需要个体化操作,考虑疾病的严重程度、患者合并症以及使用新药物可能带来的额外治疗毒性。在芦可替尼时代,将生物标志物纳入前瞻性临床试验对于分层治疗以及解释某种研究药物的相对疗效至关重要。
其他被接受的临床定义包括在糖皮质激素减量期间或之后GVHD复发,或在接受每天1 mg/kg泼尼松治疗皮肤或上消化道GVHD后出现新的器官受累。很多临床试验允许纳入更多SR-AGVHD的额外人群,例如糖皮质激素依赖(SD-AGVHD)的患者。SD-AGVHD是指最初对糖皮质激素有反应但在减量时AGVHD复发的患者,通常是在指定的最小剂量(每天0.25至1 mg/kg)时。这些患者异质性较高,因为糖皮质激素减量的速度和复发(flare)时的剂量可以显著影响结局。例如,一个在每天1.5 mg/kg糖皮质激素时复发的患者可能与在每天0.25 mg/kg时复发的患者预后不同。事实上有证据表明这些患者有不同的结果。El Jurdi等人表明,与SR患者(46%)相比,糖皮质激素反应组和SD组的2年总生存率显著提高(均为68%)(p<0.1)。糖皮质激素反应组和SD组的2年非复发死亡率也相似,尽管SD-AGVHD与随后慢性GVHD(cGVHD)的更高发生率独特相关。尽管如此,一些前瞻性试验未能发现基于SR类别的结局差异。例如,在REACH-1中,进展组、无反应组和SD组患者对芦可替尼的反应无显著差异;但相对较小的样本量可能限制了检测到有意义差异的能力。
病理生理学:SR-AGVHD的病理生理学是否独特?
新出现的临床前研究表明,与激素敏感性AGVHD相比,SR-AGVHD可能具有不同的病理生理机制。这些机制部分是由糖皮质激素对免疫生物学和胃肠道微生物组的独特作用以及免疫抑制与组织再生和修复之间的复杂相互作用驱动的。传统上,激素的难治性主要归因于免疫抑制不足,从而促使临床试验中强化治疗方法。然而最近的研究提出了另一种假设,了解这些机制对于开发有针对性和有效的治疗方法至关重要。
胃肠道在SR-AGVHD中的作用
大多数SR-AGVHD患者会出现胃肠道受累。胃肠道上皮作为屏障,可防止肠腔内物质的侵入,同时促进营养吸收。肠干细胞(ISC)微环境(包括潘氏细胞)是AGVHD的重要靶点。这些ISC位于肠腺底部,可通过Wnt靶基因Lgr5进行识别,在维持上皮完整性方面发挥关键作用。它们的功能依赖于细胞因子介导的增殖和分化,关键细胞因子包括干扰素γ、IL-17、IL-10、IL-13和IL-22,这些细胞因子促进多能干细胞的发育,从而实现上皮的更新。该通路的某些成分已被探索用于潜在治疗,例如碳酸锂,因其可调节Wnt信号通路。最近,IL-22特别受到关注。在小鼠模型中,IL-22缺乏与肠腺凋亡、ISC耗竭以及胃肠道GVHD进展相关。在小鼠中给予IL-22与改善肠道病理和提高生存率相关,但IL-22在人类中的作用尚未明确,研究表明IL-22可能会加重急性和慢性GVHD。与此同时,一项关于重组IL-22联合皮质类固醇用于新诊断的下消化道GVHD患者的2期研究显示,在第28天时反应率为70%,并且在检查微生物组时发现有独特的微生物反应。此外,小鼠模型已证实,由肠L细胞产生的胰高血糖素样肽-2(GLP-2)具有支持ISC和潘氏细胞修复和维持的再生效应。以teduglutide和apraglutide形式的治疗应用正在研究中。其他细胞,如表达脂联素-2的中性粒细胞,可通过胰岛素样生长因子1受体(IGF-1R)信号通路保护肠道免受GVHD侵害,这也是潜在治疗结果的一个途径。
除了再生作用外,ISC还可以作为抗原呈递细胞(APC),诱导干细胞的分化和修复。CD4和CD8异体T细胞通过黏附分子(mAdCAM)途径迁移到肠道,有助于T细胞的募集和移植后持续的炎症反应。最近的临床数据显示,在一项随机3期试验中,使用药物维得利珠单抗可抑制这一过程,有助于降低胃肠道GVHD的发病率。
Rho相关卷曲螺旋蛋白激酶(ROCK)1和2可介导Rho/ROCK信号通路,驱动T细胞迁移、炎症和炎症细胞因子释放。最近的一项研究突出了在SR-AGVHD患者中ROCK1的主导地位,随后在用ROCK1/2抑制剂治疗的小鼠中观察到AGVHD严重程度的改善。鉴于ROCK2抑制剂belumosudil最近获批用于治疗慢性GVHD,这一发现尤为引人注目。
皮质类固醇及耐药机制
皮质类固醇(CS)通过糖皮质激素受体介导的抑制抗原呈递细胞(APCs)和T细胞中的核因子κB(NF-κB)通路,以及阻断Toll样受体(TLR)介导的信号传导,从而抑制炎症,是治疗AGVHD的核心手段。因此,皮质类固醇能够抑制促炎细胞因子和趋化因子,抑制Th1和Th17细胞的分化,并促进Th2细胞和调节性T细胞(Tregs)的生成。然而矛盾的是,长期使用皮质类固醇可能会加剧炎症,也促使了对SR-AGVHD中耐药机制的研究。
皮质类固醇不仅抑制T效应细胞的功能,还会损害调节性T细胞的诱导,从而破坏长期的外周耐受性。临床前研究表明,长期使用皮质类固醇会导致Toll样受体(TLR)和NLRP3表达增加,进而改变糖皮质激素受体并释放促炎细胞因子,从而加剧炎症。鉴于完整的糖皮质激素受体对于减轻GVHD的严重程度是必要的,因此认为细胞因子、DAMPs和PAMPs可能是SR-AGVHD的关键驱动因素。
尽管供者T细胞是引发AGVHD的核心因素,但在SR-AGVHD的发展中,它们似乎并不那么重要,这可能与它们受到之前皮质类固醇和钙调磷酸酶抑制剂(CNI)暴露的抑制有关。小鼠模型的研究显示,在对类固醇有反应和类固醇难治性受试者之间,供者T细胞的特征没有显著差异,这表明还涉及其他机制。此外,评估去除T细胞(如抗胸腺细胞球蛋白ATG或inolimomab)对SR-AGVHD结果影响的试验也未显示出改善。特定的T细胞亚群(特别是Th17细胞)可能逃避皮质类固醇的抑制,这可能是由于它们具有耐药机制,例如P-糖蛋白外排泵,从而导致持续的组织损伤。
涉及ISC及其微环境的肠道特异性类固醇耐药机制已被识别。Hanash等人最近的研究表明,皮质类固醇直接靶向肠道上皮细胞,并损害其再生能力,导致ISC、潘氏细胞的丢失,最终导致小鼠模型中肠腺的丢失。这最终加剧干扰素γ诱导的ISC凋亡,并导致免疫调节蛋白(如α1-抗胰蛋白酶)的丢失(这些蛋白对肠道完整性至关重要)。而芦可替尼可通过抑制干扰素γ信号传导和细胞因子反应,促进调节性T细胞的生成,从而保护ISC免受干扰素γ诱导的凋亡,并减少ISC/潘氏细胞的丢失。
皮质类固醇对肠道愈合能力的损害以及对免疫稳态的破坏会影响肠道微生物群,导致肠道菌群失调和微生物多样性降低。这种菌群失调会刺激促炎细胞因子的产生,从而加剧组织损伤。短链脂肪酸(SCFAs,如丁酸)是细菌的代谢产物,会影响黏膜免疫。值得注意的是,在小鼠模型中,口服丁酸与减轻胃肠道GVHD的严重程度和改善长期预后相关。共生菌的丢失会促进与胃肠道GVHD相关的病原体的增殖。进一步研究微生物代谢产物对于理解其在SR-AGVHD中对免疫反应的影响至关重要。
SR-AGVHD的治疗
芦可替尼
芦可替尼是一种口服Janus激酶(JAK)1/2抑制剂,已成为SR-AGVHD的核心治疗药物,它通过调节免疫细胞的发育、增殖和激活,抑制细胞因子信号传导并促进调节性T细胞的生成。此外,芦可替尼可抑制干扰素γ(IFN-γ)信号传导,保护细胞免受IFN-γ诱导的凋亡,并可能直接影响ISC。
芦可替尼的耐受性总体良好,常见不良事件包括血细胞减少症、巨细胞病毒(CMV)再激活/感染、败血症和菌血症。2019年,美国FDA基于REACH-1试验的结果批准了芦可替尼用于SR-AGVHD,随后欧洲药品管理局(EMA)于2022年也批准了其应用。这一批准显著改变了SR-AGVHD的治疗模式,确立了芦可替尼作为二线标准治疗的地位。
REACH-1试验是一项开放标签、单臂、多中心的II期临床试验,共纳入71例≥12岁的SR-AGVHD患者,患者接受剂量递增的芦可替尼治疗(起始剂量为每日两次5mg)。68%的患者为III–IV度AGVHD。结果显示第28天的总缓解率(ORR)为55%,完全缓解(CR)率为27%,治疗期间的最佳ORR为73.2%。
随后的国际多中心随机III期REACH-2试验进一步验证了这些结果,其比较了芦可替尼(每日两次10 mg)与最佳可用治疗(BAT;包括ECP、吗替麦考酚酯、依那西普、ATG、间充质干细胞[MSC]、英夫利昔单抗和 mTOR 抑制剂)的效果,结果显示芦可替尼组的第28天ORR显著优于BAT组(62.3% vs. 39.4%;OR=2.64,p<0.001),且这种改善在 III/IV 度 GVHD 中持续存在(III度;53% vs. 28%,IV度;56% vs. 23%)。尽管最初对芦可替尼有令人印象深刻的反应,但第56天的持久缓解率下降到约40%,仍显著优于对照组 (22%);表明两组中的大多数患者需要额外治疗或死亡,再次突出了 SR-AGVHD 患者的不良预后。中位缓解持续时间为163天。令人失望的是两组间 NRM 无显著差异,但中位 OS 有改善趋势(11.1个月vs. 6.5个月;HR=0.83;95%CI,0.60–1.15)。无应答者的结局不佳,NRM在第100天接近80%,中位生存期仅为1个月。缓解降低的相关因素包括 III/IV 度疾病、下消化道和肝脏受累。不良事件与 REACH-1 相似,主要是血细胞减少(血小板减少27%,贫血22%)和感染(巨细胞病毒感染;26%)。芦可替尼组和 BAT 组的不良事件发生率(包括病毒再激活发生率)相当。
芦可替尼的剂量优化仍存在关键挑战,尤其是在管理血细胞减少症和与CYP3A4抑制剂(如唑类药物,可增加芦可替尼血药水平)的相互作用方面。在REACH-2试验中,38%的患者需要调整剂量。厂家建议在严重血细胞减少症或与强CYP3A4抑制剂联合使用时,将剂量减少至每日两次5mg。实际应用中,许多患者(48%–66%)从5mg每日两次开始治疗,随后增加到10mg每日两次。密切监测血细胞计数对于管理需要剂量调整的血细胞减少症至关重要。虽然药物监测具有一定潜力,但目前尚无数据支持其常规使用。
芦可替尼难治性患者
这些结果表明,定义芦可替尼难治性和芦可替尼依赖性患者极为重要,以便区分缓解较慢的患者和需要三线治疗的患者。在REACH-1试验中,至缓解的中位时间为7天(范围6–49天),其他回顾性数据显示至缓解时间范围为7到77天。大多数患者似乎在14天内有所改善,但也有约30%的患者在1–2个月后出现晚期缓解。不同器官的至缓解时间也有所不同,皮肤和肝脏通常比胃肠道疾病更早出现缓解。在临床实践中,芦可替尼在获得批准并广泛使用后,被更早地整合到治疗方案中(在达到类固醇难治性标准之前),尽管缺乏数据支持这种干预措施的获益。
Mohty等人将芦可替尼难治性患者定义为在芦可替尼治疗后5–10天出现GVHD进展(分期/分级或新器官受累)、在>14天后没有改善或在最初改善后失去反应的患者。这一亚组患者存在重大的治疗挑战,真实世界的数据一致显示其预后较差。一项回顾性研究报告了48例芦可替尼耐药的SR-AGVHD患者的结果,其中“芦可替尼难治”的原因包括无反应(50%)、AGVHD进展(21%)和失去反应(29%)。胃肠道是这些耐药病例中最常见的AGVHD受累部位(69%),在该组中,对后续治疗的总缓解率为36%,中位生存期仅为21天。值得注意的是,芦可替尼治疗的中位持续时间为9天(范围4–29天)。关于那些因无反应而被标记为“难治”的患者中,有多少是真正的难治者,有多少是缓解较慢者,仍存在争议。在作者的实践中,在没有毒性的情况下,会给予芦可替尼至少1个月的治疗时间,并可以选择同时开始三线治疗,以考虑上述30%的对芦可替尼反应较晚的患者。在芦可替尼减量结束时复发的患者可以被定义为芦可替尼依赖,并应恢复治疗。
尽管没有明确的证据指导如何管理类固醇难治性GVHD患者的其他免疫抑制剂,但无效的治疗应该被停止。在没有毒性的情况下,应在充分尝试10–14天后快速减量皮质类固醇,以给缓解较慢的患者留出时间。作者通常每4–7天将皮质类固醇减少25%,直到患者处于最小剂量。传统上,钙调磷酸酶抑制剂等免疫抑制剂会继续使用,但作者的做法是停止其他预防性药物,如吗替麦考酚酯。支持性护理,包括在适当情况下提供肠内营养(在没有肠梗阻的情况下)、谨慎使用阿片类药物和止泻药、物理治疗、感染管理以及预防措施,都应得到重视。
芦可替尼之外的治疗
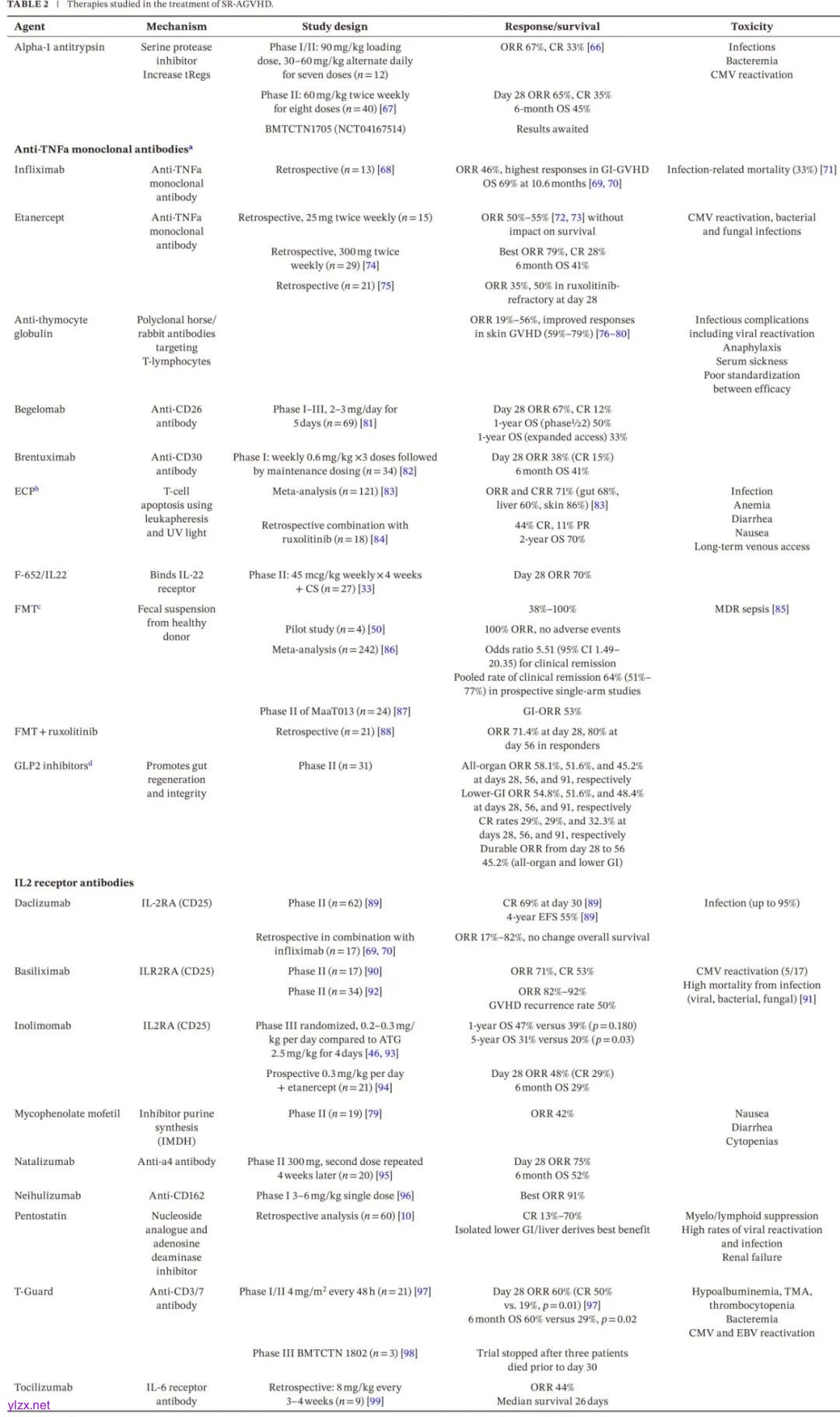
关于最佳三线治疗尚未达成共识,每种选择均伴有相当大的费用。由于缺乏前瞻性试验数据、试验设计的变异性和患者数量较少等因素,确定最佳治疗具有挑战性。严格的入选标准通常会导致低危患者比例过高,从而扭曲研究结局。芦可替尼早期引入治疗方案使新疗法的评价进一步复杂化,使许多三线选择的严格科学评估机会有限。目前尚不清楚是否应在芦可替尼之外或直接比较中进行进一步研究。此外,由于越来越多地在预防背景下研究芦可替尼,其对总体病程的影响,尤其是在后来发生 SR-AGVHD 的患者中,将带来治疗挑战。因此,治疗决策必须考虑毒性风险、给药便利性、合并症以及医生和机构的经验。以下章节简要综述了 SR-AGVHD 的当前治疗和缓解率(表2),重点关注新型和细胞疗法。
细胞疗法
间充质干细胞
间充质干细胞 (MSC) 是具有多能分化能力的干细胞,它们可以从骨髓、脂肪组织或脐带中获得,并通过静脉输注,通常无不良事件。它们通过释放吲哚胺2,3-双加氧酶 (IDO)、前列腺素E2、IL-10、TGF-β等细胞因子,抑制 T 细胞增殖,促进组织再生,证明其免疫调节特性。这些效应是通过旁分泌活性以及将DNA、RNA和其他小分子转运至靶细胞的外泌体(或微泡)转运产生的。
虽然诱导应答的生物学机制很有前景,但MSC在 GVHD 中的疗效一直存在争议。初始病例报告和欧洲研究显示了显著的结果,包括 IV 期 SR-AGVHD 完全缓解,但后续研究未能一致地重复这些结果。行业申办的 Osiris 试验 (NCT00366145) 是第一项研究骨髓来源MSC (BM-MSC) 治疗 SR-GVHD 的 III 期随机对照试验,尽管其仅以摘要形式发表。该研究显示与安慰剂相比,第28天 CR 未改善(82% vs. 73%, p=0.12)。肝脏和肠道 GVHD 患者的 CR 和 PR 率较高,儿童人群的事后分析符合统计学显著性。在另一项多中心随机安慰剂对照试验中观察到相似结果,发现组间结局无差异。主要结局为持久CR,定义为 CR 至少28天,MSC组和安慰剂组分别有37%和32%达到;ORR分别为58%和54%,OS分别为34%和42%。与该领域的许多研究一样,对照组二线药物的选择存在显著异质性。Kurtzberg 等人已发表的儿科患者单臂 III 期数据支持第28天 ORR 改善,以及第100天 OS 显著改善 (82.1% vs. 38.6%,p<0.001)。然而,即使在该患者人群中也不具有广泛的适用性。
在成人中进行的许多研究显示出获益混杂,并且最近的Cochrane综述(纳入2018年12月之前的12项RCT)未发现支持疗效的证据,尽管MSC治疗被广泛认为是安全的。最近对64例接受 BM-MSC 治疗芦可替尼难治性 GVHD 患者的真实世界数据进行的回顾性审查表明,与未接受 MSC治疗的患者相比,OS令人鼓舞。MSC与替代 AGVHD 药物的协同组合仍在研究中,随机数据支持MSC中加入钙调磷酸酶抑制剂和巴利昔单抗(改善第28天OR,82.8% vs. 70.%,p=0.043)。
结果的不一致可能归因于研究设计的差异、学术和行业之间的生产差异(包括培养扩增和增殖方法)、供者来源和反应定义的差异。这些问题阻碍了在成人和儿童环境中的FDA批准。最近 FDA 批准Remestemcel-Lrknd(Ryoncil,Mesoblast Inc.) 用于儿童 SR-AGVHD 是一个重要的里程碑,可能为在成人中进行更稳健的研究铺平道路。截至2024年10月,多项试验正在进行中,以研究MSC与BAT以及与其他药物的比较(见表3)。

粪便菌群移植
粪便菌群移植 (FMT) 是将健康供者的粪便悬液移植给 AGVHD 患者,以恢复菌群多样性并调节 T 细胞功能。病例报告显示前景良好,在4例肠道 SR-AGVHD 患者中开展的一项小型初探性研究显示 ORR 为100%,未发生重度不良事件。有趣的是,微生物群多样性的变化似乎与患者症状相关,同时观察到效应 T 调节细胞的增加。
另一项纳入8例接受 FMT 治疗 GI SR-AGVHD 患者的研究显示,所有患者均达到临床缓解,且细菌多样性得到改善。类固醇难治性和类固醇依赖性 AGVHD 的荟萃分析(23项研究,242例患者)报告,观察性研究中临床缓解的比值比为5.51,前瞻性单臂研究中临床缓解的汇总率为64%。虽然基于较小的患者队列和有限的质量,但不良事件极小且可耐受。有趣的是,还描述了 FMT 对皮肤和肝脏 aGVHD 的有益全身作用。然而,随后的病例报告说明了加强供者筛查以减少微生物传播的重要性,因为已报道2例多重耐药菌菌血症重症病例,包括1例导致死亡的病例。
一项在111例III–IV度GI SR-AGVHD 患者中开展的异基因微生物治疗 (MaaT013) 的大型欧洲单臂研究显示出合理缓解,更新后的 GI-ORR 为53%。24例患者中有3例发生败血症,但尚不清楚 FMT 在该易感人群中增加风险的作用。在接受含多重耐药菌的 FMT 产品治疗的患者中,已有关于致死性血流感染的报告,且粪便测序将感染与同一粪便供者相关联。严格的供者筛查和粪便检测对于避免 MDR 传播至关重要。MaaT013 目前正在欧洲芦可替尼耐药人群中进行 III 期研究 (NCT04769895)。
已经探索了 FMT 和芦可替尼的联合治疗方式,包括在最近的4例患者的小病例系列中,早期给予联合治疗产生有希望的结果。另一项研究报告了21例III–IV度下消化道 AGVHD 患者的结局,这些患者在 CS 治疗3天后进展或5天后无缓解。该研究显示出令人鼓舞的结果,第28天的 ORR 为71.4%。正在进行许多前瞻性研究(表3),以进一步评价安全性和疗效。虽然早期结果很有前景,但需要更大规模的研究来验证。
AAT
A1-抗胰蛋白酶 (AAT) 是一种由肝脏产生的丝氨酸蛋白酶抑制剂,具有多种免疫调节作用,包括减少促炎性细胞因子和促进 T 效应细胞向 T 调节细胞的转变。在40例≥III度 SR-AGVHD 患者 (70%) 的单臂研究中,每4周一次静脉输注 60 mg/kg AAT 后,第28天的 ORR 和 CR 率分别为65%和35%。GI-GVHD 的第28天缓解令人鼓舞,为64%,而肝脏 GVHD 的 ORR 为57%。重要的是治疗耐受良好,无3级以上不良事件。这些有前景的结果导致在随机 BMTCTN 1705 III 期试验 (NCT04167514) 中对高危患者一线治疗的 AAT 进行了研究,其结果备受期待。
GLP2抑制剂
胰高血糖素样肽 (GLP-2) 是由肠道 L 细胞产生的一种激素,对肠道完整性具有保护和再生作用。Teduglutide是一种人重组 GLP-2 类似物,在儿科人群中显示了良好结果。STARGAZE II期试验在下消化道GVHD患者中研究了apraglutide与BAT联合治疗,证实初始良好的耐受性和疗效,尽管随访时间有限。第28、56和91天的全器官 ORR 分别为58.1%、51.6%和45.2%,下消化道 ORR 分别为54.8%、51.6%和48.4%。在第56天和第91天,较低的消化道ORR 仍然持久(两个时间点均为45.2%)。到第28天,25.8%的患者达到全器官CR,而29%达到下消化道CR,第56天和第91天的持续率分别为29%和45.2%。这些缓解的持久性令人鼓舞,尤其是在仅包括下消化道 aGVHD 的研究人群中(与 REACH-2 队列相比)。
RIP激酶抑制剂
受体相互作用蛋白激酶 (Receptor interacting protein kinase ,RIPK1) 是肠道细胞凋亡的调节因子,小鼠模型表明 RIPK1 抑制可减少 GVHD 诱导的细胞凋亡和相关死亡率。研究 RIP 激酶抑制的前瞻性试验 (Zharp1-211) 提前关闭,但这仍然是该领域的新治疗模式。
未来方向
确定SR-AGVHD临床试验的理想终点是下一步必不可少的工作。虽然在新诊断的 AGVHD 患者中,第28天缓解与6个月 NRM 相关,但其可能不是疾病更晚期的最佳替代指标。REACH-2 研究强调了这一点,其中芦可替尼导致第28天应答优于BAT,但不影响NRM。引入无 GVHD 生存期、OS和复发等终点是允许医生得出关于治疗选择有效结论的重要工具。此外,使用的终点应获得监管机构的认可,以确保批准这些患者的有效治疗。未来的试验还应纳入生物标志物,以丰富对基线患者特征的理解,并预测可能获益的人群或加深对研究干预的病理生理学和药效学的见解。临床前研究正在扩展我们对 SR-AGVHD 免疫生物学的理解,并开始基于这一见解转化为靶向治疗。未来的研究将需要确定在芦可替尼难治性患者中是否也发挥了相同机制。可以想象,暴露于芦可替尼可能导致独特的耐药机制(与类固醇不同),在试验设计中可能需要考虑芦可替尼暴露或作为差异化的研究人群。
总结
尽管 GVHD 预防和管理取得了进展,但激素难治性 AGVHD 仍然是异基因 HCT 后的重大挑战。虽然芦可替尼显示缓解率改善,但这些获益并未转化为 OS 改善,强调了对更有效治疗的持续需求。更深入地了解 SR-AGVHD 的独特病理生理学,特别是关于胃肠道、ISC以及糖皮质激素、微生物组和免疫系统之间的相互作用,为新型治疗策略铺平了道路。这些新兴疗法有望改善预后,同时最大限度地减少与传统免疫抑制剂相关的毒性。未来的研究应侧重于建立标准化标准,以定义和理解真正的激素难治性人群,纳入生物标志物以增强患者分层和机制理解,并解决耐药性的发展,尤其是在芦可替尼难治性人群中。当然,最终目标仍然是通过皮质类固醇以外的一线治疗的有效预防和优化来预防 SR-AGVHD 的发生。我们在 SR-AGVHD 管理方面取得了长足的进步,但仍有许多有待学习的地方,继续进行专门的研究对于进一步改善这些患者的预后至关重要。
参考文献
Am J Hematol. 2025 May:100 Suppl 3:14-29. doi: 10.1002/ajh.27592.


