CAR-T后的CRS,托珠单抗治疗可导致低纤维蛋白原血症
时间:2024-10-03 20:00:56 热度:37.1℃ 作者:网络
低纤维蛋白原血症
CAR-T细胞疗法是血液肿瘤的重大突破,但也可引起严重的副作用,包括细胞因子释放综合征(CRS)。每两例CAR-T治疗的患者中就有一例发生凝血异常,且凝血障碍的严重程度与CRS的严重程度相关。CRS相关凝血障碍与低纤维蛋白原血症相关,目前认为低纤维蛋白原血症是播散性血管内凝血(DIC)和肝功能障碍的结果。考虑到低纤维蛋白原血症的高发生率与重度CRS的低发生率并不一致,导致很多低纤维蛋白原血症无法解释,学者研究了41例CAR-T治疗的血液恶性肿瘤成人患者中低纤维蛋白原血症的发生率和危险因素,结果近日发表于《Haematologica》。

研究结果
研究纳入2020年1月至2023年5月期间在雷根斯堡大学医学中心接受CAR-T细胞治疗的41例连续血液恶性肿瘤成人患者(中位年龄69岁,范围38-83岁,73%为弥漫性大B细胞淋巴瘤),93%的患者发生CRS,≥3级为13%;约1/3的患者发生ICANS,2例为4级。71%的患者接受托珠单抗。
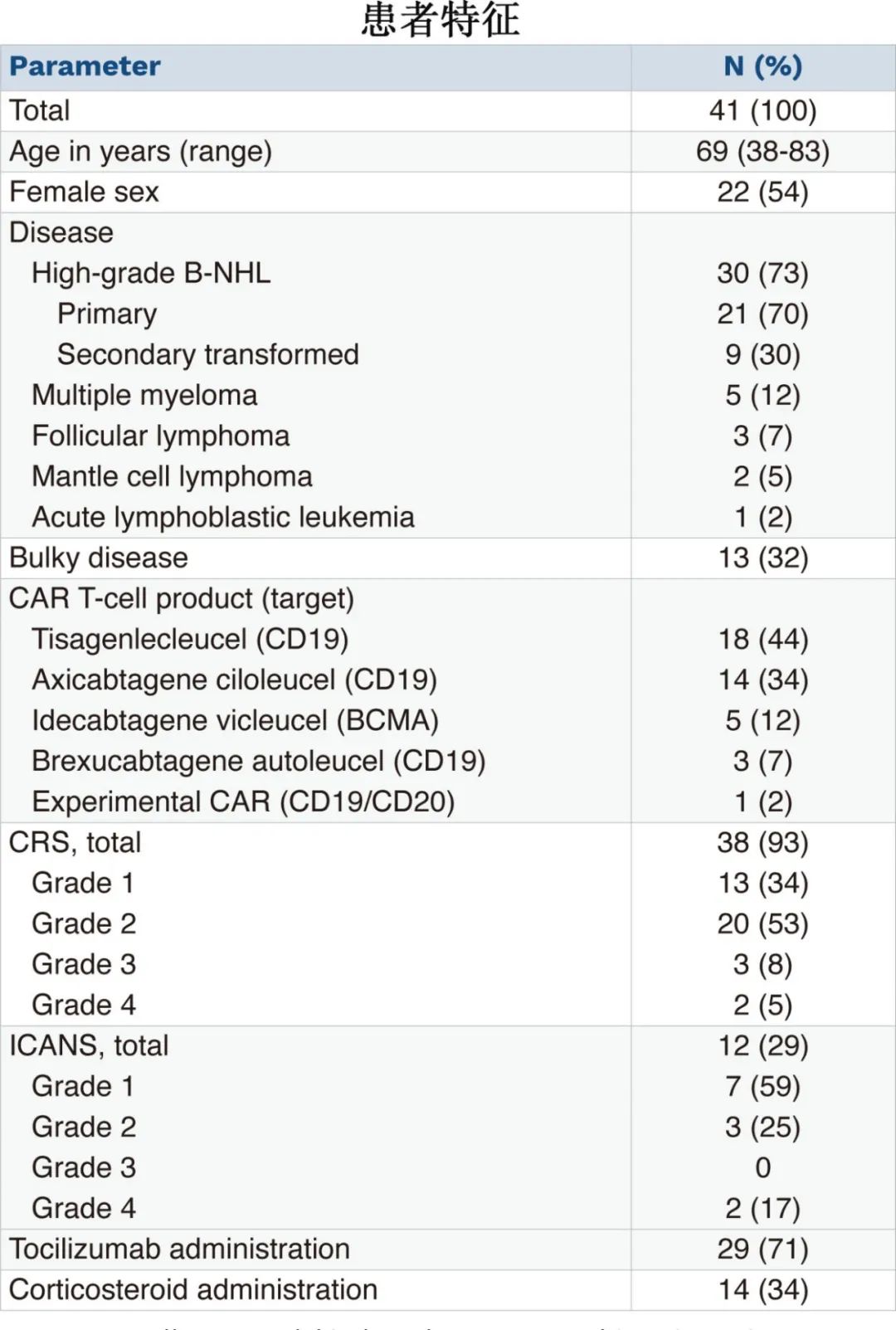
66%的患者CAR-T后发生低纤维蛋白原血症,11例(41%)为重度(CTCAE 3-4级),且均与CRS发作相关。1级CRS患者中仅38%(5/13)发生低纤维蛋白原血症,而≥2级CRS患者中高达88%(22/25),低纤维蛋白原血症的严重程度随CRS级别的增高而增高。
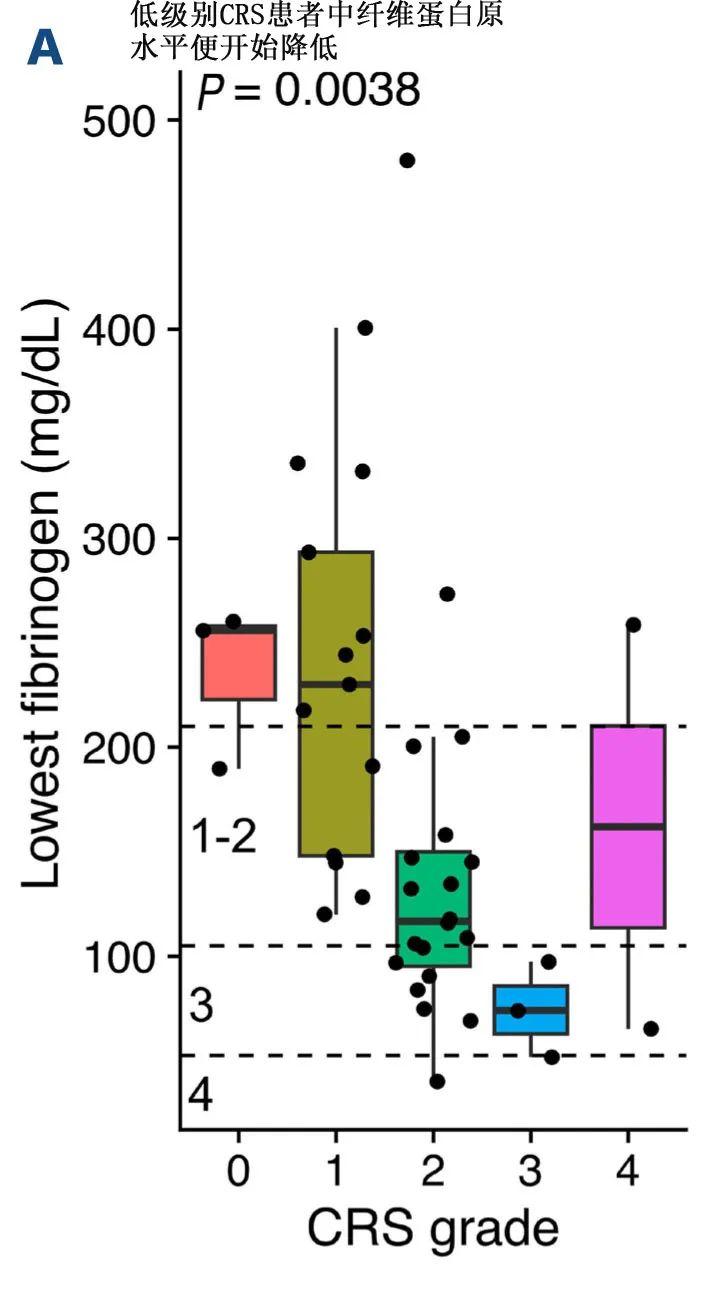
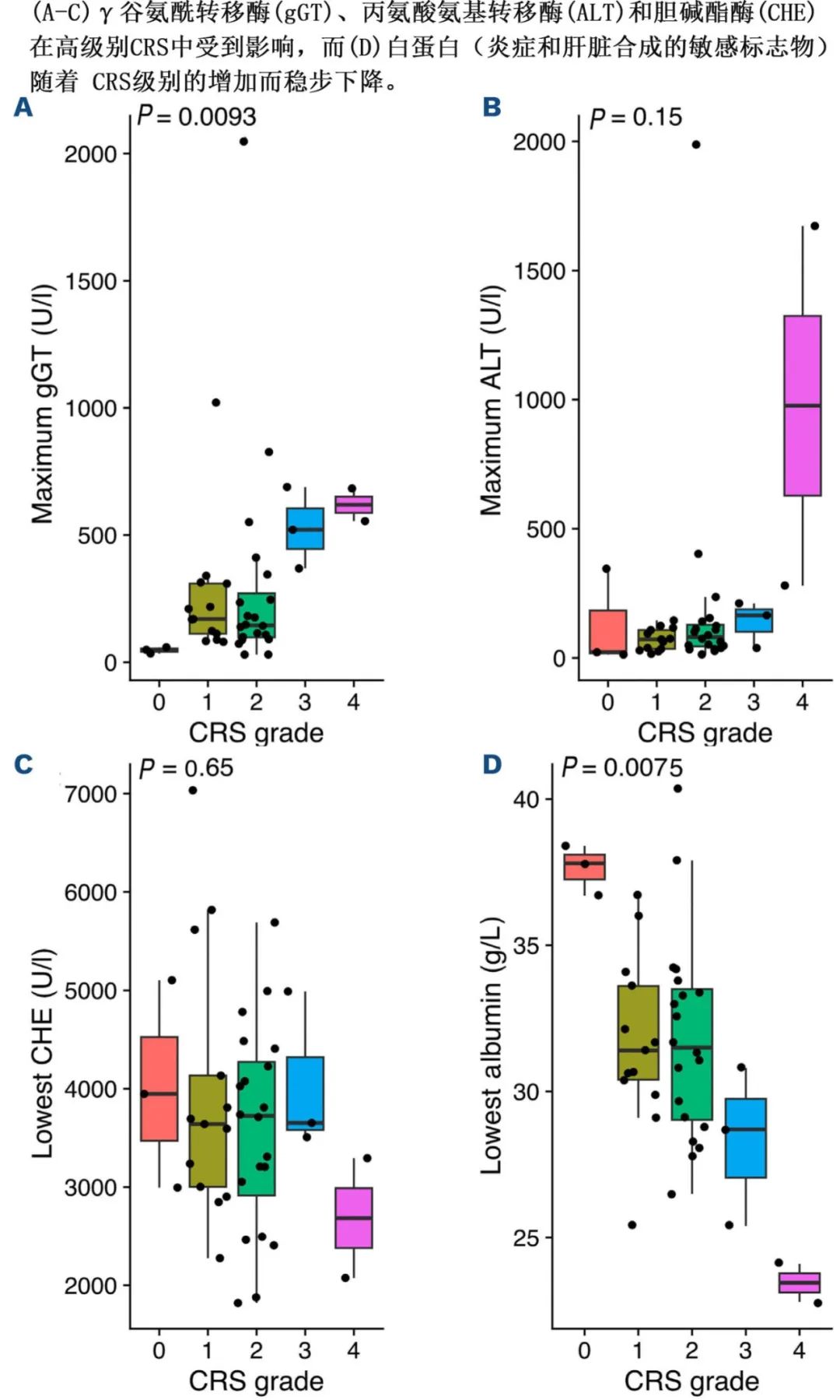
从数据看,从1级CRS便开始发生低纤维蛋白原血症;CAR-T治疗后低纤维蛋白原血症的假设之一为由于肝病导致肝脏合成受损,但研究中DIC和肝功能障碍主要发生于重度CRS(≥3级)患者中。总体而言,非功能性肝损伤发生较早且取决于CRS的严重程度,但临床有意义的肝功能障碍仅发生在CRS晚期。
CRS期间纤维蛋白原水平最初升高,托珠单抗治疗后呈剂量依赖性下降(r=-0.44, P=0.004),而未接受托珠单抗治疗的患者纤维蛋白原水平升高。Logistic回归分析确定托珠单抗是低纤维蛋白原血症的独立危险因素(优势比=486,P<0.001)。
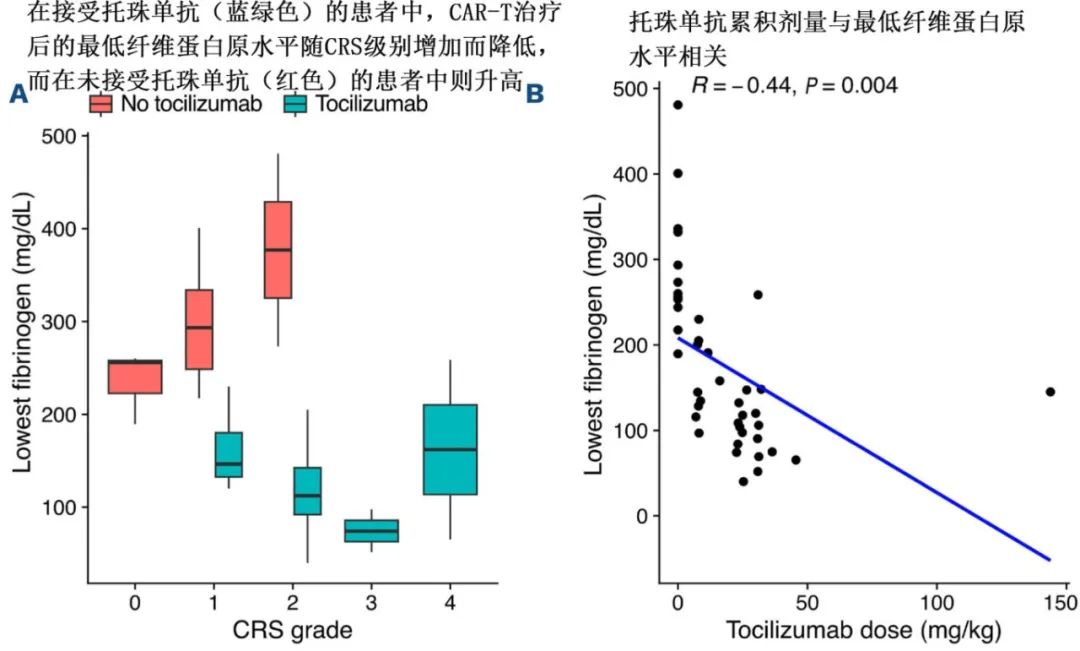
作者假设,CRS患者的纤维蛋白原合成在白介素-6依赖性急性期反应中上调,以补偿CRS诱导的凝血因子消耗,托珠单抗可抑制纤维蛋白原上调而导致长期低纤维蛋白原血症。
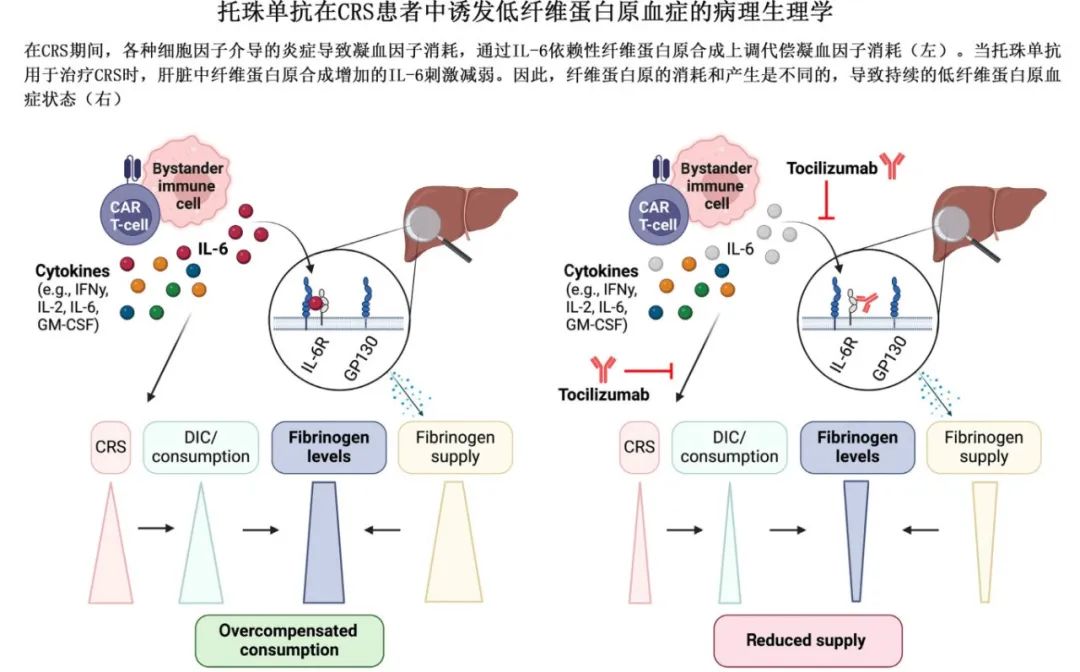
总体而言,该研究为CAR-T细胞治疗后低纤维蛋白原血症的病理生理学提供了新的见解,并强调了在托珠单抗治疗CRS后密切监测纤维蛋白原的必要性。
参考文献
Perl M, Herfeld K, Harrer DC, Höpting M, Schweiger M, Sterz U, Knödler L, Heimerl S, Hansmann L, Herr W, Poeck H, Wolff D, Edinger M, Hart C, Fante MA. Tocilizumab administration in cytokine release syndrome is associated with hypofibrinogenemia after chimeric antigen receptor T-cell therapy for hematologic malignancies. Haematologica 2024;109(9):2969-2977; https://doi.org/10.3324/haematol.2023.284564.


