衰老细胞治疗:协同抗肿瘤治疗的新策略
时间:2024-09-18 06:03:27 热度:37.1℃ 作者:网络
前言
细胞衰老是对潜在致癌刺激的反应,包括基因组损伤、强有丝分裂信号、致癌基因的激活、肿瘤抑制蛋白的异位表达和氧化应激。不同刺激诱导的衰老细胞(SNCs)具有一些共同特征:如细胞周期停滞、形态扁平化、细胞凋亡抵抗、异染色质变化、层粘连蛋白B1(LMNB1)缺失、CDK抑制蛋白的表达升高、衰老相关的β-半乳糖苷酶(SA-β-Gal)活性升高以及衰老相关分泌表型(SASP)的积累。
细胞衰老是一种公认的抗肿瘤反应,与化疗和放疗相比,治疗诱导衰老(TIS)已被证明是一种更安全的治疗策略。然而,衰老与肿瘤之间的关系非常复杂,越来越多的证据表明,尽管衰老在疾病早期有利于抑制肿瘤的发生,但衰老肿瘤细胞的长期存在往往会诱导肿瘤的发生、转移和复发。此外,衰老是一种不可逆的细胞周期停滞,肿瘤细胞的衰老逃逸是抗肿瘤治疗失败和肿瘤复发的重要原因。鉴于SNCs在促进肿瘤发展中的作用,及时清除SNCs在抗肿瘤治疗中至关重要。目前针对SNCs的疗法已经在开发中,这种方法的出现为抗肿瘤治疗,特别是衰老诱导治疗带来了新的机会。
细胞衰老对癌症发展的影响
大量研究表明,体内放疗和化疗都能轻易触发癌症细胞的衰老反应。衰老对肿瘤的发展是一把双刃剑:一方面,衰老的肿瘤细胞阻碍其增殖并分泌SASP,SASP可以将免疫细胞募集到肿瘤微环境(TME)中,由于其促炎性质而增强对肿瘤细胞生长的抑制作用。另一方面,SNC产生的频率随着年龄的增长而增加,而免疫系统的功能显著下降,尤其是适应性免疫,导致SNC无法及时清理。因此,它们在衰老的个体中积累,导致更高的概率患上与年龄相关的疾病和肿瘤。
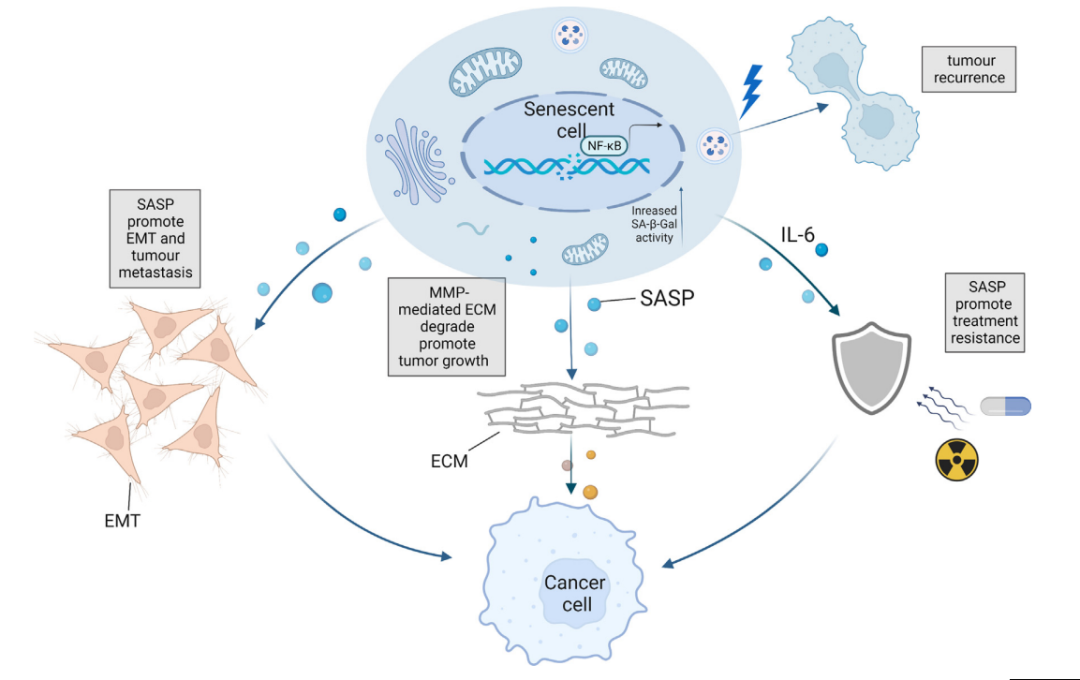
SNCs分泌的SASP是SNCs促进肿瘤发展的主要原因,基质金属蛋白酶(MMPs)和IL-6等也参与其中。基质金属蛋白酶可以处理和降解细胞外基质(ECM),释放支持肿瘤生长的细胞因子。衰老成纤维细胞可以有效促进乳腺癌细胞的上皮-间充质转化(EMT)。此外,MMPs也参与免疫抑制环境,SNCs中高水平的MMPs可以通过切割NK细胞上的NKG2D来支持肿瘤细胞,使其能够逃避免疫监测。此外,衰老内皮细胞产生的IL-6还抑制CD8+T细胞的免疫监测功能并促进髓源性抑制细胞(MDSCs)的募集。总之,这些结果表明,长期SNCs通过增强肿瘤侵袭、生长和免疫逃避,严重损害了药物疗效。
衰老细胞逃逸:治疗失败的帮凶
虽然SASP具有促进肿瘤发展的作用,但衰老逃逸可能是癌症治疗失败、肿瘤复发甚至人类癌症起源的关键原因。衰老的肿瘤细胞可以暂时进入休眠状态,鉴于大多数癌症治疗都以恶性增殖的肿瘤细胞为目标,衰老的肿瘤细胞在受到不同条件刺激时可以暂时逃避治疗并重新进入细胞周期。经历衰老逃逸的肿瘤细胞往往更具攻击性、干性和耐药性。
衰老逃逸的分子机制
SNC逃避衰老的机制多种多样,受细胞类型、组织来源、衰老诱导模式等影响,这充分反映了SNC的异质性。
目前对衰老逃逸分子机制的研究主要集中在表观遗传学上。肿瘤抑制因子,如视网膜母细胞瘤(RB)和早幼粒细胞白血病(PML)蛋白通过抑制几个转录因子E2F靶基因的表达来控制成纤维细胞衰老的可逆性,这些基因是重新进入细胞周期所必需的。E2F靶基因的长期抑制需要组蛋白H3在赖氨酸9(H3K9me3)的甲基化。通过组蛋白去甲基化酶如LSD1和JMJD2C消除甲基化修饰,或H3K9组蛋白甲基转移酶失活,可以逆转RAS/BRAF癌基因诱导的衰老黑色素细胞和治疗诱导的衰老淋巴瘤细胞的生长停滞。SETD1A是一种H3K4甲基转移酶,对维持有丝分裂和增殖至关重要。SETD1A的重新校准释放了S期激酶相关蛋白2(SKP2)的转录抑制,该蛋白降解p27和p21,从而触发衰老逃避。
p21对维持衰老表型至关重要。在致癌诱导的衰老大肠癌细胞中,p21WAF1失活导致细胞周期调节因子PLK1和CDC25的重新表达,恢复衰老肿瘤细胞的增殖能力。这些逃避衰老的恶性细胞依赖BCL-XL/ MCL1信号通路生存,使其成为衰老的靶点。p21的下调还导致Myc的表达增加,然后Myc与CD47启动子结合以抑制其表达,CD47是血小板反应蛋白1(TSP1)的受体。在三阴性乳腺癌症中,SNC产生的TSP1可以防止衰老逃逸。此外,在经历衰老逃避的肿瘤细胞中,TSP1和CD47水平降低。
另一项研究分析了SNCs衰老逃避代谢依赖的机制。谷氨酰胺耗竭被发现可以抑制大多数细胞系从治疗诱导的衰老中逃逸。此外,还有其他蛋白,如OLFM4和AGR2,也在衰老肿瘤的逃逸中起作用。
衰老逃逸的细胞形态
多倍体和衰老细胞之间有很多相似之处:两者都是由DNA损伤触发的,都具有相同的调节途径(p21、p53和Rb),更重要的是,两者都能够通过表达抗凋亡蛋白来抵抗细胞凋亡。尽管治疗诱导的SNCs是异质性和动态的,但DNA损伤剂诱导的SNC的一个共同特征就是多倍体,这表明衰老和多倍体是密不可分的。
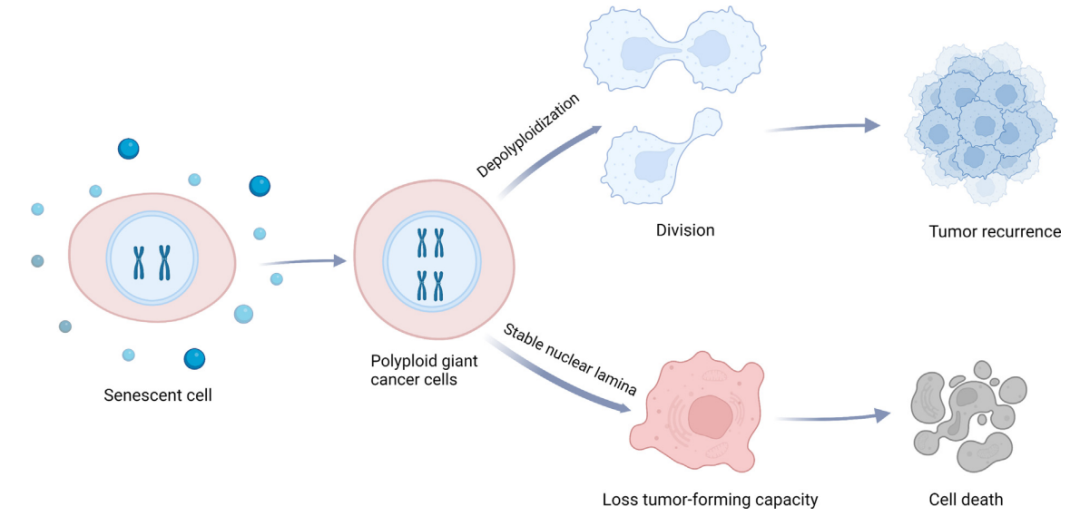
多倍体最初是阻止SNC进一步扩张的障碍。癌细胞可以经历有丝分裂滑移,导致细胞进入G1期,但没有完全完成有丝分裂和胞质分裂,形成巨大的多倍体多核细胞。最终,这些巨大的癌细胞停止复制并积累成多倍体SNC,而没有形成肿瘤的能力。
然而,多倍体细胞可以通过去多倍体化产生高度恶性的肿瘤细胞。研究表明,多倍体是有丝分裂活性细胞的来源,是肿瘤细胞逃避衰老的先决条件。这得到了多项研究的支持,例如阿霉素诱导的MCF-7乳腺癌细胞不形成多倍体,不能从衰老状态中恢复。
那么,衰老的多倍体细胞是如何进行分裂的呢?研究发现,SNCs在建立多倍体后,随后进行内胚层复制、染色体重排和进一步的无性分裂,以一种相当混乱的方式分布遗传物质,包括基因重编程、表观遗传调控等。最终,那些配备了必要DNA以执行其重要功能的后代将存活下来。经过存活选择后,存活的细胞通常更具攻击性,对基因毒性处理更具抵抗力。
衰老细胞治疗:一种协同抗肿瘤疗法
衰老细胞治疗是一种很有前途的针对SNCs的治疗方法。研究相对较新,并且存在许多不明确的机制。衰老细胞疗法主要包括senolytics和Senmorphics,它们都能发挥衰老抑制作用:Senolytics主要是选择性清除衰老细胞;而Senomorphics则是防止衰老细胞的有害细胞外部效应。
化疗和放疗通过不同的机制引起DNA损伤,并引发细胞衰老反应。细胞衰老治疗可以通过多种途径诱导SNC死亡,有些还可以通过诱导癌症细胞凋亡而发挥自身的抗肿瘤作用,从而提高治疗效率并克服耐药性。
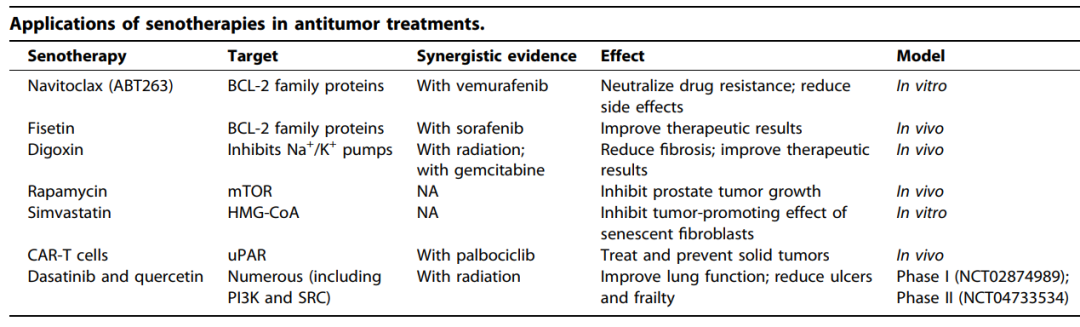
Navitoclax(ABT263)是第一批通过有效激活凋亡途径来清除SNC的衰老药物之一。Navitoclax可以选择性地清除衰老的黑色素瘤和癌细胞。当与选择性BRAF抑制剂vemurafenib联合使用时,navitoclax通过干扰BCL-2家族蛋白的功能来中和vemurafinib的耐药性。这扩大了vemurafenib的应用范围,为治疗BRAFV600E突变的癌症提供了一种很有前景的方法。
利用嵌合抗原受体(CAR)-T细胞也可以去除衰老的肿瘤细胞,提高抗肿瘤治疗的效率。尿激酶纤溶酶原激活物表面受体(uPAR)在SNCs表面大量表达,其在健康器官中不表达。实验观察到,当uPAR靶向CAR-T细胞用于治疗小鼠模型中的肺腺癌时,CD4+和CD8+T细胞的浸润增加。衰老肿瘤细胞的数量显著减少,肺腺癌小鼠的生存时间延长。
此外,雷帕霉素可通过抑制mTOR影响衰老成纤维细胞分泌SASP,其可抑制衰老成纤维细胞刺激小鼠前列腺肿瘤生长的能力。辛伐他汀是一种HMG-CoA还原酶抑制剂,通过抑制Rho家族GTP酶-Rac1和CDC42的活性来降低衰老成纤维纤维细胞中的SASP,并可阻碍衰老成纤维母细胞的促瘤作用。
除了抗肿瘤作用外,衰老细胞治疗也可以减弱多种促纤维化和促炎因子的表达,以抵消放疗和化疗引起的毒副作用。Navitoclax已被证明可减少化疗的副作用,如心脏功能障碍、骨髓抑制和疲劳,并可预防或延缓小鼠模型中的癌症复发。达沙替尼和槲皮素是最著名的衰老药,在用达沙替尼和槲皮素治疗时,去除SNCs并诱导肿瘤细胞凋亡,以减轻DNA损伤并维持组织细胞的增殖能力,从而减轻辐射诱导的溃疡。
小结
越来越多的研究表明,衰老细胞治疗可以作为一种补充疗法,在不影响当前有效抗肿瘤治疗的情况下,提高现有治疗的疗效,最大限度地减少毒副作用,克服耐药性,抑制肿瘤复发,甚至重塑免疫微环境。尽管仍然存在各种挑战,但随着我们对衰老理解的提高,衰老细胞疗法显示出非常有前景的应用,很可能在未来的临床中造福更多患者。
参考文献:
1.Senotherapies: A novel strategy for synergistic anti-tumor therapy. Drug Discov Today. 2022 Sep 14;27(11):103365


