【BJH】适合异基因移植的成人Ph+ ALL患者的管理
时间:2024-10-14 06:03:42 热度:37.1℃ 作者:网络
20%-30%的成人急性淋巴细胞白血病(ALL)患者携带费城(Ph+)染色体,历史上Ph+ ALL的预后较差,在没有异基因造血干细胞移植的情况下长期生存并不常见。而靶向BCR::ABL1融合蛋白的各种酪氨酸激酶抑制剂(TKI)的出现显著改善了预后,导致了许多适合移植的患者中有以下争议。

《British Journal of Haematology》近日发表综述,回顾了影响当代治疗的最新数据,讨论了上述争议,并提出了合理的治疗考虑。现整理主要结论供参考。
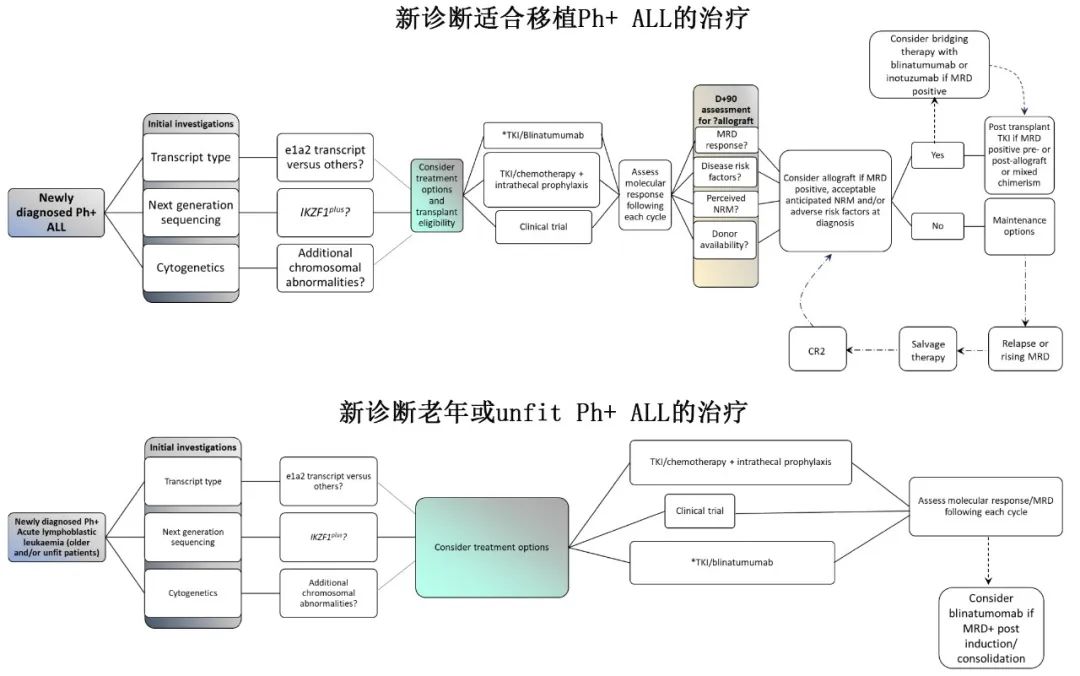
总结
•诱导治疗的最佳TKI:TKI联合化疗仍是年轻患者的标准治疗方案,因为单独使用TKI和类固醇似乎不太持久。Ponatinib似乎是最佳一线TKI,对应答患者使用减量方案。在成人中没有令人信服的数据表明达沙替尼优于伊马替尼,TKI一线治疗似乎都是合理的。
•对于计划进行异基因移植的患者,是否需要强化疗作为诱导的一部分?CALGB10701研究在异基因移植前使用达沙替尼-类固醇,未进行强化疗,但结局尚可。虽然这些数据仍有限,但对TKI-类固醇产生深层分子学反应的患者(特别是如果存在重大合并症)如果及时找到供者,就可以直接进行异基因移植。值得注意的是,GRAAPH 2014研究提示,大剂量阿糖胞苷“总体”改善患者结局,但其对移植患者的具体获益尚未得到证实。
•新组合:TKI联合贝林妥欧单抗的研究有足够随访且显示出良好效果,或许会成为标准治疗。该方案有可能使老年患者获得治愈,并有可能使年轻患者在 CR1期不再需要强化疗和异基因移植。避免强化疗的毒性可能导致后续异基因移植后的较低NRM,并具有移植物抗Ph+ ALL效应,从而有利地影响生存。奥加伊妥珠单抗在复发的 Ph+ ALL中具有良好疗效,可考虑作为多药诱导的一部分。
•CNS预防:目前的共识为使用鞘内预防,而不考虑初始全身治疗。使用大剂量全身甲氨蝶呤和阿糖胞苷进行晚期强化治疗的影响尚不清楚。晚期CNS复发仍值得关注。
•监测疾病状态:临床中最容易使用的是RT-qPCR,但替代转录本可能需要ddPCR。其他技术(如 NGS)如果可用,可能在检测MRD方面更敏感,并且联合使用时可能有助于区分CML样ALL和Ph+ ALL。评估Ig/TCR状态的技术可能有助于区分多谱系和淋系亚群,并确定影响异基因移植决策的MRD状态。
•诊断时具有不良预后因素的患者:分子学缓解和生存的不利因素包括IKZF1plus、p210转录本、附加染色体异常(特别是7号染色体单体)和WBC>100×109/ L。传统诱导方案多数无效,目前尚不清楚“传统”异基因移植方法是否可消除其风险。新型诱导策略如TKI-贝林妥欧单抗或结合INO、强化预处理,或可避免T细胞耗竭,使用“不全相合”供者、移植后TKI和/或奥加伊妥珠单抗以及在没有GVHD的情况下的预防性DLI等策略均具有吸引力,但很大程度上未经证实,这些重要的问题在未来开展研究解决。
•是否存在移植物抗Ph+ ALL效应?重要证据表明它是存在的,但在没有发生重度GVHD(足以影响NRM)的情况下,该效应是否可降低复发风险尚不清楚。
•在分子学CR1期进行异基因移植:目前而言,此时异基因移植对OS中没有任何获益,部分原因在于NRM。通过减少毒性诱导方案和改善 GVHD预防来减少NRM可能会改变这种平衡,但减少GVHD对复发的影响也是问题(下面进一步讨论)。对于诊断时无不良因素的患者,特别是年龄较大或有明显合并症的患者,推迟CR1异基因移植似乎是明智的。
•哪些分子学CR1患者应进行异基因移植?这是Ph+ ALL异基因移植中最关键的问题。尽管没有数据表明异基因移植对IKZF1plus疾病的预后有有利影响,但采用上述部分干预措施的异基因移植似乎对这些患者仍是合理方案。p210转录本和复杂细胞遗传学似乎也是合理指征。值得注意的是,尚不清楚这些高危患者达到分子学CR的频率;大多数患者可能达不到,因此他们自己会选择异基因移植。
•诱导/巩固后持续MRD阳性(由RT-qPCR定义)的治疗:对于这类患者,获得评估Ig/TCR状态的技术越来越重要;理想情况下异基因移植单位应可使用该技术。Ig/TCR阴性、BCR::ABL1稳定低水平阳性且无高危因素的患者可持续TKI治疗。适合移植的Ig/TCR阳性患者应进行异基因移植,但初步数据表明移植前近期阳性可能与较差的预后相关。如果这些患者之前未接受过贝林妥欧单抗治疗,则使用贝林妥欧单抗桥接这些患者似乎是一种合理、但未经证实的干预措施。
•RT-qPCR MRD阳性患者是否应使用贝林妥欧单抗桥接异基因移植?如果无法立即移植则似乎是合理的,但如果移植可以立即移植则不合理。
•供者选择:单倍体相合供者是合理的替代供者。来自亚洲中心的数据表明,接受异基因移植(供者并非相合同胞供者或无关供者)的MRD阳性患者的复发率较低,但需要在其他人种中进行评估,以及评估使用不全相合供者对GRFS的影响。
•预处理方案的选择:如果认为异基因移植适合MRD阴性患者且无高危风险因素,则减低强度预处理似乎是减轻NRM的合理方法,特别是在老年患者或有显著合并症的患者中。对于MRD阳性的异基因移植前患者,清髓性预处理可能更可取。TBI为基础的预处理对成人患者的获益尚未得到证实,预处理强度是否影响 IKZF1plus疾病的结局也尚不清楚。
•去T细胞?其可改善GRFS,但增加复发风险。去T细胞可能不是GVHD“低危”的高危患者的最佳选择。去T细胞后预防性DLI可能具有作用,不仅可用于新出现的MRD阳性,也可用于无慢性 GVHD且分子学缓解的高危患者。
•移植后TKI:尚无令人信服的数据表明其具有常规获益,但对于异基因移植前MRD阳性患者、移植后高危患者、持续或新出现的MRD阳性患者(下文将进一步讨论)以及存在混合嵌合(表明残留自体造血)的患者,使用达沙替尼或ponatinib是合理的。对于可耐受该治疗的患者,维持至少2年的MRD阴性可能是最佳的。Ponatinib是预先存在T315I突变的患者首选TKI。
•混合供者-受者嵌合:尚不清楚这是否是Ph+ ALL复发的显著风险因素,也不清楚不同水平的受体嵌合体对该风险的影响。然而在这种情况下,如果停用免疫抑制且无GVHD但混合嵌合体仍持续存在,则考虑预防性DLI是合理的。
•异基因移植后的分子学复发:选择包括DLI、贝林妥欧单抗、奥加伊妥珠单抗和对任何新出现突变有活性的TKI。目前还没有比较它们相对疗效的数据,谨慎的做法可能是最初仅使用其中一种治疗方案,在反应不佳时使用更积极的干预措施和联合治疗。
•未移植患者的形态学复发:初步报告表明,挽救疗法(ponatinib、贝林妥欧单抗、奥加伊妥珠单抗、CAR-T)单独或联合有效。关于后续异基因移植后反应者的特征和反应持久性,还需要更多数据,这对于适合移植患者延迟 CR1 异基因移植的决策至关重要。
参考文献
Shanmuganathan N, Grigg A. A critical review of management of allogeneic transplant-eligible adults with Ph+ acute lymphoblastic leukaemia. Br J Haematol. 2024;00:1– 15. https://doi.org/10.1111/bjh.19682


